 > Техника, страница 9 > Аккумуляторы электрические
> Техника, страница 9 > Аккумуляторы электрические
Аккумуляторы электрические
Аккумуляторы электрические,
источники тока, способные возобновлять после истощения свободную энергию посредством работы внешней эдс и т. о. возвращаться к начальному физ.-хим. состоянию. С точки зрения хим. динамики А. представляет обратимую систему, и именно обратимый гидроэлектрич. элемент. Восстановление свободной энергии такого элемента выражается накоплением на электродах продуктов электролитического распада. В теории гальванических элементов (смотрите) такое накопление, вторичный эффект эл.-хим. процесса, носит название поляризации. Вредное в обычных элементах, это побочное явление положено в основу службы А., называемых поэтому вторичными, или поляризационными, элементами. В принципе, всякий А. состоит из одного электролита, содержащегося в некотором баке, и двух электродов с клеммами. Согласно франц. терминологии, проводимой в настоящей статье, положительный электрод называется анодом, отрицательный — катодом (в американской литературе катод — положительная пластина, анод — отрицательная). Аккумуляторы различаются между собою химической природой электролита и электродов, формой и строением электродов, устройством бака и т. д.
I. Теория аккумуляторов.
I. Основные характеристики А. Всякий А. характеризуется рядом электрических постоянных, определяющих его ценность: эдс Е, разность потенциалов, или напряжение, U, среднее напряжение при зарядке
Г7С, среднее напряжение при разрядке Ud — все в вольтах; внутреннее сопротивление г в омах; емкость Q в ампер-часах или в кулонах; мощность Р в ваттах; энергия W в ватт-часах; кобфф. отдачи (электрическая, количественная отдача) η9; кпд, или энергетическая отдача, η№ наконец,
коэфф. понижения — Я. Эдс есть разность потенциалов на клеммах незамкнутого А. и называется также незамкнутым напряжением. Напряжение U при прохождении тока силы I через замкнутую с А. цепь связано с Е соотношениями:
| при зарядке
UC=E+Icre, |
ω |
| при разрядке
Ud=E-Idrd, |
(*) |
| где г — сопротивление А. Среднее напряже- | |
| ние за промежуток времени т от дается соотношением: | 0 до i |
| при зарядке
— 1 гТ |
(3) |
| при разрядке | |
| Vi=^rfTi Vidi.
1 dJ О |
(4) |
Емкость Qe А.—количество электричества, которое поглощается при зарядке А., а емкость Qd — количество электричества,
| при | разрядке: | |
| О | (5) | |
| II
ча О |
ад“ J 0 | (fi) |
Мощность Р на клеммах при данном режиме разрядки:
рс= ад. (7)
Энергия Wc, поглощаемая при зарядке:
Т!
ад“·
(8)
При зарядке или при разрядке постоянным током эти выражения [по ф-лам (3) и (4)] дают соответственно:
п;=адг,., (9)
Wd=UdldT,
(10)
Коэфф. отдачи электричества »7? есть отношение между количеством электричества, отданным при разрядке, и количеством электричества, поглощенным при зарядке:
4 =
| Qd Qi τ,ι | f.b* |
| Qo | /ад |
(11)
Коэффиц. отдачи энергии >?w есть отношение энергии отданной к энергии поглощенной:
{*Т
Wi. ViIiTd _J „ Vihdr
i г.
’ d 1 d d
Uti Ie Tc
rT
(12)
Коэфф. понижения λ есть отношение среднего напряжения при разрядке к среднему напряжению при зарядке:
TJ, fT,d Uddt
ив
(13)
и„ dr
Принимая во внимание ф-лы (11), (12) и (13), находим соотношение между тремя коэфф.
4n,= Vq); (14)
справедливое при постоянном токе, одинаковом для разрядки и зарядки.
2. Общие для всех А. технические условия.
Ко всякому А. с помощью характеристик π. 1 могут быть предъявлены следующие принципиальные требования, вытекающие из самого понятия о его технической функции (смотрите табл. 1):
ным и группируя вместе разрядки с значительными промежутками, можно дать непрерывное распределение по двум путям, идущим от нулевой интенсивности разрядки к некоторой максимальной (фигура 1, А). Наглядной оказывается секторальная диа-
Т а б л. 1. — Схема общих технических условий, предъявляемых к А.
Удельная энергия большая
(
I
Эдс высокая
Хим. реакции весьма экзотермичны Катоды из материала, весьма электроположительного
Эл.-хим. эквиваленты малые Удельная емкость большая !
V Вес неактивных поддержек малый
Отдача энергии высокая
Разность потенциалов при зарядке и разрядке возможно постоянная
i Обратимость сколь возможно совершенная < Внутреннее сопротивление г малое I Коэфф. понижения λ близкий к единице
Длительное сохранение за- | 0тсутствие
местных действий
Себестоимость эксплуатации небольшая
ί
Стоимость обзаведения небольшая
Содержание недорогое
Стоимость исходного сырья мала г Выработка простая Рабочий труд небольшой
Составные части долговечны Замена изношенных частей легкая
3. Функциональная классификация А. устанавливается в зависимости от различных типов разрядного режима их и учитывает электрич. характеристики, наиболее рационально обеспечивающие службу аккумуляторов при данном режиме, причем известные пункты принципиальных технических условий (п. 2) утрачивают свою жесткость. Процесс разрядки А. характеризуется приложенною к цепи разностью потенциалов Ud, количеством прошедшего через цепь за все время разрядки электричества Qd и силой тока Id. Отсюда основное деление А. на три группы: на А. напряжения (группа V), А. емкости (группа q) и А. тока (группа г). Группы v и г могут рассматриваться как крайние типы, а группа q — как лежащая между ними. Батарея Планте, дававшая шаровую молнию, и батарея Капицы, позволившая получить магнитные поля огромной напряженности,— таковы крайние пределы, достигнутые типами V и г. Процесс разрядки А. сопровождается попутными медленными накоплениями и перемещениями электрических масс. Поэтому, разделение всего процесса разрядки на отдельные, отстоящие друг от друга во времени промежутки значительно изменяет характер разряда и служит основанием для дальнейшего подразделения функциональных типов. Тут вводится в каждом типе группа постоянного действия и группа перемежающегося действия, с дальнейшим подразделением последней на подгруппы с промежутками работы длительными и подгруппы с промежутками работы кратковременными. Т.о. устанавливаются де-вять принципиальных типов (смотрите табл. 2). Практически эту классификацию можно несколько упростить, т. к. общая продолжительность разрядки обычно невелика, а кратковременные перерывы имеют малое значение и отражаются лишь на средней силе тока. Относя такие разрядки к постоян-
грамма (фигура 1, В,В,Г),тем более, что в некоторых случаях применения от А. требуется соединение функций двух смежных секторов.
Таблица 2.—Ф ункциональная классификация типов А.
Типы аккумуляторов
| Действие | напря жения | емко сти | тока |
| V | q | г | |
| Постоянное .. | VI | «i | {ι |
| i с промежутка-1 ми кратковре- | |||
| Перемежа-1 менными. | vn | «II | *11 |
| ющееся | |||
| 1 с промежутка-1 ми длительны-1 ми. | vm | «III |
4. Химическая классификация А. В табл. 4 перечислены лишь те обратимые пары, которые хотя и не усвоены промышленностью, но могут притязать на практическое значение.
5. Описание физ.-хим. процессов в А. Разрядка и зарядка свинцового А. характеризуются графиком (фигура 2), причем как разрядная, так и зарядная кривые претерпевают три последовательные стадии (табл. 3).
Этим трем стадиям соответствуют характерные видимые явления: в заряженном А. катод имеет серо-металлический вид и состоит из губчатого свинца,тогда как анод покрыт перекисью свинца РЬ805 интенсивного черного цвета, нестойким, сильно окисляющим веществом с значительной электропроводностью. Внезапное понижение стадии I разрядки происходит от уменьшения концентрации кислоты в порах активной массы, после чего концентрация выравнивается диффузией. Стадия III разрядки связана со вторичным уменьшением концентрации кислоты. В разряженном А. анод состоит из двуокиси свинца РЬОа,
Стадия
ί I
Зарядка
Разрядка
Занимает короткое время.
Сперва разность потенциалов быстро подни- Сперва разность потенциалов очень быстро мается над значением, соответствующим плот- падает до 1,9 V. Это т. н. coup de fouet.
ности электролита 2 V, а затем падает до 2,1V.
II
III
Занимает наибольшую часть.
Разность потенциалов медленно возрастает, I Разность потенциалов медленно убывает, при-приблизительно до 2,2 V. I близительно до 1,85 V.
Занимает сравнительно небольшое время.
Разность потенциал ов довольно быстро возра- I Разность потенциалов быстро падает, причем стает до 2,8 V п затем падает до 2,5—2,6 V. | кривая претерпевает изгиб и стремится к нулю до 1,2—1,1V. В стадии III разность потенциалов быстро опускается до 1,2—0,75 V и, продержавшись короткое время на этой
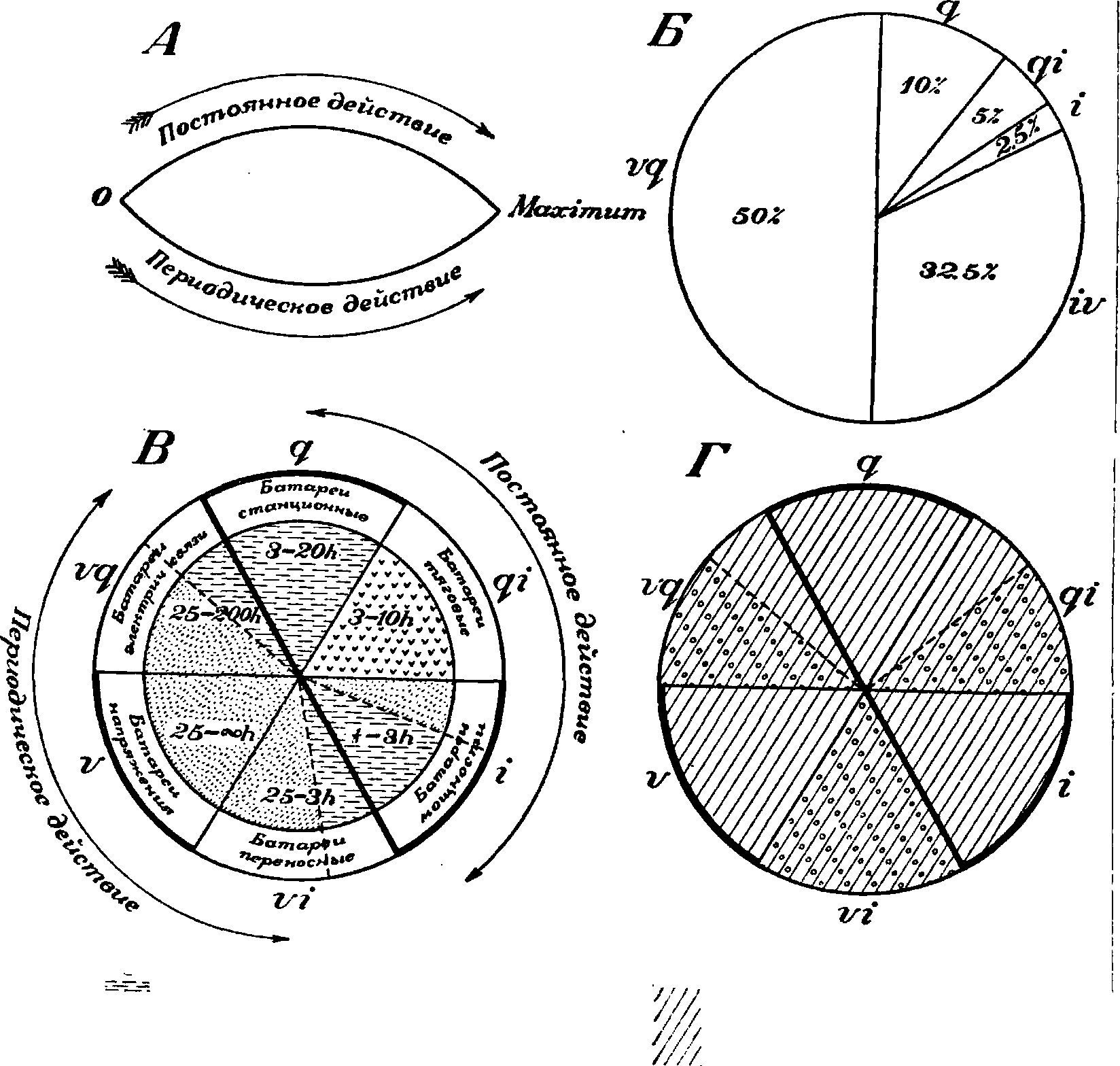
qj Поверхностные электроды
Пастированные электроды массовые
Пастированные электроды ·-· тонко-решетчатые
Область применения, свинцовых А.
Область применения щелочных А.
Фигура 1. Диаграммы функциональной классификации А.
вещества бурого цвета, с уд. сопротивлением в 22 раза большим, чем у перекиси свинца Pb2Os. Катод состоит из недокисного сернокислого свинца Pb2S04, вещества темносерого, почти черного цвета, обладающего значительною электропроводностью и весьма нестойкого.
Уд. в электролита падает от уменьшения концентрации кислоты как раз в количестве, потребном для образования на катоде недокисной сернокислой соли. Оставленный в бездействии незаряженный А. гибнет («сульфируется»,
«су л ьфатируется»), причем и катод и анод покрываются окисным сернокислым свинцом PbS04, веществом белого цвета, электронепроводящим и стойким. При этом концентрация кислоты опять падает. При зарядке А. с пластинами, не подвергшимися побелению, катод вновь принимает серометаллический цвет, анод чернеет, а кон-центрац. электролита повышается. Зарядные и разрядные кривые свинцового А. не совпадают между собой, и площадь между ними выражает потерю энергии на цикл зарядки и разрядки. Однако совершенное смыкание кривых доказывает, что в А. не происходит побочных реакций и что его можно рассматривать как элемент с почти совершенной обратимостью. Потеря энергии примерно в 20—30% объясняется разностью концентраций на электродах, причем 60—70% потери падает на анод, а 30—40% на катод.
Разрядка и зарядка щелочного А. представлены графически на фигуре 2. Разрядка проходит три стадии: в стадии I разность потенциалов быстро падает до 1,5—1,4 V. В стадии II происходит медленное падение высоте, резко падает. При разрядке происходит некоторое увеличение концентрации электролита, однако незначительное, в виду большого объёма жидкости. При зарядке наблюдаются две стадии: I — быстрый подъем разности потенциалов до 1,7V; II — медленный подъем до 1,9V. Кривые зарядки и разрядки хорошо смыкаются, так что щелочной железоникелевый А. обладает хорошей обратимостью. Отдача энергии >?w=45—55%, а отдача электричек ства yjq=60—80%.
6. Химическая теория А. Согласно т е-ории Фери, заряженный свинцовый А.
| Изобретатель | Общий характер действия обратимой пары | Вещества, составляющие обратимую пару | Хим. реакции обратимой пары | ||||
| типа и дата изобретения | элек- | электро- | |||||
| тро- | анод | катод | лит | анод | катод | + - + | |
| ЛИТ | |||||||
| I стадия: | |||||||
| Планте, 1895 г. | X | £ | Нера ство рим | •г о
СО в |
О
м ХЗ Λ |
Свинец
РЬ |
PbaOi+HaSO1+Pba^2PbOa+HaO+PbaS01II стадия:
Pb0a+2HaS04+Pb^;PbS04+2Ha0+PbS0« |
| Я | ев | ев | |||||
| Рейнье, 1888 г. | я | £ | h
О |
ег я | Цинк
Zn |
PbaO4+HaSO4+Zn^;2PbOa+HaO+ZnS04 | |
| я | а | ч | я | ||||
| Коммелен, | О | X | Кадмий
Cd |
||||
| 1892 г.; Вернер, | X | Я | В
X |
х | Pba0t+HaS04+Cd^2Pb0a+Ha0+CdS04 | ||
| 1896 г. | ев | X | |||||
| Рейнье | X | с. | св
X |
Й
X X |
Медь
Си |
Pba0t+HaS04+Cu^2Pb0,-|-Ha0+CuS04 | |
| X | а | а | Сурьма | 3Pb,06 + 3HaS04+2Sb"^6Pb0a + 3Ha0-(- | |||
| Дарриз | 4 | X | м | Sb или | +Sba(SOt). | ||
| н | о | о | Висмут
Bi |
3Pba04+3HaS04+2Bi^6Pb0a+3H.0 + | |||
| Я | + BMSO,), | ||||||
| X | CuO + 2KOH+Zn^Cu+H,0+Zn(OK)« | ||||||
| Коммелен, | ь* | Едкое ка- | а | Цинк | 1 | ||
| В а дел ь, Энтц | ли КОН | ® о | Zn | Цинкат | |||
| X | св | н | go | калия | |||
| Эдисон | Едкий натр | я к о | Кадмий | CuO+NaOH+H.O+Cd^; | |||
| а | о | NaOH | Cd | ^Cu+NaOH+Cd(OH)a | |||
| NiaO,+2KOH+ Zn ^2NiO+HaO+Zn(OK), | |||||||
| Кригер, | Н | св | Едкое на | η
о |
I 1 1 | ||
| 1896 г. | О | X | ли КОН | £
я « аз Я |
d
S3 |
Окись Закись Цинкат никеля никеля калия | |
| Михаловский, 1900 г.; | ев | к | Οι | Едкий | X | NiaO, + 2NaOH +Zn*”2NiO +Н.0 +Zn(ONa)·
1 I i | |
| Эдисон, | натр
NaOH |
Я
Я |
№ | Окись Закись Цинкат | |||
| 1900 г. | X | Η | никеля никеля натрия | ||||
| Ра ство рим | Нера ство рим | Щелочные | я | ||||
| Лащинский
• |
карбонаты цинка
Zn |
X
О |
ЕГ | NiaO„+ZnCOa+6NaOH +Zn^ X2NiO +NaaCO,+3HaO +2Zn(ONa)a | |||
| I стадия: | |||||||
| О
н |
AgaOa + 2NaOH +2Cu^~AgaO +2NaOH +CuaO
I I | ||||||
| Юнгпер, | 2
и |
£
а |
Едкий натр | Перекись серебра | Медь | 1 1 Окись Закись серебра меди | |
| 1899 г. | х | а | Од | NaOH | AgaOa | Си | II стадия: |
| я | о | О | AgaO +2NaOH +Cuaot;Aga+2NaOH +2 CuO | ||||
| я | X | X | 1 1 1 | ||||
| X
£ |
н | 6ч | Окись сер. Закись меди Окись меди | ||||
| св | св | I стадия: | |||||
| Эдисон, | Я | & | а | Едкий | Окись | NiaOa3HaO+2KOH+Fe^2Ni(OH)a+2KOH+ | |
| 1901 г.; | X | X | натр NaOH | никеля | Железо | +Fe(OH)a | |
| Юнгнер, | я | к | в | или едкое | NiaOa | Fe | II стадия: |
| 1901 Г. | кали КОН | NiaOa3HaO +КОН +2Fe(OH)a^2Ni(OH)a + | |||||
| + KOH+FeaO,+HaO | |||||||
| и | Хлорист. | ||||||
| цинк | Платина | Платина | |||||
| i | К | £ | я | Бромист. | Уголь | Уголь | |
| £9 | X | X | цинк | ||||
| Писка, Шюмо, | X | св | Хлорное | Пл&тини- | Платини- | ||
| Россе, | X | ев | железо | рованное | рованное | ||
| Пуанкаре | ев | и | « | Хлористое | серебро | серебро | |
| X | серебро | ||||||
| Галоиды | Ртуть | Ртуть | |||||
| X | (0 | <?> | щелочных | Hg | Hg | ||
| н | X | металлов | |||||
| Грове, | х | ев | св | ||||
| i 1893 г.; | X | & | а | ||||
| Нальете, 1894 г.; | н о | X | X | Вода
НаО |
Кислород
Оа |
Водород на | Ha+HaO+0^211*0 |
| Коммелен, | В | и | |||||
| 1900 г. | >» | ||||||
ОБЩАЯ ХАРАКТЕРИСТИКА ОБРАТИМЫХ ПАР.
| Электрич. характеристика разрядки | ОСНОВАНИЯ ОЦЕНКИ | |
| Выгодные стороны | Невыгодные стороны | |
| I стадия: напряжение быстро падает с 2,1 до 1,9V, затем медленно — до 1,85V.
II стадия: напряжение быстро падает до 0. |
Высокие эдс и уд. емкость. | Значит, местн. действия, вследств. чего при наийучш. уходе теряется до 1% емк. в день. Легкость суль-фации. Необходимость тщательного ухода. |
| I стадия: напряж. падает быстро с 2,8 до 2,5V. затем медленно с 2,5 до 2V и снова быстро с 2 до 0,6V.
II стадия: напряж. медленно падает с 0,6 до 0,4 V, затем быстро до 0. |
Эдс и уд. емк. > чем у Планте. На 1 Ah потребно 1,21 г цинка. | Катод разъедается при незамкн. цепи, амальгамир. лишь частично устраняет местн. действия. Осадок цинка падает с катода. |
| Уд. емк. > чем у Планте и Рейнье. | Неудобства те же, что у Рейнье; кроме того, Cd дорог. | |
| Среднее напряжение 1,25V. | Уд. емк. > чем у Планте. На 1 Ah потребно 1,17 г меди. | Катод разъедается при незамкн. цепи. Уд. энергия < чем у Рейнье. |
| Напряжение 0,75V. | Уд. емк. высокая. | Уд. энергия<чем у Планте. Кпд мал, т. к. катод растворим; местные действия усилив, осаждением на цинке меди, несмотря на пористые 1 перегородки. |
| Образующ. окись Cd нерастворима, электролит не изменяется и катод не растворяется. | Растворимый гидрат окиси меди дает осадок меди на Cd, почему возник, местн. действия. i
i | |
| Эдс 1,85V; среднее напряжение 1,65V при разрядке в 2 часа и 1,70V для разрядки в 3 часа. | Уд. энергия 30 kW на 1 килограмм полного веса, то есть не меньше, чем у Планте. | Местн. действия меньше, чем у j Рейнье, но на цинке осаждается ни- ] кель, и активн. вещество т. о. те- i ряется. Цена никеля выше, чем меди.,
1 |
| !
1 1 j | ||
| Эдс 2,1—2,2V. | Цинк не растворяется в электролите. | Никел. анод разъедается бикарбо- > натом, никель осаждается нацинке, [ почему—значит, мести, действия. j |
| I стадия: эдс 0,93V.
II стадия: эдс 0,65 — 0,7V. |
Высок, уд. энергия—4 0—5 0 kW на 1 килограмм полного веса. Длит, сохраняемость заряда. Отсутствие мести, действий. Долговечность аккумулятора. | Высок, цена исходн. материалов. |
| I стадия: напряжение быстро падает от 2,1 до 1,5—1,4V.
II стадия: медл. пад. до 1,2—1,1V. III стадия: быстрое падение до 1,2—0,75V и затем снова быстрое падение до 0. |
Отдача электричества 60 — 80%. Отдача энергии 45 — 5 5%. | j
i |
| Эдс 2,14V.
Эдс 1,8V. Эдс IV. Эдс 1,85 V (для Na Л. |
1
1 j 1 | |
| 1
Напряжение 1,2—1,3V. |
При золот., платин. или паллад. губч. электродах уд. емк. значительна: 5 6 Ah на 1 килограмм платины и 170Ah на 1 килограмм губч. палладия. | При атмосфер давлении запасенная уд. энергия весьма мала. При повышенном давлении электроды из серебра, ртути, олова и никеля растворяются. Золото, платина, палладий очень : дороги. Баки тяжелы и громоздки. ! Обратимость очень несовершенна. | Коэфф. понижения весьма мал. |
представляет собою систему из губчатого свинца РЬ на катоде и перекиси свинца РЬ20?на аноде, погруженную в раствор серной
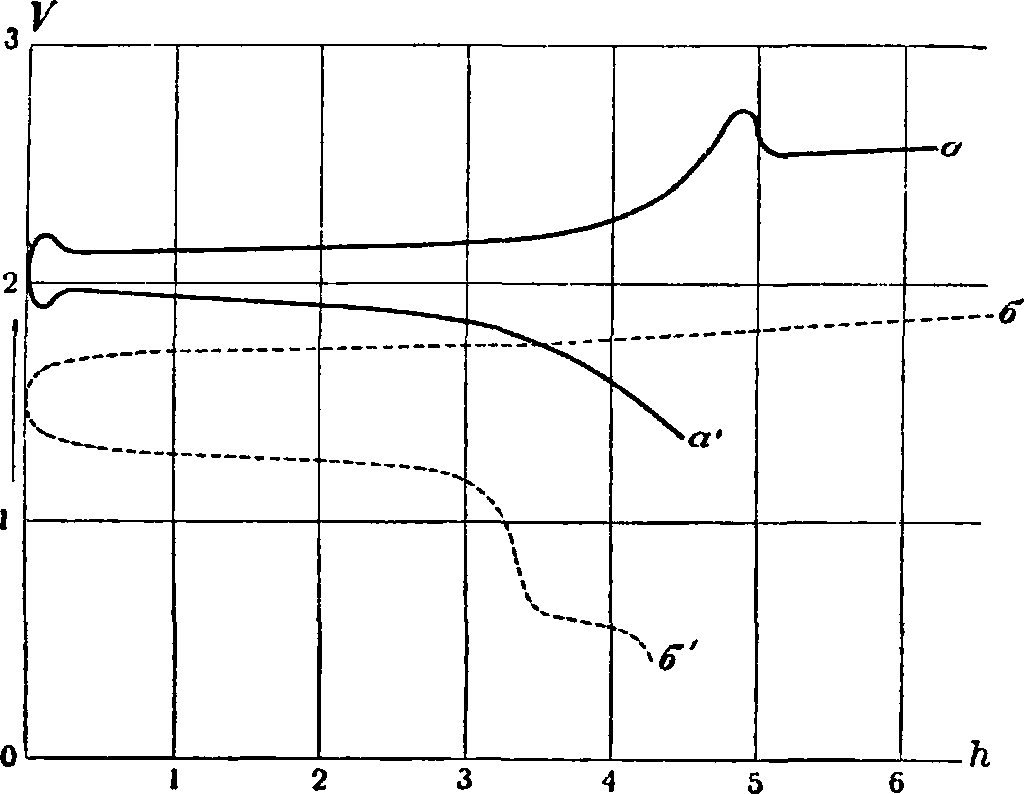
Фигура 2. а — зарядка свинцового аккумулятора,
«—разрядка свинцового аккумулятора, б—зарядка щелочного А. Эдисона, 6—разрядка щелочного А. Эдисона. кислоты H2S04. При разрядке такая пара действует подобно всякому другому гальваническому элементу с сильным деполяризатором, а именно: свинец разъедается серной кислотой, давая недокисный сернокислый свинец Pb2S04, соответствующий недокиси свинца РЬ20; освобождающийся же водородный ион направляется к аноду, отнимает от перекиси часть кислорода и превращает ее в двуокись свинца РЬ02, сам же дает воду Н20. При зарядке, наоборот, водородный ион разлагающейся воды направляется к катоду и, отнимая ион S04, восстанавливает металлический свинец, а сам дает серную к-ту; кислородный же ион окисляет двуокись свинца РЬ02 на аноде в перекись РЬ205. Химическую схему реакций свинцового А. по Фери дает табл. 5.
свинца, причем и тот и другой переходят в окисный сернокислый свинец. Ход реакций таков:
на катоде.. Pb+H2S0,+0 PbS04+Hs0 I
на аноде. PbIS04-i-H1!S0,+0 2PbS04+Hs0 ΙΓ
Это и есть процесс сульфации или сульфитации, разрушающий электроды оставленного незаряженным А.
По теории сульфации Гладстона и Трай-ба, господствовавшей до последнего времени, анод заряженного А. состоит из двуокиси свинца РЬ02, а катод — из губчатого свинца РЬ2. В процессе разрядки вещества катода и анода сульфируются, то есть переходят в окисный сернокислый свинец PbS04, согласно ф-лам I и II.
Химическая теория щелочных железо-никелевых А. В изготовленном виде щелочной А. имеет катод из железа, анод из двуокиси никеля Ni02 и электролит из 20%-ного едкого кали. Реакции этого элемента недостаточно изучены, и неизвестно, соответствует ли это исходное состояние элемента какой-либо из стадий дальнейшего эл.-хим. процесса. Наиболее вероятной м. б. признана схема реакций, представленная в таблице 6.
Юнгнером, Гиббертом, Цеднером и Фер-стером даны также и другие схемы реакций, но в виду невыясненности продуктов, образующихся в железоникелевом А., этих схем мы не приводим.
7. Классификация свинцовых А. При классификации свиьцовых А. существенно отметить различие электродов: электроды большой поверхности, типа Планте, или пластины поверхностные, и электроды с наведенными оки, типа Фора, или пластины пастирован-н ы е. Дальнейшая классификация основывается на более частном подразделении тех и других (табл. 7).
| Таблица 5. — | Схема | реакций свинцового А. | п 0 | Фери. | |||
| Катод | Электролит | Анод | Катод | Электролит | Анод | ||
| РЬ2 + | H2S04 + | +
РЬ205 |
разрядка
------у |
Pb2S04 | + | н2о + | +
2РЬ02 |
| Губчатый свинец | Серная кислота | Перекись свинца | зарядка | Недокисный сернокислый свинец | Вода | Двуокись свинца | |
Наряду с этим основным процессом могут происходить как на аноде, так и на катоде, под действием кислорода из воздуха на разрядившийся А., различные реакции, заключающиеся в окислении не-докисиого сернокислого и металлического
Электроды поверхностные (фигура 3,4). Чтобы получить сравнительно быстро достаточную емкость, приходится возможно более повышать удельную поверхность электрода, то есть отношение поверхности к массе. Этого достигают, увеличивая
Таблица 6. — Схема реакций щелочного никелевого аккумулятора по Жюмо.
| Катод | Электролит | Анод | |
| — | + | ||
| i N i 203 3H20 | + кон + | Fe | |
| ag J
<D >· |
I Гидрат окиси | Едкое | Металлич. |
| Ко | 1 никеля | кали | губч. железо |
| *Й 1 | , NiaO, ЗНгО | + КОН + | Fe(OH)2 |
| S <и * 9ή i g* 1 | 1
1 Гидрат окиси |
Едкое | Гидрат дву- |
| cq о | никеля | кали окиси железа | |
| Катод | Электролит | Анод | ||
| разрядка | — | + | ||
| -у
Ч-- зарядка |
2Ni(OH)2
Гидрат двуокиси никеля |
+ КОН
Едкое кали |
+ | Fe(OH)2
Гидрат двуокиси железа |
| разрядка
-> ч-- |
2Ni(OH)2 | + КОН | + | Fe203 ЗН20 |
| зарядка | Гидрат двуокиси никеля | Едкое кали | Гидрат окиси железа | |
i
I
I
Электроды с большой поверхностью (Планте)
Электроды с наведенными оки (Фор)
I
Автогенного образования
Смешанные пластины
Решетчатые поддержки
Различные поддержки
( Полученные I С сердечником I отливкой i Без сердечника Однородные <
I Полученные I Единственная I механически пластина
Разнородные |
Различные соединения, полученные отливкой или механически.
(Простые решетки; решетки с корытцами; решетки из двух частей; двойные специальные решетки; рамки, пластины из массы; двойные решетки цельные поверхностное развитие электрода, то есть отношение действительной поверхности к плоскости проекции наружного контура электрода. Поверхностное развитие литой ребристой пластины достигает 6—10, далее 12, а у пластин, фабрикуемых прокаткой или нарезкой, развитие поверхности достигает 12—15. Однако такое развитие не полезно, т. к. узость зазоров между ребрами затрудняет диффузию электролита, а самые ребра, олень тонкие, быстро разрушаются. На практике 1 дм2 развернутой поверхности дает емкость 0,5—1 Ah. Пластины большой поверхности прессуются иногда также и из проволок, лент или зернышек. Распет электродов болын. поверхн. массы М делается по ф-ле:
8-Щ™, (15,
где S — активная поверхность в дм2 электрода, состоящего из пластинок толщ, h миллиметров, или проволок диам, к миллиметров, или зернышек поперечником h миллиметров; к — коэффициент, равный 1—для пластинок, 2 — для проволок и 3 — для зернышек. Толщина пластинок не делается менее 0,5 миллиметров, а число пластинок на 1 см—от 7 до 14. Чтобы избежать коробления электродов, Пфафф располагает пластинки под углом в 45°. Пластины большой поверхности делятся на однородные, сформованные целиком из чистого свинца, и разнородные, состоящие из системы механических поддержек и электрически соединенного с ними свинца, дающего большую поверхность (ленты, проволоки ит. д.).
Электроды пастированиые (фигура 5, 6, 7, 8). Фор устранил необходимость развития поверхности электрода и процессов формования, помещая в электроды при самом процессе их изготовления пасту из веществ, которые помощью легкой дальнейшей обработки превращаются в пористую массу, тождественную с продуктами формования поверхностных электродов.
Селлон усовершенствовал пастированиые электроды, указав конструкцию свинцовой основы электрода, предотвращающую выпадение пасты. Наконец, Фолькмар увеличил прочность этой основы, заменив чистый свинец сплавом его с сурьмою, более прочным механически и не-разъедаемым химически. Дальнейшие усовершенствования касались формы этой основы из сурьмянистого свинца, причем одни конструкторы от первоначальных решеток перешли к сплошным пластинам с желобками, а другие— к простым рамам, заполняемым крупными пластинами (например
30×G5 миллиметров и даже 90x130 миллиметров) из одной только пасты (так назыв. рамочные пластины или масс о-вые пластины), или далее совсем без рам.
Пластины Тюдора,
Поллака и др., в которых сочетается большая поверхность с па-стированием, сперва работают как пасти-рованные; по мере разрушения и выкрашивания пасты, происходит формование

Фигура 5. Наиболее употребительная простая решетка. свинцовой поверхности, возмещающее потерю емкости, и под конец электрод работает как поверхностный (фигура 9).
Катод и анод изнашиваются в А. от различных процессов. Поэтому в настоящее

Фигура 3. Поверхностная однородная пластина Тюдора, полученная отливкой с 14 ребрами на 1 см.

Фигура 4. Поверхностная однородная пластинка Пфаффа, полученная отливкой, с ребрами, наклоненными на 45°.

.[J .A .A ыищиф миптолгл аышишочитэки п интэшоД .0 ,ιιιΦ
-пл πππικγπιο,ιιιιοη то ытоомпопяяя я .ядотдл н
-уплмяя ХУ ЯД ЯП ·£Μ9Τ0Μ

-j;r.ir iicimomwO .0 лнФ -iniyiiuii ,ι;οι;ι,ι,ι>Π laurr»
. ШЛТГ.ИИфТ iiuniioiij, iu,ii
о ппншрпкоолI ллтог.О oqqT, ypoq/nanii хит -П9ЯТ90ДЖ0Т М уТ^Д
мор iiqn ,11 ы I .А хин -oqTHOr.e тнлддодоо I
НЩ^[ТН9ДПОЯ тпг. .11 МОР. П9ШЯГ.00
т 11 д о я i«гя л о г, η а. о ко)’., г i гл о о р им я i ш д о i л q о т
-УГ) ЯМ9Т9П0 НТО OTP -qouc лтяяядто тот, -unqiJH topo як опп
-ЯДТПОДПОЛ 1ШПЯЯ1Ш -JiT уЯЯГ.ОЛООИ ,ШЦ1
-тондиеояохдюо ноаол .Ш ЛЮТ МОШЮРЧДЫЯ ко -уГ) I ,опя1У)Тняодог,’3
.KOdTKVKm.jTKq тчд .0 .Т ,11 KfTKnqfiH -!,!Я ядоютО. ДДЛ < ΓΛ ЯТ0ОШЮИЯЯ8 КОТИДОЯ -([ОДОО то (γΓΛ) о до ЮТОГ.ОДЛ-^ миллиметровялс /ЛиУГЛвГ.ОМЫЯДТ я 1ЮК.ЯД1О1ГШ0М811 ,Д ЯП
: .οι лю .адодтлог.о нтлоптодр Я .iioqyTnqoiiMOT о
(01) 48i0O,lAf4SI(lSlr0 + TrG.r ----- °0 iiqn
(Γί) д1 о!,0-|-SG, t ^ (Ά °8t iiqn
ятоо мтог.онл шдп^тпчддол ошюпомнИ кнпялод л я VI .A LiToonq цотляф шлпллха ο,Όί· (ΤΟ,i) .А оде ιίοιικυιι ян ,лодясог.оД II iivioqon онпог.яопятоооя яд топдян (V 8,0) -oqn яп — (ΤΙ-,Ο) о ()^, ндииао ошюг/шло и -оппдооо οι,π .omioiKjoo я покоило oinionmqa ог/ппюпдядтподнол яп— (V 8.0) <До1 н миллиметров ллтог.онл анод
-г.глоЭ ,с то о д е я т о о и и о п я и V.
U πΓ.ΠΡΙίΙΙ КПЛООРПМЯПНДОМДОТ МНДЮО оно
-око нмыптпокяахуяд о qim xwMimiqoo КОТЮНКЯДИЯ .А олояоднняо оде длмдтпом хпоОо ыпптояпп топшддооо .А а кмодя
-ПГ.00 Ы1ШТ0ЯКП ЯДОПЯ КГ.Д RKIIOMIiqn, попит
,οίοτ oMoqn .ошюяонлыоо .iiTOOHxqoaon ίιοιπ
, С.—г- ~
—С—
”ΊΤ
I
r~v
=¥11
itz
ж
.j;ini;q<l> mirirnoq ненлгол пкиГтлД,. T лнФ
-oq — ядотнл кпд я ,(qor,oiT) оидиднодитоид
.^.1 4
-от Гютооптокп oHtior.oqoqnonq ooiiriniiauqll УДЛЮМ НОДОПЛ и мошюдюмм котол штоод ял ;пкядотля 1 -г i -оддяд оог.оилял
-ОШОПТО ОПЯКЯН HToOHxqoaon θιιη -on л яодопя -отял iiTOOirxqoa V. : Si л ял, аод .(пдоФ)
-йоаээыдоЭО .8 xiaao^JHNaa вата -и о п а я С .А .д - .с ятоо и
-ПОТОП II ы г. п о -Л У П С Я Г. Я И д т о я о д о q т -я q Т II 9 Д II о л -о Г. О II Л II II JI 0П9ГЛ.10Н ЛТОУ 1ШЯТ1.НЮ Ш/ЛЛ1Ш9П911Р0Л0н1/1 ЛЛ Т
ядоня аокшцшотоп члелят я, оде oiiiifiTonqnoa
I
Л
ь*
fp/pppA,
I · I * i “. I * ’ I
^ * ША * i ’ ш
Jf rfWirty^SSf/Y/JSSJ^
Ί- Y/?/ss////s//^/fy-ss/s7/^//s/Ys; vs.
- HTM i; 11 ni;TJ;ifT)iiri4. И лиФ
соотношением Гельмгольца (смотрите чес-кие элементы):
Qc jlE
Е =
23 000 +
Гальвани-
18)
где Θ — абсолютная темп-pa, Qe — теплота, выделяемая входящими в реакцию грамм-
dE
атомами двухвалентного элемента, ^ —
температурный коэффиц. По теоретическим вычислениям и опытным измерениям Долезал ека, этот коэфф. меняется с концентрацией; соответственно с этим различно и «поведение» А. (табл. 8).
При низких t° работа свинцовых А. ограничена замерзанием электролита, что зависит от его концентрации (фигура 10); при замерзании электролита эдс резко падает. считать, по Айртону, сопротивление в 0,08 Ω; например, сопротивление элемента из 5 положительных пластин 250 лиг х 400 миллиметров будет^2х5-)°,(|| 5Х^ —0,0 008 Ω. Оно составляется почти целиком из сопротивления электролита. Наилучшая проводимость электролита — при содержании 30 — 35 % кислоты (26—30° В6). Потеря напряжения А. на внутреннее сопротивление — несколько сотых V, что влечет потерю энергии, самое большее, на 2—5%. Сопротивление А. убывает во время зарядки и возрастает при разрядке; последнее явление происходит: 1) от уменьшения концентрации всего электролита, 2) от частичного понижения ее в порах активной массы, 3) от увеличения удельного сопротивления активной массы,
Таблица 8.—«Поведение» А. в зависимости от концентрации кислоты.
| Концентрация кислоты | Коэфф.
dE | Эдс при повышении V | t3 аккумулятора | ||||
| число граммоле-кул на 1 л | ЧИСЛО
г/л |
уд. вес. | градусы
Βέ |
d« | при зарядке | при разрядке | |
| < 0,7 | < 69 | < 1,044 | < 5,8 | Отрицательп. | Понижается | Повышается | Понижается |
| 0,7 | 68,6 | - 1,044 | — 5,8 | Нулевой | Без изменения | Без изменения | Без изменения |
| Очень небольшое, но > 0,7 | Немного > 69 | Немногом ,044 | Немно-
го>5,8 |
Положитель ный | Возрастает в линейной зависимости | Понижается | Повышается j
j |
| 2 | 196 | 1,125 | 15,5 | Максимальн.: + 0,38mV/l Ц. | Возрастает наиболее быстро | Понижается наиболее быстро | Повышается наиболее быстро |
| 2,43 | 239 | 1,15
Обычная концентр. |
18,8 | Положитель ный | Повышается | Понижается | Повышается |
Внутреннее сопротивление. Внутреннее сопротивление свинцового А. весьма мало и представляет малый практический интерес. У больших А. оно равно нескольким десятитысячным ома, у малых— самое большее нескольким сотым. На 1 дм2 неразвитой поверхности анода надо
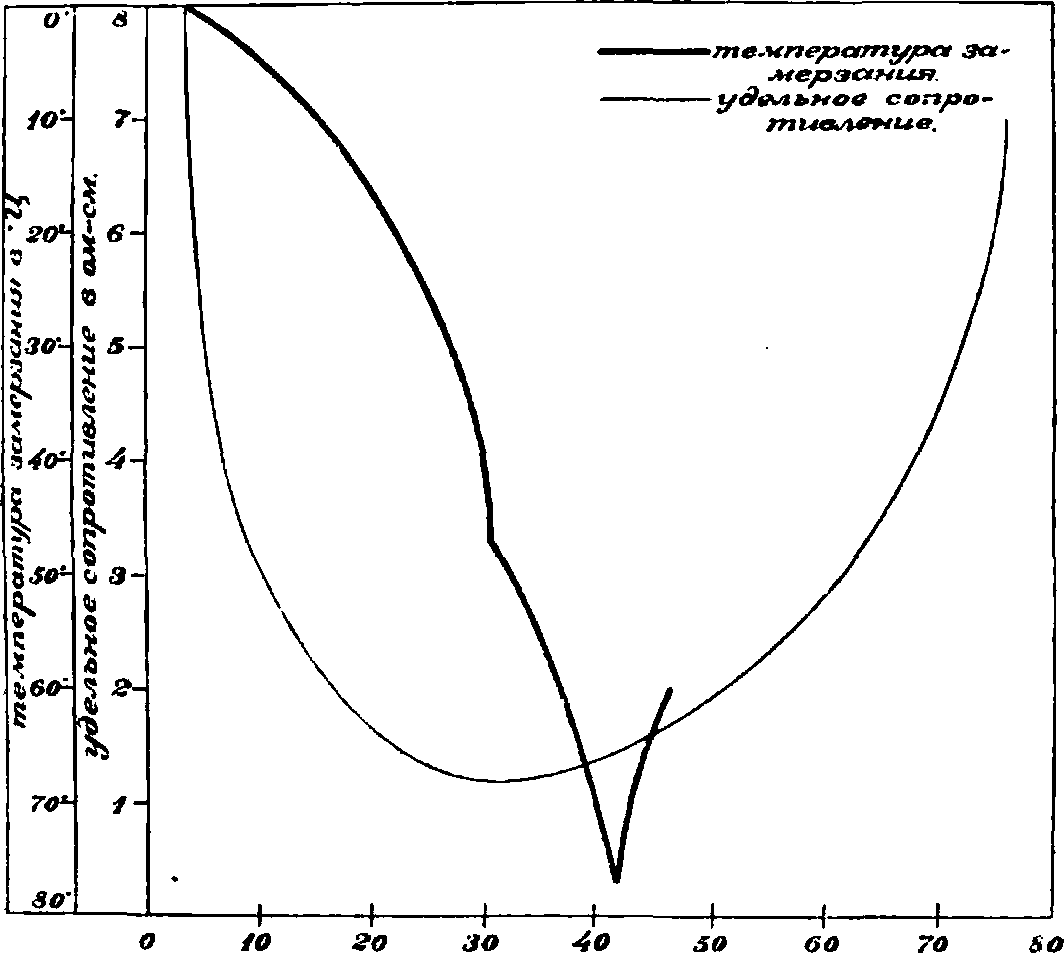
С одержание II,SOj в %
особенно на аноде. Проводимость электролита возрастает с t° (для 20%-ной кислоты, примерно, на 1,5% на 1°).
9. Емкость. Емкость С свинцового А. зависит от его устройства, от формы и размеров электродных поддержек, хим. состава и физ. строения активных веществ. При прочих равных условиях, она зависит от условий его службы: режима разрядки, концентрации электролита и t°.
Зависимость емкости от режима разрядки. С увеличением силы разрядного тока, емкость А. уменьшается. Для слабых разрядных токов (при разрядках, длящихся более 8 ч.) общее отношение, на основании закона диффузии Фика, можно выразить так:
С =
и
β + I ’
(19)
где и и β — постоянные элемента, которые могут быть вычислены по двум разрядкам; формула эта применима к разрядке с изменчивым режимом. Опытная кривая зависимости С от разрядного тока 1 подобна фигура 11. Для разрядок более сильными токами Пей-кертом в 1892 года установлена эмпирическая функция:
Т=Const, (20)
или /,<-1. С=Const. (21)
Фигура 10. Температура замерзания и удельное сопротивление водного раствора серной кислоты в зависимости от содержания кислоты. где I—разрядный ток в амперах, Т—время в часах, п—постоянная, характерная для типа А. и содержащаяся между 1,2 и 1,8. Ф-ла Пейкерта имеет силу только для раз-Ah рядок постоянным током. Эта ф-ла применима к свинцовым А. любого типа с точностью 1 — 2%. Для быстрого вычисления отношения емкостей С2: Сг по заданному соотно
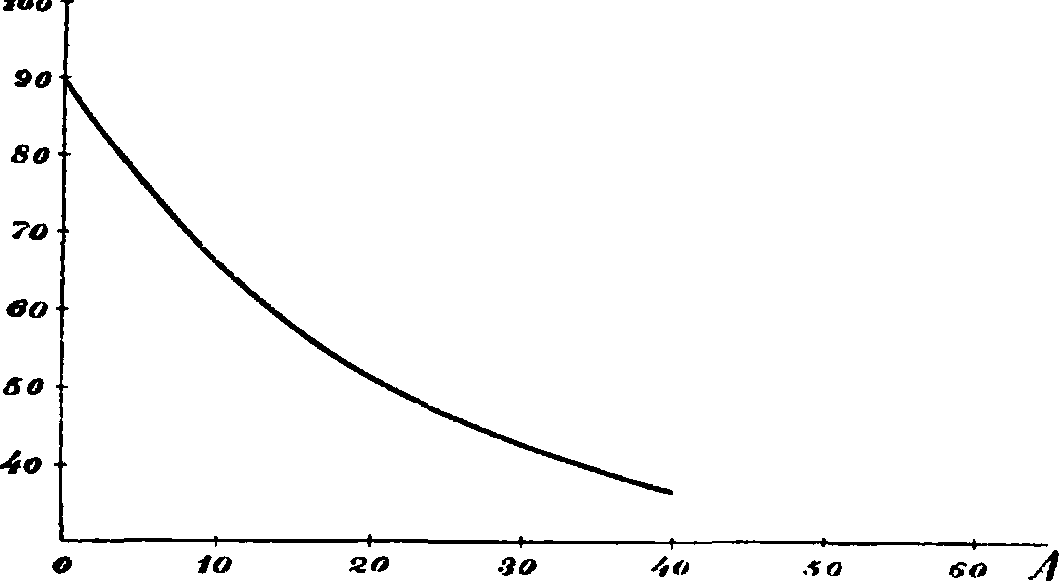
сила разрядного тока
Фигура 11. Емкость аккумулятора в зависимости от силы разрядного тока (примерная кривая).
шению соответствен, времен разрядок Т2и Т] и характеристичному числу п—или, наоборот, для нахождения числа п по отношению емкостей С2 : С3 и отношению соответствен. времен разрядок Т2: Тх служит табл .9.
Таблица 9.—Д анные Ф. Лоппе для применения формулы Пейкерта.
| Отно
шение | Отношение | е м к | о | с т е и С2 | Сг | ||||
| вре- | |||||||||
| мен | з н | а | ч | е в | И | е η | |||
| раз- | |||||||||
| рядок
Т,:ТХ |
1,20 | 1,30 | 1, | 40 | 1,50 | 1 | ,60 | 1,70 | 1, 80 |
| 0,1 | 0,68 | 0,59 | 0, | 52 | 0,46 | 0 | ,42 | 0,39 | 0,36 |
| 0,2 | 0,76 | 0,68 | 0, | 63 | 0,59 | 0 | , 55 | 0,52 | 0,49 |
| 0,3 | 0,81 | 0,76 | 0, | 72 | 0,67 | 0 | , 6 3 | 0,61 | 0,59 |
| 0,4 | 0,86 | 0,82 | 0, | 76 | 0,75 | 0 | ,71 | 0,68 | 0,67 |
| 0,5 | 0,89 | 0,85 | о, | 82 | 0,79 | 0 | ,77 | 0,75 | 0,73 |
| 0,6 | 0,92 | 0,88 | 0, | 86 | 0,84 | 0 | ,83 | 0,81 | 0,8п |
| 0,7 | 0,94 | 0,92 | 0, | 91 | 0,89 | 0 | , 88 | 0,87 | 0,86 |
| 0,8 | 0,96 | 0,95 | 0, | 94 | 0,93 | 0 | ,93 | 0,93 | 0,92 |
| 0,9 | 0,9 8 | 0,98 | 0, | 97 | 0,97 | 0 | ,97 | 0,97 | 0,97 |
| 1,0 | 1,00 | 1,00 | 1, | 00 | 1 ,00 | 1 | ,00 | 1,00 | 1,00 |
| 1,1 | 1,02 | 1,03 | 1, | 03 | 1,03 | 1 | ,03 | 1,04 | 1,04 |
| 1 ,2 | 1,03 | 1 ,04 | 1, | 05 | 1,06 | 1 | ,07 | 1,08 | 1,08 |
| 1,3 | 1,04 | 1,06 | 1, | 07 | 1,09 | 1 | ,10 | 1,11 | 1,12 |
| 1,4 | 1 ,05 | 1,08 | 1, | 10 | 1,12 | 1 | ,14 | 1.15 | 1,16 |
| 1,5 | 1, 07 | 1,10 | 1, | 12 | 1,14 | 1 | ,16 | 1,18 | 1,20 |
| 1,6 | 1,08 | 1,11 | 1, | 14 | 1,16 | 1 | ,19 | 1,22 | 1,23 |
| : 1,7 | 1,09 | 1,13 | 1, | 16 | 1,19 | 1 | ,22 | 1,24 | 1,26 |
| 1,8 | 1,10 | 1,14 | 1, | 18 | 1,22 | 1 | ,25 | 1,27 | 1,30 |
| 1,9 | 1,11 | 1,16 | 1, | 20 | 1, 24 | 1 | ,27 | 1,30 | 1,33 |
| 2, 0 | 1,12 | Ы7 | 1, | 22 | 1 ,26 | 1 | , 30 | 1, 33 | 1,36 |
| 2,5 | 1,16 | 1,24 | 1, | 30 | 1, 36 | 1 | ,41 | 1 ,46 | 1,50 |
Зависимость емкости от концентрации электролита. Емкость А. возрастает с концентрацией кислоты до некоторого максимума и затем убывает. По Долезалеку, максимум емкости совпадает с концентрацией наибольшей проводимости кислоты (30%, уд. в 1,224). Однако, по Жюмо, оптимальная концентрация зависит от режима разрядки и, кроме того, различна для анодов и катодов (табл. 10).
Таблица 10.—Зависимость концентрации от режима разрядки.
| 1
Режим разрядки | Уд. в электролита, соответств. наибольшей емкости | ||
| всего | анода | катода | |
| Медленный. I 1,2 Быстрый.1 1,32 | 1,20
1,38 |
2,12
1,20 | |
Эти данные имеют значение лишь примерное и относятся к определенному типу пластин.
Зависимость емкости А. от t° такова, что можно считать нарастание емкости, сравнительно с таковою же при t° 15°, примерно в 1% на 1°. Однако повышение емкости посредством повышения t° не рекомендуется, т. к. это разрушает электроды (катоды) и усиливает местные действия, а получающиеся потери при очень медленных разрядках приводят к нулю выгоду увеличения емкости нагреванием. Возрастание емкости с t° объясняют увеличением при нагреве проводимости и диффузии электролита. Увеличение емкости от повышения t° трм более значительно, чем быстрее разрядка. Оно зависит также от типа пластин, от предшествующих разрядок, от концентрации кислоты и различно для катодов и для анодов.
10. Отдача А. Отдача электричества свинцового А. при наилучших условиях достигает 0,90 и даже 0,95 (то есть 90—95%); она мало зависит от увеличения силы тока и от концентрации электролита. Потеря в 10—5% обусловлена гл. обр. местными действиями, особенно при длительном отдыхе после зарядки. При расчетах nq принимается равным 0,9. У щелочного А. отдача равна 0,72-^-0,80.
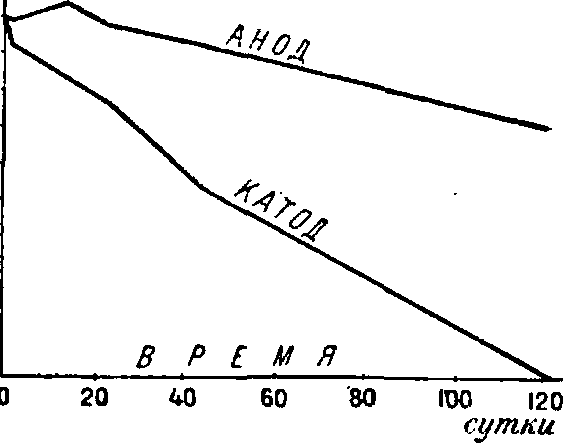
Саморазрядка. А. обычного типа при хорошем содержании теряют не менее 1% своего заряда в сутки; А. же загрязненные «не держат» своего заряда, и потеря их может доходить до 50% и более. Даже наилучшие современные А. за месяцы отдыха дают 40—60% потерь. Страдают от потери преимущественно катоды,—как по- t0называют графи- §оэ ки (фигура 12), че-рез 120 суток в опытах Жюмо ка- ^o.s тод потерял весь ξΰΑ заряд, а анод— только 25%. Но, |oj при возможном, устранении местных действий, в А. Фери достигнута весьма малая потеря заряда, а именно: 5—7% в первый месяц после зарядки и средним числом 3% в последующие. Источником саморазрядки А., обусловливающим местные действия, ранее считали платину; теперь, когда серная кислота готовится без платины,—железо, к-рое служит передатчиком кислорода от анода к катоду. Однако главная причина потери заряда — кислород воздуха, вызывающий самопроизвольную сульфацию катода, согласно двум реакциям:
H2S04+Pb=PbS04+H2 и Н2 + 0=Н20. Этот процесс усиливается от прохождения пластин через слои электролита с разной концентрацией растворенного воздушного кислорода. Поэтому горизонтальное помещение катода на дне бака дало в А. Фери (фигура 13) превосходную меру борьбы с саморазрядкой, и на разработку этого принципа должен быть направлено внимание конструкторов. Напротив, рекомендованное недавно прибавление к электролиту щелочного бисульфата
нс оказывается полезной мерой; кроме того, вследствие некоторой растворимости сернокислого свинца в сернокислых щелочных мет, оно может ускорить разрушение пластин.
Отдача энергии η„ при наилучших условиях колеблется между 0,75 и
0,85 (75—85%); на
+

Фигура 13. Сухой аккумулятор Фери. иболынее значение ее при 30 %-ной кислоте (уд. вес ок. 1,22). При расчетах i7w принимается равным 0,75—0,82; Vw < rlq (с которой связано соотношением 9«=V)’ потому что коэфф. понижения > 1. Так как с повышением t° 4qубывает, а λ возрастает, то ηι0 мало зависит от t°. При той же отдаче электричества η9 отдача энергии Чп возрастает с концентрацией электролита и убывает при возрастании тока, теряет энергию в фор-однако, не джоул ев-
При разрядке А. ме теплоты; это, ская теплота, а теплота происходящего от нескольких причин смешения кислоты разных концентраций. Потеря энергии, вызванная токами концентрации, выражается соотношением:
W=a~lH (22)
в вольт-кулонах, где а — константа, b — конструктивная постоянная пластин, Ат— средняя проводимость кислоты. В первом приближении можно считать b/Ат независящим от I, так что
W= αΡτ. (23)
В силу пропорциональности W квадрату силы тока потерю энергии в первом приближении можно рассматривать условно как джоул евское тепло, но при возросшем внутреннем сопротивлении. У щелочного А. отдача энергии 0,52—0,55.
И. Технические факторы емкости. Использование материала электродов в свинцовых А. опреде ляется следующими данными: не все активное вещество обслуживает зарядку А.; отношение между массой вещества, действительно дававшего емкость, и полной массой активного вещества называется коэфф. использования. Очевидно, при тех же самых опытных данных, коэфф. использования окажется различным в зависимости от принятой эл.-хим. схемы А. Имеющиеся данные приведены и в таблице 11 и 12.
Таблица 11. — Данные для вычисления пра к тич. достижимого коэфф. использования свинцового А.
| Составляющая массы А. | Составляет от полной массы | Наибольшая удельная, отнесенная к кг | |
| электродов о
/о |
емкость
Ah/кз |
энергия
W/кг | |
| Активное вещество электродов. | 60—5 5 | 50 | 100 |
| Поддержка электродов .. | 4 0—4 5 | __ | |
| Электроды в целом. | 100 | 30 | 60 |
| Бак, электролит и принадлежности. | 50 | _ | |
| Аккумулятор в це-. лом.. | 150 | 20 | 40 |
Значение диффузии. Использование активного вещества ограничено недостаточным притоком кислоты внутрь пластин. Заставляя проникать кислоту в катод под давлением, Либенов получил емкость А. в три раза большую, чем без давления. Отсюда вытекает необходимость по возможности увеличивать пористость активной массы, в частности—тонкостью ее кристаллов. Проникновению кислоты способствует также малая толщина пластинок; по приближенной формуле Либенова
С =
а
(24)
1 + βΐΐι ’
где С—емкость А. с электродами из одного и того же количества активного вещества, h — толщина пластин, ос и β — постоянные. Однако недостаточная механическая прочность слишком тонких пластин и быстрая их изнашиваемость эл.-хим. процессом ставит предел увеличению емкости путем дальнейшего утончения.
Долговечность пластин. Положительные пластины большой поверхности сперва работают своей пастой. Емкость их возрастает до некоторой наибольшей
Таблица 12. — Данные для вычисления максимального коэффициента использования свинцового А.
| Объекты сопоставления | Теория недокисного сернокислого свинца Pb2S04 | Теория окисного сернокислого свинца PbSO« | ||
| теория |опытн. данные Фери j Фери | теория Гладстона и Трайба | опытные дапные Жюмо | ||
| Наемк. 1 Ah требуется Стотта’ Ill акт. вещества в з ™а ; ; j, 57; Д
Наиб. уд. емкость в Ah на 1 килограмм акт. ι вещества.. 64 Коэфф. использования.j 0,7 8— |
7,86
11,12 19,20 50- 52 -0,81 |
4,46
3,86 8,32 120,20 |
30—72, в среднем 51. 0.25—0,35 длянаилучш. пастиров. пластин *. | |
| * При исключительно благопр. условиях достигнуто значение 0,60: для пластин большой поверхности, при разрядке в 10 ч., наибольшее значение 0,40. | ||||
величины и затем держится неизменной, пока отпадение пасты возмещается превращением в перекись ребер. Затем, после полного преобразования этого материала, емкость постепенно убывает до полного изнашивания электродов. Пастированные пластины ведут себя различно, в зависимости от их пористости и молекулярного состояния. Отрицательные пластины по емкости превосходят положительные, но вскоре, из-за сжатия свинца, пористость и проводимость пластин уменьшается, и емкость убывает, сперва довольно быстро, затем медленно, причем активное вещество дает трещины. Попытка устранить это явление прибавкой к свинцу инертных материалов не имела полного успеха. В общем, все приемы увеличения уд. емкости сокращают срок службы электрода.
Аноды Аккумуляторного треста выдерживают 108 — 150 зарядов, катоды — несколько больше. При хорошем уходе аноды станционных батарей служат 5—6 лет, а катоды— до 10 лет. Германские аккум. батареи высокого напряжения для радио в лучшем случае могут работать 2 — 3 года.
Сурьмянистый свинец более прочен механически и менее окисляем, чем чистый. Обыкновенно он содержит 6—12% сурьмы. Сплавы РЬ менее чем с 13% Sb имеют Рпл. ниже, чем каждый из компонентов; сплав с 13% Sb остается жидким до 228°. Понижение £°пл. пропорционально содержанию сурьмы и может служить для вычисления этого содержания. Точно так же уменьшение уд. в сплава пропорционально содержанию сурьмы и, начиная от 11,35 для чистого свинца, составляет 0,074— 0,072 на 1% Sb. Изготовление сплавов производится двумя способами: если требуется большое содержание Sb, то сурьму расплавляют в графитовом тигле, дают охладиться до t°ome., прибавляют часть расплавленного свинца и полученный сплав смешивают со свинцом, расплавленным в чугунном тигле; если же содержание Sb должно быть невелико, то в свинец, находящийся в чугунном тигле при 500°, прибавляют куски сурьмы и размешивают их до растворения.
Свинцовые соединения. В аккумуляторном деле применяются соединения РЬ; с данных о них дана в таблице 13.
Таблица 13. — Характеристика свинцовых соединений дляА.
| 1 | Колич. | |||||
| Ф-ла | Молекул. | λ дельный вес | Отнош. | свинца | ||
| Соединения | молекул. | на 1 килограмм | ||||
| В6С | абсол. | кажущ. | масс | вещества в г | ||
| ί
1 Гпхтнри J пульверизованный. 1 свинец ^ губчатый .. |
РЬ | 207 | 11,4 | 5—6
3—4 |
1,00 | 1 000 |
| ί Окись свинца, или глет. | РЬО | 223 | 9—9,5 | 4—4,5 | 1 ,08 | 928 |
| Сурик
Двуокись свинца, называемая (неточ- |
РЬ,04 | 685 | 8,5—9,5 | 4— 4,5 | 1 ,10 | 906 |
| но) перекисью.. | РЬ02 | 239 | 7—9 | 3,5—4, 5 | 1,15 | 866 |
| Свинец сернокислый окисный. | PbS04 | 303 | 6,2 | — | 1 ,46 | 683 |
| Свинец углекислый.. | РЬСО, | 267 | 5—6 | — | 1,29 | 775 |
| Свинец хлористый .. | РЬС1г | 278 | 5,7 | — | 1,34 | 744 |
| Свинец сернокислый недокисный. Перекись свинца, или надсвинцово- | Pb,S04 | 510 | *- | 1,23 | 811 | |
| кислый ангидрид .. | PbaOs | 494 | 1 ,49 | 838 | ||
II. Производство аккумуляторов.
. 12. Сырье для свинцовых А. С в и н е ц —
главный материал производства свинцовых А. В дополнение к описанию его свойств (смотрите Свинец) отметим: линейный коэфф. усадки при затвердевании—ок. 0,01. Органические кислоты (уксусная, винная, щавелевая и др.) растворяют его. Из загрязнений рыночного свинца главные: цинк, сулема, медь, железо, серебро, олово. Переходя в раствор в А. и осаждаясь на катоде, эти соединения вызывают местные действия. Особенно опасны в качестве примесей металлы платиновой группы: 0,0001% их может вызвать саморазрядку А. в течение двух часов. Рафинированный свинец должен содержать 99,95—99,98% чистого свинца. Количественный анализ производится либо химически, либо электролитически. К лучшим маркам свинца относится английский свинец фирмы Куксон и Мак-Ланг.
Сурьма применяется для составления сплавов со свинцом. Рыночный товар содержит 97,5—98,8% чистой сурьмы, а электролитическая—99,98%. Главные примеси: S, As, Pb, Fe и Си. В виду сплавления сурьмы почти со всеми металлами, ее следует плавить исключ. в графитовых тиглях.
Свинцовые соединения могут содержать различные вредные примеси для аккумуляторного дела: железо, марганец, медь, хлор, уксуснокислые соединения и азотистые. К сурику подмешиваются охра и толченый кирпич, а к другим соединениям—мел, сернистый барий и свинец.
Связывающие вещества. К смеси свинцовых соединений прибавляются для образования пасты различные вещества; приводим список главнейших из них.
Главные связывающие средства для пастовых смесей.
Кислоты и их соли.
Серная кислота и сернокислые соли щелочных и щелочноземельных металлов (К, Na, NH3, Са, AI, Mg). Кислоты сернистая и гипосернистая.
» тионовая и тиосульфаты щелочных металлов.
» сульфоновая.
» фосфорная.
» щавелевая и щавелевокислый аммоний.
» уксусная и уксуснокислый свинец.
» феноловая и фенолят свинца.
-> мочевая и сернокислая мочевина.
» пикриновая.
Основания, окиси и минеральные соединения.
Едкое кали и едкий натр.
Нашатырный.
Окиси алюминия и магния.
Квасцы, марганцевокислый калий.
Насыщенная кислородом вода.
Органические соединения. голь.
Глицерин с серной кислотой.
Фенол в водном или гольном растворе. Нафталин.
Антрацен (раствор в уксусной кислоте).
Глюкоза, декстрин, сахароза, крахмал.
Камфора, коллодий, чатая хлопчатая бумага (раствор в бензоле или щелочи).
Альбумин, фибрин, казеин.
Пиридин (гольный раствор).
, сернокислый хинин.
Льняное масло, некоторые смолистые мыла, янтарь, некоторые ископаемые смолы (в гольном растворе).
Каучук.
Асфальты (в гольном растворе).
Битум (раствор в бензоле или в метиловом голе).
Инертные вещества.
Глина, инфузорная земля и фарфор в порошке. €ажа и т. д.
Одни из этих веществ служат физич. склейкой, другие ведут к возникновению различных химич. соединений, третьи дают пористость анодам, четвертые задерживают выкрашивание катодов. Но каково бы ни было вещество, примененное для связи, цементирует активное вещество электродов и дает ему твердость сернокислый свинец, образующийся либо при пастиро-вании электродов, либо при одной из последующих операций.
Вод а—дистиллированная, но б. ч. допустима и профильтрованная речная.
Серная кислота — применяется предпочтительно полученная из серы; обыкновенная кислота тоже допустима, но лишь после пропускания через нее в течение 24 час. сернистого водорода, последующего отстаивания в течение 24 ч. и декантации. Растворение кислоты следует производить приливанием кислоты в воду, а не наоборот, т. к. иначе могут получаться опасные брызги. Баки для смешивания должны быть не-разъедаемыми кислотой и делаться деревянными со свинцовой обкладкой, каменными, свинцовыми и т. д. Кислота производит опасные ожоги кожи; нейтрализуют ее нашатырным ом или содой. Главные загрязнения кислоты: азотистые соединения, сернокислый свинец, хлор, платина, овые соединения, железо, медь, цинк и тому подобное. Наиболее вредна примесь благородных металлов; например, недопустима примесь платины свыше 0,0001%. По стандарту ВСНХ, принятому также НКПиТ, аккумуляторная серная кислота должна удовлетворять условиям: 1) крепость кислоты 20—66° Вё, уд. в 1,83 при 66° Вё; 2) содержание железа и азотистых продуктов должен быть 0,01%; 3), хлор и окись азота должны отсутствовать; 4) кислота должен быть прозрачна и бесцветна.
Стандарты аккумуляторных кислот существуют до настоящего времени только в СССР и утверждены как обязательные общесоюзные стандарты Комитетом по стандартизации при СТО. Эти стандарты предусматривают два вида кислот: аккумуляторная кислота I, крепостью 22° Вё и аккумуляторная кислота II, крепостью 65°,5 Вё. Для этих кислот устанавливаются следующие предельные содержания примесей:
Аккум. кислота I
Железа не более.. 0,006%
Твердого остатка не более 0,05 %
Аккум. кислота II 0,02%
0,1 5%
Кислоты должен быть прозрачны и бесцветны и не должны содержать хлора, окислов азота, а, органических примесей и металлов, осаждаемых сероводородом. Допускаются следы аммиака и металлов, осаждаемых сернистым аммонием. Помимо строгого регламентирования порядка отбора проб, стандарты аккумуляторных кислот дают подробную методику аналитической проверки приведенных условий. Удельный вес определяют ареометром Боме (смотрите Ареометрия). Содержание железа определяют осаждением полуторных окислов, восстановлением окис-ного железа в закисиое и последующим титрованием ΚΜηϋ4. Содержание твердого остатка определяют выпариванием кислоты досуха и прокаливанием остатка до постоянного веса. Остальные примеси определяют исключительно качественным путем. Отсутствие а определяют аппаратом Марша; зеркало должно отсутствовать. Отсутствие хлора проверяют реакцией с AgN03. Отсутствие азотистого ангидрида проверяют реакцией с крепким раствором железного купороса. О т-сутствие органий м е с е и проверяют прибавлением к кислоте 2 — 3 капель КМп04, причем раствор не должен обесцвечиваться. Упаковка аккумуляторных кислот пока не стандартизована, в стандартах же имеется только указание на то, что к-та должна наливаться в стеклянную посуду.
13. Производство свинцовых электродов. О τη и в к а. Электроды поверхностные делаются из чистого свинца—либо отливкой, либо механик. способом,а поддержки иастированных электродов—из сурьмянистого свинца и чаще всего литьем. Многократная переплавка свинца вредит его качеству. Плавление свинца и отливка ведется в специальных печах (фигура 14), при t° металла от 500 до 900°. Т. к. сурьма легко окисляется, то ее убыль возмещается прибавлением новых порций богатого сурьмою сплава. Уменьшение поверхности испарения и покрытие ее древесным углем, дающим восстанавливающую атмосферу, предохраняет свинец от образования окислов, делающих отливки весьма ломкими. Отливка производится иногда под пневматическим давлением. Матрицы для отливки, снабженные
13

Фигура 14. Печь системы «Бельвю» для плавления свинца, (газовая или керосиновая).
Т. Э. m. I.
продухами, употребляются чугунные, стальные или бронзовые; поверхность их покрывается сангвиной или припудривается тальком или ликоподием; после отливки
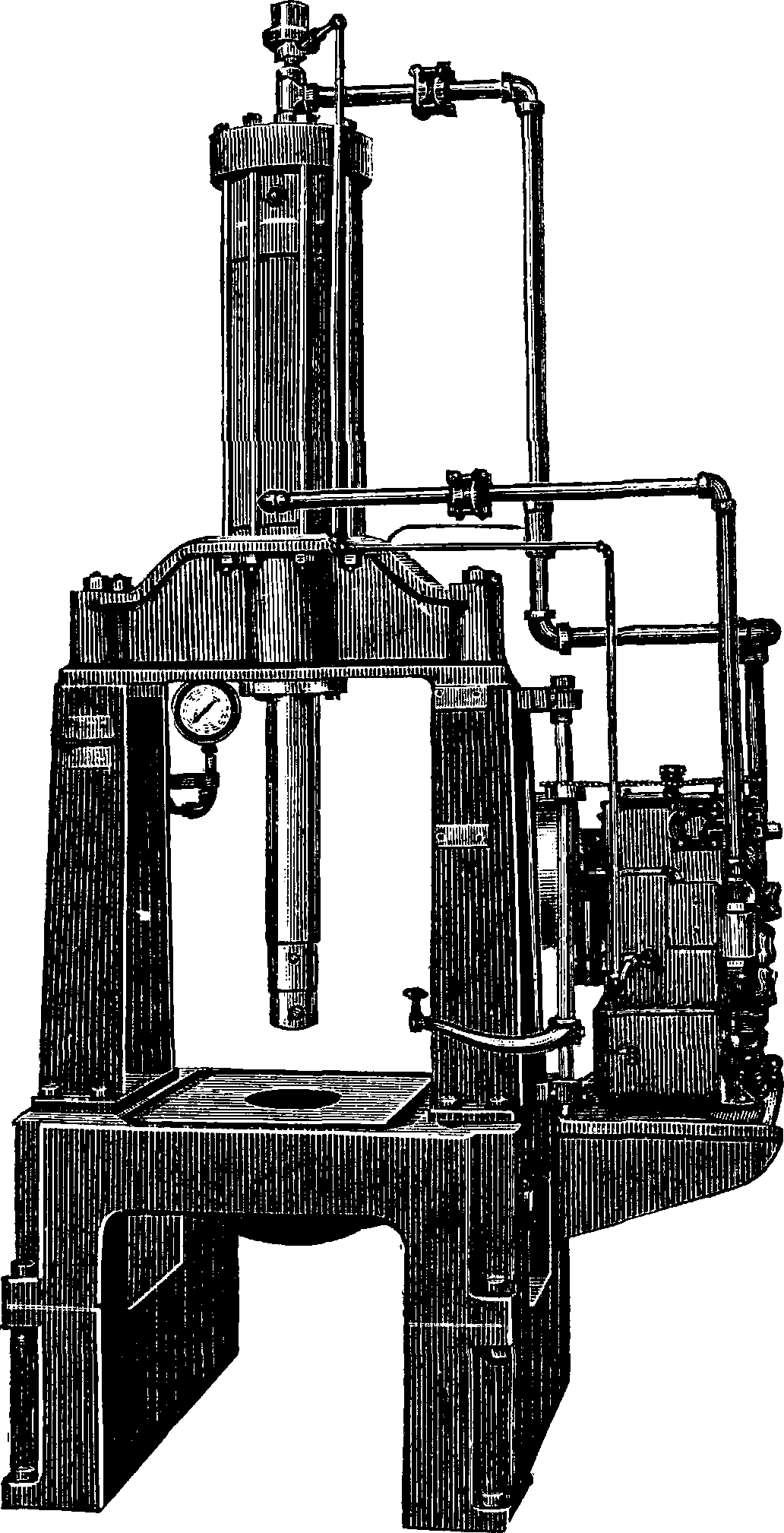
Фигура 15. 50-тонный гидравлический пресс системы Ойлгир, с помпой постоянного давления для композиционных отливок. пластины отделываются. Вальцованный свинец менее разъедается и более равномерно окисляется, нежели литой. Поэтому предпочитают мехаиич. производство электродов;
при этом свинец обрабатывается либо при t°, близкой к плавлению, и отжимается гидравлическим прессом (фигура 15), либо в холодном состоянии.
Пастировка. Существуют различные рецепты смеси для активной массы (табл. 14). В интересах емкости выгодно исходить от возможно более окисленных соединений и получать возможно более сернокислого свинца. Увеличение глета в анодах увеличивает твердость пасты, но уменьшает пористость. Применяются также пасты на свинцовой пыли и с сернокислым аммонием. Для рамочных пластин пасту замешивают на слабом растворе одного из органических связывающих веществ, как-то: водный или гольный раствор фенола, ацетоновый раствор антрацена, гольный раствор (или пары) пиридина, некоторые смолистые масла, асфальт или битум в гольном или бензиновом растворе,—после чего пластины просушиваются в течение 6 часов при 110°. Пастовая смесь размешивается возможно тщательнее, в машинах (фигура 16).
Фигура 16. Автоматическая мешалка для окиси свинца системы Дай. облицованных сурьмянистым свинцом для предохранения от разъедания составными веществами смеси. Столы для смеси покрываются свинцом, стеклом, шифером, асбестом, парафинированным деревом и прочие Па-стирование электродов делается б. ч. вручную, причем катоды пастируются под сильным давлением, а аноды под легким. Сушка пластин ведется либо на воздухе, либо в печах, при 25 —100°; при 100° она продолжается 3 суток. По Г. Вагнеру, пластины болын. поверхности прессуются из древесных
Таблица 14.—Р е ц е п т ы смеси для активной массы свинцовых А.
Аноды ! Катоды
1 i Чистый сурик, серная кислота 15" Вё. Чистый глет, серная кислота 15° Вё.
2 1ч. глета и 3 ч. сурика, серная кислота 15° Вё.. 1 ч. сурика и 3 ч. глета, серная кислота
! ! 10° Вё.
3 Чистый сурик или смеси сурика с глетом в разных пропорциях, раствор сернокислого аммония
15—18" Вё.
4 ; Сурик, раствор сернокислого магния, уд. в 1,18.
5 ! Сурик, 5% кристаллич. сернокислого магния, раствор
! сернокислого магния., —
6 1 80 ч. сурика, 10 ч. глета, 10 ч. кристаллич. сернокпс-, 10 ч. сурика, 80 ч. глета, 10 ч. еерно-
лого магния, серная кислота 15" Вё. I кислого магния, сернаякислота 10Вё.
7 i Смесь сурика и глета в различных пропорциях, раствор сульфоглицерина (1 объём глицерина на
1 5 объёмов серной кислоты 15" Вё).
8 i Сурик замешивается с раствором едкого кали, уд. в 1,10—1,15 (литаподы Фитц-Дшеральда).
После сушки и вымочки в воде погружается в ванну с сернокислым магнием. опилок, пропитанных раствором сернокислого аммиака уд. в 1,142 и закатанных затем в последовательные слои сурика (или глета, смотря по знаку пластины), угля и прокаленного гипса; просушенные при 120° пластины погружаются в серную кислоту уд. в 1,2—до разрушения ядер из древесины. В. де-Пльюс сушит пластины обычного состава перегретым паром при 260° и давлении 9—13,5 килограмм/см2. О’Кинан примешивает к активному веществу около 10% инертного пломбажина, порошка из ретортного или древесного угля, опилок никелевых, вольфрамовых, железо-никелевых и т. д. Шимадзу делает пасту из 300 ч. перекиси свинца, 0,45 ч. воды или серной кислоты; паста дает гидрат и тем компенсирует усушку. Перекись свинца он получает измельчением свинца в барабане. Наиболее интересны пластины Каваками. Рамы их делаются из свинцовой амальгамы (1% ртути), и в них наливается сплав по одному из следующих рецептов:
| № сплава | РЬ
% |
Mg
% |
Са
% |
К
% |
1
Состав евтектики |
! t° при центри-1 фугировании 1 электродов |
| I | 99,2 | 0,8 | _ | _ | 97% РЬ + 2,9% Mg | 280 |
| II | 99,1 | 0,8 | 0,1 | — | 97% РЬ + 2,9% Hg + + 10,1% Са | 280 |
| III | 99,4 | - | 0,6 | 92,2% РЬ + 1,82% К | 300 |
После центрифугирования таких пластин при t°rui. евтектики в течение 20 — 30 метров остается один чистый свинец пористого строения.
14. Формовка электродов. Этим термином обозначается совокупность операций, преобразующих поверхностный слой чистого свинца у электродов большой поверхности или смесь свинцовых соединений, составляющих пасту наведенных пластин, в перекись свинца на аноде и в губчатый свинец на катоде. Формовка всегда слагается из двух процессов:
1) хим. преобразование, ведущее к образованию на обоих электродах некоторого количества сернокислого свинца; 2) эл.-хим. преобразование — окисление веществ на аноде и восстановление их на катоде. Для наведенных пластин эти про цессы последовательны, для пластин большой поверхности они сперва последовательны, а затем совместны, т. к. по мере превращения уже имевшегося сернокислого свинца образуется новый. Формовка положительных и отрицательных пластин может вестись как вместе, так и порознь. Совместная формовка, применяемая большинством мастерских, дает экономию времени, места, труда, материала и тока. Неудобства: окончание процесса формовки анодов раньше, чем катодов, вследствие чего приходится делать замену первых; электролитически— перенос на катоды загрязнений с анодов. Предпочтительно поэтому вести формовку анодов и катодов врозь, применяя в качестве парных электродов свинцовые пластины в 3—4 миллиметров толщиной или непастиро-ванные решетки. Формовка бывает черной и белой. Первая доводит электроды до окисленного состояния, и потому при установке их на станциях не требуется специальных реостатов, но зато электроды хуже выдерживают перевозку. Вторая дает губчатый свинец; такая формовка механически прочнее, но при установке А. необходимы специальные реостаты.
Формовка пластин большой поверхности идет медленно и требует большого расхода тока. Ради облегчения этого процесса придумано много различных приемов, ведущих к образованию рыхлой поверхности (табл. 15).
Формовка пластин с наведенными оки состоит в зарядке их, причем электролитом служит либо серная кислота 3—10° Вё, либо сернокислые соли щелочных или щелочноземельных металлов. Если в пасте содержатся хлористые и другие соли, то электроды сперва подвергаются восстановлению посредством образования пар с цинковыми катодами в растворе хлористого цинка, затем уже, после промывки, электроды заряжаются током плотностью 0,02 А/дм2, увеличиваемой постепенно до 0,04 А/дм2, а затем снова уменьшаемой до начальной
Т а б л. 15.—П риемы формовки пластин большой поверхности.
1) Формовка обращениями.
2) Формовка электро - химия, (обычно только одна разрядка, с замедлением образования двуокиси сввица).
3) Формовка инородная или осаждением.
Прием Планте в собственном смысле состоит в многократных зарядках - разрядках с изменением знака электродов. Сначала зарядки - разрядки быстро следуют друг за другом, затем электродам дается все более длительный отдых между зарядкой и разрядкой. а) Прибавка посторонних веществ, анионы которых отделяются при разности потенциалов меньшей, чем это требуется для отделения ионов РЬ02.
б) Предварительное разъедание свинца хим. путем. в) Без прибавления посторонних веществ.
Осаждение перекиси и губчатого свинца электролизом свинцовой соли.
Продолжительность от нескольких недель до нескольких месяцев. Требует большого расхода тока. Концентрация серной кислоты 1—10%. Рекомендуется повышение Г ванны. Предлагались и иные растворы, но они дают не лучшие, или даже худшие, результаты.
Азотная кислота, азотпокислые, хлористые, двухромовокислые и прочие соли щелочных металлов; кислоты муравьиная, уксусная, щавелевая и т. д. Глюкоза, голь, альдегиды и т. д.
Разбавленная азотная кислота, азотнокислый свинец и т. д.
Слабое напряжение с подогреванием.
Сернокислый свинец в растворе виннокислого аммония. величины, чтобы избежать газообразования, разрушающего пористую массу. Длительность зарядки — 60 ч. для анодов и 100 ч. для катодов, а при массовых пластинах —
4—6 дней при постоянном токе и в кислоте 10° Вё. Зная состав пластины, можно с помощью таблицы 16 подсчитать количество электричества, потребного на формовку.
Таблица 16,— Количество электричества, потребное на преобразование свинцовых соединении.
| Исходное соединение | Конечное соединение | Масса исходи, соединения, преобраз, посредством 1 Ah, в г | Число Ah, идущих на преобраз.
1 килограмм исходи.соединения в конечное |
| РЬО | Pb, PbSO* | 3,86 | 259 |
| РЬ | РЬО. | 1 ,93 | 518 |
| РЬО | РЬ, РЬО, PbSO* | 4,14 | 241 |
| РЬОг | Pb, Pbscn | 4,46 | 225 |
| РЬОг | РЬ | 2,23 | 45 0 |
| PbS04 | РЬ, РЬОа | 5,63 | 177 |
При практическом подсчете все указанные в таблице 16 числа должен быть помножены на коэфф. 1,2—1,5, в зависимости от строения электродов и условий формовки.
15. Сборка свинцовых А. Аккумуляторные баки делаются: из дерева со свинцовой обкладкой в 1—3 миллиметров толщиной, из литого и прессованного стекла, целлулоида (фигура 17),
эбонита и из гуммита. Свинцовые баки тяжелы и при тряске иногда пробиваются стеклянными частями; стеклянные имеют преимущество прозрачности,но хрупки и фабрикуются не более как на 100 л, что соответствует 400 килограмм электродов; целлулоидные имеют преимущество прозрачности и легкости, но огнеопасны; эбонитовые легки, но непрозрачны, дороги и нередко дают течь. Цена эбонита понижается в три раза прибавлением органических веществ (гудроны, смолы, вар, жирные масла, фактисы) и наполнителей (асбест, тальк, известь, каолин, углекислый кальций или магний, сернокислый барий, кремнезем, кремнекислый алюминий, окись железа, окись цинка, окись свинца и углекислый свинец, эбонитовые опилки и т. д.). Иногда делается чрезвычайно вредная примесь соединений железа. Эбонит для баков уд. в 1,4—1,6 может содержать примерно: 30—50% каучука и фактисов, 15—20% сульфированных соединений и свободной серы, 25—15% минеральных и 5—10% смолистых ве

Фигура 17. А. почтовый неподвижный в стеклянном баке фирмы Гейнца. Аноды автогенные большой поверхности с поверхностным развитием 1 0, катоды — пастированные с двойной цельной решеткой. ществ. Эбонитовые баки испытываются либо наполнением концентрированной серной кислотой, иногда нагретой до 50°, и оставлением в баках насутки, иногда холодной, либо, высоким напряжением (румкорф, дающий искру до 30 см).
Соединения между электродами делаются либо автогенной пайкой на водородной или ацетиленовой паяльной лампе, либо сваркой электрической. Этот процесс требует опытности и тщательности; для облегчения пайки применяется иногда припой Поллака (15 ч. свинца, 4 ч. ртути и 1 ч. сурьмы), при котором достаточно газовой горелки или бензиновой паяльной лампы. Токоотводящие провода делаются медные, с гальванопластическим свинцовым покрытием для защиты от разъедания.
Электродные прокладки («сепараторы») делаются из перфорированных листов эбонита или целлулоида, а также тех или других с деревянной фанерой; они имеют назначением предупреждать короткие замыкания при короблении электродов и выкрашивании активной массы. Применяемая тут фанера предварительно освобождается от инкрустирующих веществ, т. к. в противном случае эти последние могут способствовать растворению активной массы. Бюро стандартов в Вашингтоне изучило действие двух видов обработки—перегретым паром (а) и щелочью (б)—на древесину разных видов дерева и нашло, что механическая прочность сепараторов идет в убывающем порядке по ряду: кедр б, кедр а, кипарис б, кипарис а, липа б, липа а, тогда как электрическое сопротивление идет по убывающему ряду: кипарис а, кедр а, кипарис б, липа а, кедр б, липа б, причем и та и другая величина пропорциональна толщине слоя.
Электролит в некоторых, сравнительно редких, случаях «сухих» А. приводится к неподвижности либо при помощи пористых неактивных тел, например пористого гранулированного фарфора (Фери), либо прессованных древесных опилок, помещенных как сепаратор (Фульмен), либо при помощи геля кремнекислоты, осаждаемого из жидкого стекла. По Шоопу, к 1 000 ч. серной к-ты, уд. в 1,25, подмешивается 20 ч. протертого волокнистого асбестового картона и в эту смесь быстро вливается и перемешивается 350 ч. продажного жидкого стекла, не содержащего хлора и других примесей. Заранее формованные пластины заливают этой смесью, когда она получит консистенцию масла, а через 24 ч. приступают к зарядке, налив слой разбавленной кислоты. Всеобщая комп, электричества применяет для той же цели тесто из глины с инертными веществами, в роде аморфного угля, кизельгура и т. д.
16. Производство, щелочных А. Промышленностью усвоены щелочные А. трех типов: американские—«Эдисон», шведские по патентам Юнгнера — «Nife» и французские, близкие к американским более раннего типа — «S. A. F. Т.» (Societ6 des accu-mulateurs fixes et de traction) (фигура 18). Промышленная история щелочных А. едва насчитывает 36 лет; за этот срок придуманы разные мелкие конструктивные и производственные усовершенствования, однако главные начала конструкций всех типов остаются сходными между собой, а подробности производства составляют секрет фирм. Чтобы дать представление о сложности этого производства, здесь излагается один из процессов получения активной массы по Э д и с о н у. Для анод ов раствор азотнокислого никеля обрабатывается при нагреве гидратом окиси магния. Осадивши йс я гидрат окиси никеля Ni(OH)2после промывки и просушки током сухого хлора превращается в гидрат перекиси Nia(OH)e. После промывки из этого последнего делается в смеси с чешуйками графита, водой н поташом тесто, раска-тываемое в тонки е листы, которые раздробляются и вновь раскатываются, пока каждая чешуйка графита не будет обволокнута перекисью. Тогда масса прессуется. Для катодов окись железа Ге203 восстанавливается током сухого водорода при 480°, причем ток этот продолжается после охлаждения еще 15 ч. Затем порошок смешивается с окисью ртути и аммиачным раствором окиси меди н прессуется.
Затруднения при конструировании железо-никелевых щелочных А. проистекают от малой проводимости активной массы и от легкости поглощения углекислоты из воздуха щелочным электролитом (20%-ный раствор едкого кали с некоторым содержанием едкого лития); кроме того, активная масса легко выкрашивается. Отсюда вытекает необходимость устройства электродов из массы, пронизанной никелевой основой и окруженной стальными никелированными пластинами с отверстиями. Одно из новых усовершенствований—составление этой основы последовательно скручиваемыми в пучки тонкими проволоками. Баки делаются тоже стальными, никелированными н должны закрываться герметически. Прилагаемыми изображениями поясняется в общих чертах устройство железо-никелевых А. Они характеризуются значительным внутренним сопротивлением, и потому увеличение силы разрядного тока весьма понижает среднее напряжение разрядки. Емкость же, напротив, доало зависит от разрядного режима, так что энергия убывает в зависимости от мощности менее быстро. Т. о. железо-никелевый А. имеет перед свинцовым преимущество только при больших

нагрузках. Кроме того, он допускает весьма сильные токи и не повреждается, будучи оставленным без заряда. Отдача электричества им—60—80%, а энергии — 45—55%. Железо-никелевый А. превосходит свинцовый по энергии, отнесенной к массе, при 3-часовой разрядке и равен свинцовому при
5-часовой. Но по энергии, отнесенной к объёму, он ниже свинцового А. па 5% при 3-часовой разрядке и на 20% при 5-часовой. Емкость его зависит также от режима зарядки. В итоге железо-никелевый А. приблизительно равноценен со свинцовым, т. к. имеет свои преимущества и свои недостатки, а более высокая стоимость его компенсируется большим сроком службы (фигура 19).
17. Экономические данные производства аккумуляторов. Аккумуляторное производство в СССР сосредоточено в руках Элементно-аккумуляторного треста, имеющего два завода: «Ленинская искра» (б. Тюдор, основан в 1892 г.) и «Имени лейтенанта Шмидта» (б. ТЭМ; з-д основан в 1915 году). В довоенное время потребление свинца в России на А. составляло 1 200 ж, а в настоящее— СССР перерабатывает 600 ж, Германия 15—20 тыс. ж, то есть в 25—30 раз больше, чем СССР, а С.-А. С. Ш. от 35 до 40 тыс. ж, то есть в 60—70 раз больше. Весь аккумуляторный свинец ввозится к нам из-за границы. До войны 75% из-делий заграиичн. рынка приходилось
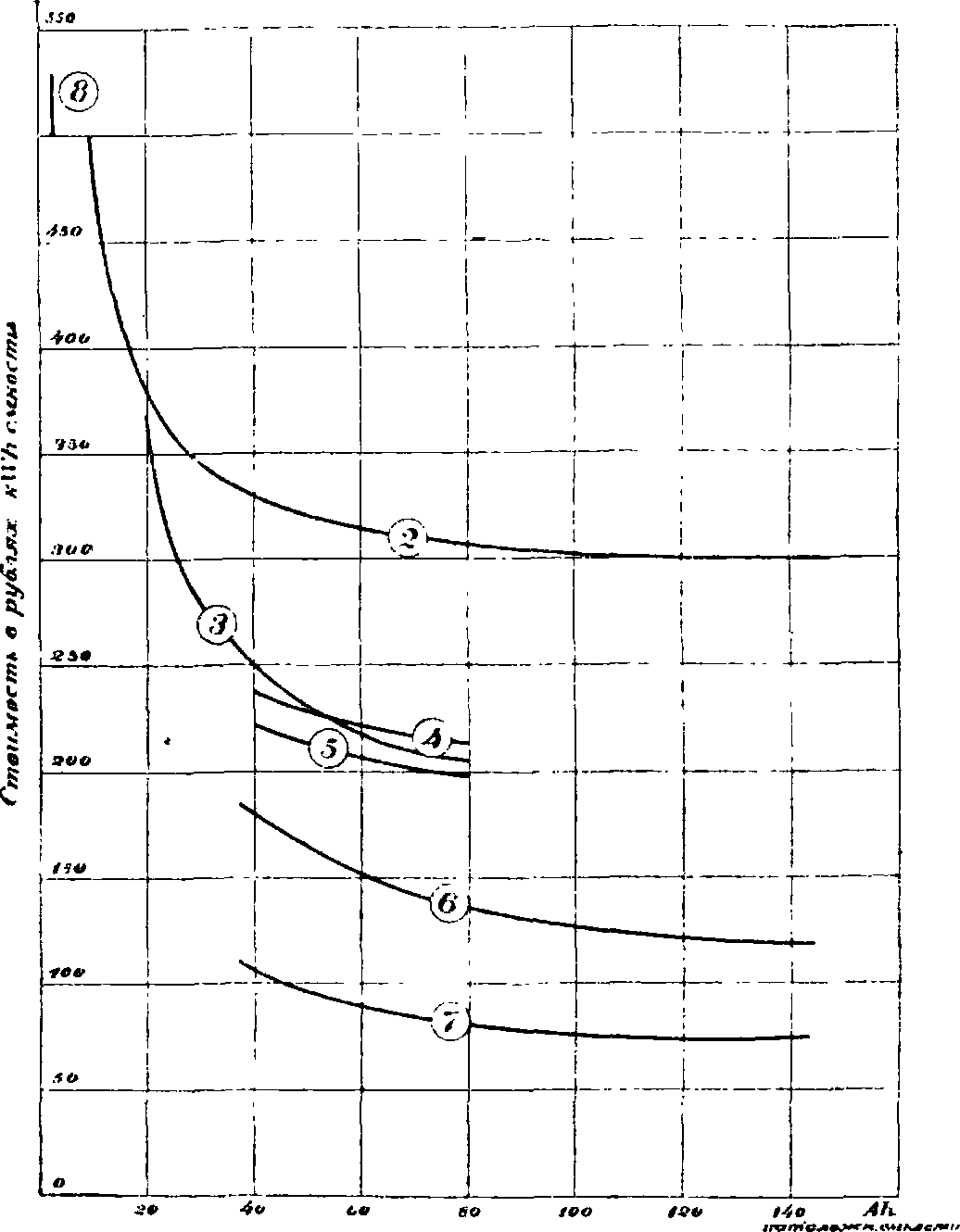
Фигура 19. Стоимость kWh емкости щелочных и кислотных аккумуляторов разных типов. Щелочные А.: 1—радиобатарея, 2—емкостный. Свинцовые А. разных типов производства Аккумуляторного треста СССР: 3. 4 и 5—типа Ц.В., ч—Г.О.,
к., 8—Р.г. на А. с поверхностными пластинами, тогда как в настоящее время приблизительно такое же распространение получили А. с электродами пастированными, так что главное применение А. перешло за границей от станционных батарей к переносным. У нас, как показывает следующая таблица, происходит процесс обратный.
Сравнительное потребление типов А. в процентном отношении.
| Тип А. Год ^ | Поверх ностные | Пасти-
рованные |
Щелочные
Юнгнера |
Итого |
| 1923/24 годах | 21,5 | 78,5 | 100 | |
| 1924/25 » | 30,0 | 5 8,0 | 12,0 | 100 |
| 1925/26 * | 36,5 | 57,0
. |
6,5 | 100 |
Фигура 1, Б дает диаграмму примерного распределения выпуска источников тока (А. и гальванических элементов) по назначению. Главная стоимость А. падает на материалы и энергию, тогда как рабочая сила, производительная и непроизводительная, составляет лишь около 0,1 себестоимости продукции: материалы 60%, заработная плата 10%, накладные расходы, включая заработную оплату вспомогательных рабочих и технического персонала, 35%. Для заграничной калькуляции нужно учитывать меньшую стоимость материалов (около 20%) и энергии, а также меньшую величину заработной платы и накладных расходов. Т. о. соотношение отдельных статей остается при грубом подсчете приблизительно таким же. Из этой калькуляции видно, что механизация производства едва ли может значительно удешевить продукцию А.
18. Санитарные условия. Производство А. требует особых мер безопасности и нуждается в особом внимании инспекции труда. Главные материалы свинцовых А., свинец и его соединения, вызывают, при поступлении в организм как в газообразном, так и в пылеобразном или растворенном состоянии, ряд заболеваний, хронических и острых, известных под общим названием сатурнизма, или свинцового отравления (смотрите). Пары свинца выделяются при отливке пластин, при горячей прокатке и прессовке их и при пайке электродов. Пыль свинцовая и свинцовых соединений может распространяться от форм для отливки и при изготовлении и намазывании пасты; в растворенном виде свинец может поглощаться при пастировке вручную, при трогании пластин и прочие Хроническое отравление свинцом («свинцовая болезнь») выражается в общем расстройстве питания, трясении рук, свинцовых коликах, свинцовых параличах, свинцовой эпилепсии и вообще в свинцовой кахексии (анемии); острое — в ярко выраженных желудочно-кишечных заболеваниях и в параличах. Отмечено, что у пьющих ные напитки свинцовое отравление чаще и тяжелее, чем у непьющих. Санитарные и гигиенические меры: хорошая вентиляция, просторное, светлое и сухое помещение,—в частности, особый отвод свинцовых паров в литейном цехе, — обилие умывальников в рабочих помещениях, соблюдение строжайшей чистоты в помещениях, ванны и души для рабочих, запрещение еды в рабочих помещениях, мытье рабочих перед уходом и перед перерывом, особая одежда, хранящаяся при заводе, по лоскание рта перед едой, сравнительно короткий рабочий день (особенно в более опасных помещениях), регулярный медико-санитарный надзор и осмотр рабочих, борьба со ными напитками. В качестве профилактики указывается употребление слизистых и жирных обволакивающих кушаний и напитков, особенно молока, частое мытье и перемена белья, теплая одежда; противоядие — сернокислые натрий и магний. Кроме свинцового отравления, аккумуляторное производство имеет еще ряд опасных сторон, вынуждающих к принятью предупредительных мер. Прежде всего опасность представляет серная кислота, дающая испарения, брызги и выделяющиеся при формовке газы; затем пары различных веществ (смотря по способу производства), аммиак, ожоги в литейном цехе, связанные с быстротой и непрерывностью процесса отливки; наконец, возможность возникновения пожара в эл.-хим. помещениях. Эти обстоятельства подтверждают необхот димость вышеуказанных мер и требуют ряда новых — особого запрета курить и пользоваться огнем в формовочных помещениях, наличия тут же, в литейном цехе, средств от ожогов кислотой (тряпки, сода) и от горячих ожогов (перманганат). Кроме всего прочего, производство А. нуждается, с точки зрения санитарно-гигиенической, в возможно последовательно проведенной механизации, хотя бы даже таковая и не была экономически бесспорно выгодной. Женщины и несовершеннолетние к производству А. не допускаются. П. Флоренский.
III. Применение аккумуляторов.
19. По своему назначению А. подразделяются на: 1) неподвижные (стационарные), 2) п е р е д в и ж н ы е (для нужд транспорта) иЗ) переносные. От первых требуется гл. обр. долговечность, без особых ограничений объёма и веса, от вторых — компактность и легкость, от третьих — выносливость при плохом уходе. У свинцовых А. каждый из типов имеет различную уд. емкость: наибольшая — у передвижных (до 20 Ай на кг полного веса), наименьшая — у больших стационарных (3 Ай на кг веса). Щелочные А. имеют для всех применений почти одинаковую уд. емкость, порядка 15—20 Ай. Совокупность нескольких А., соединенных между собой для работы на общую сеть, называется аккум. батареей.
1) Стационарные А. применяются или в качестве источника энергии (емкостные батареи), или как регуляторы колеблющейся нагрузки станции (буферные батареи).
Емкостные батареи применяются на небольших электростанциях постоянного тока для работы ночью при бездействии генераторов и для выравнивания графика работы последних. В сетях постоянного и переменного тока батареи А. устанавливаются как резерв на случай аварии в театрах, кино и т. д. На электростанциях переменного тока устанавливаются батареи А. для питания автоматических выключателей, приборов и аппаратов и как источник для освещения на случай аварии. На Шатурской ГЭС для этой цели имеется батарея из 120 А., емк. в 1 740 Ah при 10-часовом разряде. Для поддержания постоянного напряжения у батареи во время заряда и разряда число аккум. батарей, включенных в сеть, может изменяться вручную или автоматически при помощи элементного коммутатора (целленшальтера), посредством которого во время разряда число А.
постепенно увеличивается от величины
До
Е
1,83
2,1
во время заряда концевые А.,
присоединенные к элементному коммутатору, постепенно выключаются. К простому элементному коммутатору присоединяются 14%-ные А., причем во время зарядки батарея не может работать на осветительную сеть; если же требуется поддержание постоянного напряжения и во время заряда, то устанавливается двойной элементный коммутатор (иногда применяется автоматическое регулирование напряжения цел-леншальтером) и число добавочных А. батареи увеличивается до 33,5%. Емкостные батареи применяются часто на ветросиловых станциях, где, работая при отсутствии ветра, они заряжаются, когда ветряной двигатель дает мощность, превышающую потребность. На больших телефонных станциях емкостные батареи являются рабочим источником энергии, обеспечивающим отсутствие колебаний напряжения. В СССР применяются А. исключительно стационарные Тюдор, типа «И». Стационарные А. производятся для емк. до 18 000 Ah при 3-часовом разряде.
Телеграфные А. можно отнести к группе стационарных (по характеру работы) и к группе переносных (по размерам). Наиболее распространенными у нас типами телеграфных А. являются: свинцовые (типа «ПО»), емк. 12,5 Ah при разрядном токе 0,9 А (максим, зарядный ток 2,5 А) и емк.36 Ah при разрядном токе 3,5 А(максим. зарядный ток 9 А); щелочные, системы Юнгнера, емк. 22 Ah при разрядном токе 2,75 А (максим, зарядный ток 9,4 А) и емк. в 45 А при разрядном токе 5,6 А (максим, зарядный ток 20 А). Кроме вышеперечисленных типов, применяются свинцовые в 73,109 и 363 Ah при 10-часовом разряде и юнг-неровские в 20, 23 и 100 Ah. Телеграфные батареи рассчитывают, исходя из силы тока и сопротивления цепи. Щелочные А. в качестве емкостных стационарных А. применять невыгодно.
Буферная батарея А. применяется гл. обр. на трамвайных станциях при небольшом количестве одновременно курсирующих вагонов. Эдс буферной батареи должен быть равна напряжению между точками ее присоединения к сети, при полной нагрузке генераторов станции. При дальнейшем увеличении нагрузки в сети батарея автоматически берет на себя часть нагрузки, а при уменьшении последней в сети излишек энергии, вырабатываемой генераторами, заряжает батарею. Применяются различные схемы соединения буфер- *
* Е — напряжение, которое должно поддерживаться в сети. ной батареи с сетью при посредстве вольтодобавочных машин (смотрите) для усиления буферного действия. Правильно рассчитанные буферные батареи в течение суток в среднем почти не разряжаются, но, тем не менее, требуют ежедневного подзаряда для покрытия потерь на саморазряд. Щелочные А., вследствие относительно большего внутреннего сопротивления, менее приспособлены для буферной работы, чем свинцовые. Буферные батареи (свинцовые) при правильном уходе служат 10 и более лет без смены пластин. В СССР применяется в качестве буферных А. почти исключительно тип «ИС»Тюдор.
2) П е р е д в и ж н ы е А. применяются гл. образом: на подводных судах, на электровозах разного рода и а к-кумуляторных тележках; сюда же надо отнести батареи, служащие для освещения ж.-д. вагонов, автомобилей, и стар-торные А. — для пуска в ход бензиновых двигателей. Все подводные суда, почти без исключения, пользуются для движения в погруженном состоянии электродвигателем, к-рый получает в это время энергию от мощной батареи А. Во время хода над водой или во время стоянки надводный двигатель вращает динамомашину, которая заряжает батарей А. При конструкции А. для подводных лодок стремятся достигнуть большой удельной емкости при минимальном объёме и весе. У свинцовых А. делают легкие эбонитовые сосуды; расстояние между пластинами, несмотря на их большой размер, делают возможно меньшим. Во избежание выплескивания электролита во время качки, эти А. закрываются герметически эбонитовыми крышками с эбонитовыми пробками. Удаление газов, скопляющихся в аккумуляторном помещении подводной лодки, гл. обр. при зарядке А., производится специальным вентилятором. Щелочные А., как более прочные, конкурируют на подводных лодках со свинцовыми. Здесь их большая стоимость не может играть решающей роли, а их большая прочность очень ценна. Если же они не вытесняют в этой области свинцовых А., то это происходит гл. обр. потому, что при том же объёме они все же имеют меньшую емкость при медленных разрядках, даже если при быстрых разрядках емкость их больше. Между тем, на практике, на подводной лодке, в громадном большинстве случаев, приходится разряжать батарей медленно.
Аккумуляторные электровозы получили некоторое распространение на заграничных ж. д., взамен маневренных паровозов, имея перед ними то преимущество, что они моментально готовы к пуску, не расходуя энергии во время бездействия. Эти А. с успехом применяются на автомобилях, которые иногда называются электромобилями или а к к у м о б и-л я м и. Их преимущество перед бензиновыми — более спокойный ход при отсутствии неприятного запаха; недостаток — сравнительно малая скорость и ограниченный район действия. В крупных городах С.-А. Соед. Штатов электромобили являются значительным и выгодным ночным абонентом электрических станций, т. к. потребляют энергию для зарядки в момент минимума нагрузки станций. Особенно распространены там аккумуляторные грузовые автомобили для перевозки грузов на короткое расстояние, вынужденные поэтому часто останавливаться. В этих случаях аккумуляторный автомобиль работает выгоднее, чем бензиновый. Аккумуляторные тележки (фигура 20) распространены на Западе для перевозки на территории заво-
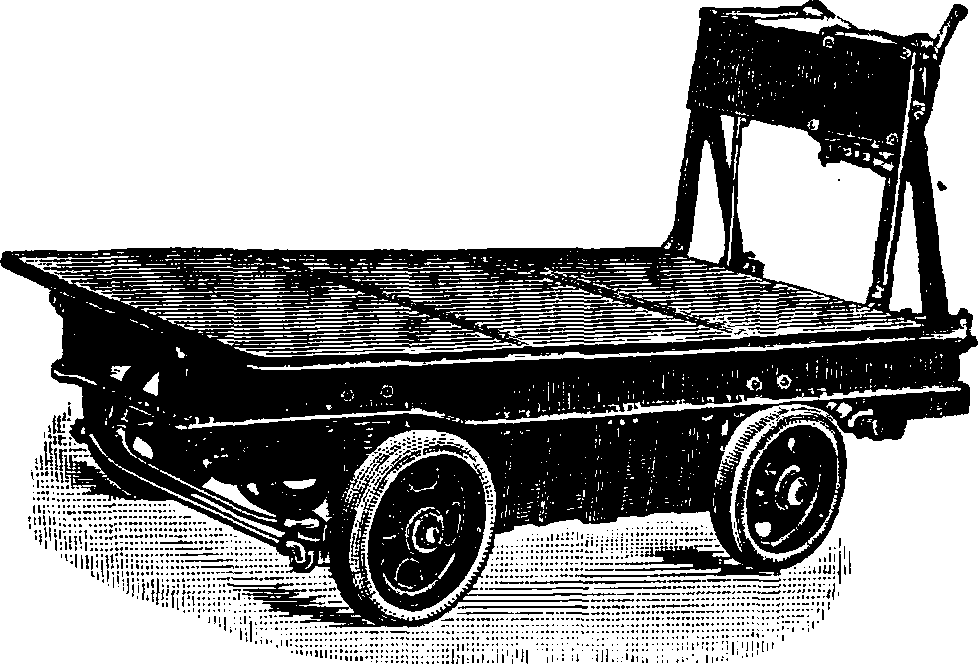
Фпг. 20. Обыкновенная аккумуляторная тележка. дов сравнительно небольших грузов, товаров или почты по улицам города, посетителей на обширной территории большой выставки и т. д.
Аккумуляторные батареи для освещения ж.-д. вагонов, помещаемые обычно под кузовом вагона, заряжаются во время хода поезда специальной динамомашиной и разряжаются во время стоянки. В СССР применяется система Тюдор - Розенберг, то есть установка с А. Тюдор и динамомашиной Розенберг. А. имеют емк. 370 Ah при 10-часовой разрядке. В этой области применения А. щелочные успешно вытесняют свинцовые вследствие своей большой выносливости как механической, так и электрической. Осветительные А. для автомобилей применяются в виде батарей из 2—6 свинцовых А. или в полтора раза большего числа щелочных. Применяемые в СССР А. типа «ЦВ> имеют емкость 40, 60 или 80 Ah; щелочные А. в этой области успешно конкурируют со свинцовыми. Старторные А. служат для пуска в ход бензинового двигателя, взамен ручного разворачивания. От них требуется кратковременный очень сильный ток; часто служат они и для освещения автомобиля. Свинцовые А. в СССР для стартерных батарей изготовляются типа «СТ», емк. 60, 100 и 150 Ah и собираются в батареи из 3 или 6 последовательно соединенных элементов. Щелочные А. и в этой области имеют преимущество перед свинцовыми.
3) Переносные А. имеют чрезвычайно разнообразное применение и разнообразные размеры и формы. Там, где имеется возможность заряжать А., они вытесняют элементы. Щелочные А., как не требующие столь тщательного ухода и более прочные, успешно конкурируют со свинцовыми во всех областях применения переносных А., кроме тех, где требуется очень медленная разрядка (например сигнализация). Для ра диоустановок применяются специальные, главн. обр. переносные аккумуляторные батареи, о которых см. Батарея. Для той же цели · изготовляются и щелочные А., состоящие из двух пластин. Лабораторные А. изготовляются в стеклянных сосудах, емкостью (свинцовые) 12,5, 25, 37,5 или 50 Ah, типа «ПО». Для сигнализации и телефонии широко применяется у нас специальный тип свинцовых А. — «Аккомет», приспособленный для очень слабых разрядных токов и отличающийся сравнительно малым саморазрядом. Для пожарной сигнализации применяются А., емк. около 60 Ah, рассчитанные на медленную разрядку, с сравнительно редкими зарядами. Для рудничных переносных ламп применяются свинцовые А. емк. ок. 6 Ah, разрядной силой тока 0,85 Ah (зарядная сила тока 1, 0,5 А). Для такого же фонаря применяется батарейка из 2 щелочных А.; начальное напряжение батареи 2,48 V. Батарейка при токе 0,72 А имеет емкость 7 Ah и зарядную силу тока 3 А. Для лабораторных целей иногда применяются высоковольтные батареи из большого числа (до 500) последовательно соединенных А. небольшого размера и небольшой емк. для получения источника энергии небольшой мощности, но высокого напряжения, до 1 000 V, — обычно для измерительных целей. Такие батареи собираются в специальных шкафах, в которых А. установлены на полках и хорошо изолированы друг от друга и от стенок. Батарея из 800 А., устроенная Планте и снабженная системой конденсаторов с особым переключателем («реоетатическая машина»), позволила изобретателю воспроизвести шаровую молнию и другие загадочные явления атмосферного электричества.
Особняком стоят безъемкостные А., изготовленные инж. II. А. Капица для опытов над сверхмощными магнитными полями. Его А. служили только для того, чтобы в лабораторной обстановке давать огромный мгновенный толчок тока в несколько тысяч А, получающийся при коротком замыкании такой батареи. Безъемкостные А. могли бы получить и другое применение— в качестве посредников для преобразования тока при помощи редуктора-преобразователя системы С. А. Кукель (сов. патенты №№ 1 738 и 1 623).
20. Экономика. Несмотря на многочисленные применения А. и даже на то, что чуть ли не с каждым годом появляются новые и новые применения А., они, в сущности, совершенно не удовлетворяют основным требованиям, которые должны были бы предъявляться к электрическим машинам, служащим для накопления электрической энергии. Они имеют большой удельный объём и уд. вес, высокую стоимость и сравнительно небольшой кпд. Изобретение железо-никелевых А. не изменило по существу положения, и можно наверняка сказать, что для разрешения задач аккумулирования электроэнергии должен быть найден совершенно другой принцип. Вопрос об экономической выгоде применения А. зависит,
конечно, прежде всего от условий их работы, и поэтому вопрос о том, при каких условиях затраты на аккумуляторы и на их зксплоатацию окупаются приносимыми ими выгодами, разрешается различно в различных отраслях применения. Приводим ориентировочные цифры, характеризующие расходы на батареи А.: стационарные А. на
1 kW в течение 3 ч. имеют вес в среднем 150 килограмм (от 425 до 500) и требуют площади пола 0,7 м2; стоимость их на 1 kW в советских условиях, с установкой, но без здания, в среднем — 400 р.; по америк. данным 1922 г., эта стоимость колеблется от 160 до 500 р.; эксплуатонные расходы, включая амортизацию, колеблются от 4 до 10% от первоначальной стоимости; низшая цифра относится к батарее, играющей исключительно роль аварийного резерва. Батареи для электромобилей требуют в среднем площади пола 0,12 м2 на 1 kW и весят 105 килограмм. Следующие цифры характеризуют распространение А. в различных областях. В С.-А. С. Ш. в 1920 году находилось в работе 193 стационарных свинцовых батареи, на общий запас энергии в 177 000 kWh при одночасовом разряде. Для освещения ж.-д. вагонов, для телефонов и сигнализации имелось ок. 700 000 Ah. Для освещения автомобилей (етарторные А.) и для воспламенения смеси двигателей внутреннего сгорания применялось всего 15 000 000 Ah па суммарный запас энергии ок. 3 000 000 kWh. Для осветительных станций на фермах было в работе 3 000 000 Ah на 1 000 000 kWh. Для электрических автомобилей, аккумуляторных тележек (уличных, шахтенных, фабрично-заводских), тракторов, аккумуляторных локомотивов — 1 166 000 Ah на 440 000 kWh. В СССР в 1924/25 годах было изготовлено Гос. аккум. трестом, в круглых цифрах, стационарных А. 300 т, А. для освещения автомобилей и старториых — 3 000 штук, для освещения ж.-д. вагонов—3 000, телеграфных, сигнализационных и тому подобное.—
2 000, для радио —10 000. В америк. данных указаны только свинцовые А., данные по СССР включают и щелочные типа Юнг-нера, продаваемые Гос. аккум. трестом. В 1924/25 годах трестом продано А. на 2,3 млн. р., а в 1925/26 годах на 3,2 млн. р.
21. Монтаж А. Батареи переносных и большинства подвижных А. собираются в деревянных ящиках, которые окрашены кислотоупорным или щелочноупорным составом. Более крупные из таких батарей А. изолируются от стенок ящика и друг от друга фарфоровыми или эбонитовыми прокладками. Для щелочных А., имеющих металлические баки, изоляция их друг от друга необходима во всех случаях. Для стационарных А. должен быть отведено специальное помещение, t° которого не. должна превышать t° наружного воздуха в жаркие дни и не должна понижаться ниже нуля, больше чем на несколько градусов. Помещение должен быть сухим, очень хорошо вентилироваться (для больших батарей необходима искусственная вентиляция, обязательно вытяжная, а не вдувная), не содержать никаких механизмов, быть безопасным в пожарном отношении, выкрашенным кислотоупорной краской, иметь це ментный пол, покрытый слоем чистого асфальта, с уклоном и канавками для стока жидкостей (фигура 21). А. устанавливаются па

Фигура 21. Общий вид стационарной аккуммуля-торной батареи. деревянных пропитанных брусьях, — которые ставятся при напряжении выше 100 V на метлахских плитках, — или на стеклянных ножках. Если последовательно соединено больше 36 А., то они ставятся на 4 подкладках из фарфора (фигура 22и 23). Свинцовые стационарные А. имеют стеклянные или, чаще, деревянные, обитые внутри свинцом баки. А. располагаются на стеллажах обычно вдоль, изредка поперек (небольшие А.).
Положительныещла -стины одного А. соединены с отрицательными пластинами другого общей свинцовой полосой, к которой они припаиваются обычно водородным паяльником с помощью специальных металлических форм или паяльных щипцов. От нескольких концевых А. идут провода к элементному коммутатору.
22. Уход за А. Зарядка А. производится либо при постоянной силе тока, либо при постоянном напряжении, либо при
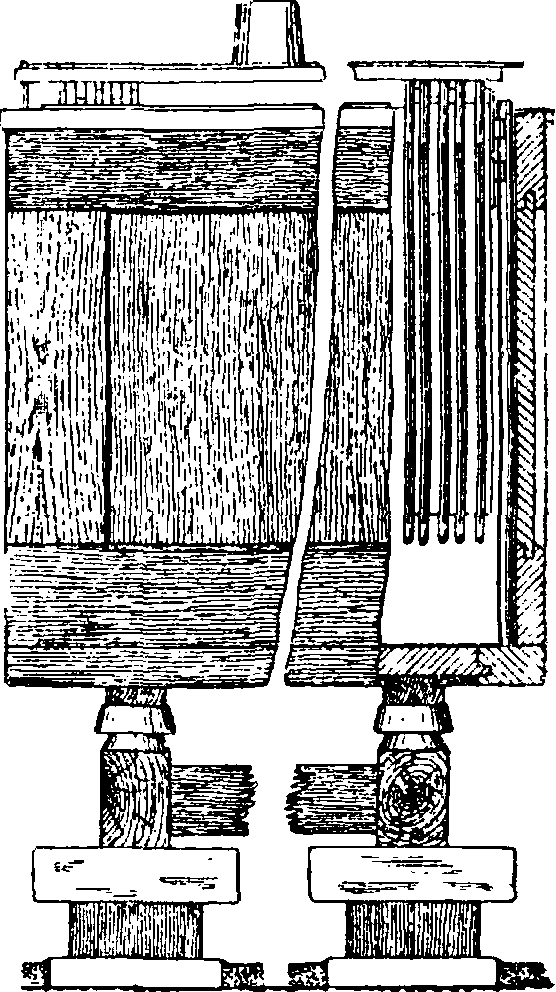
Фигура 22. Установка стационарного А.
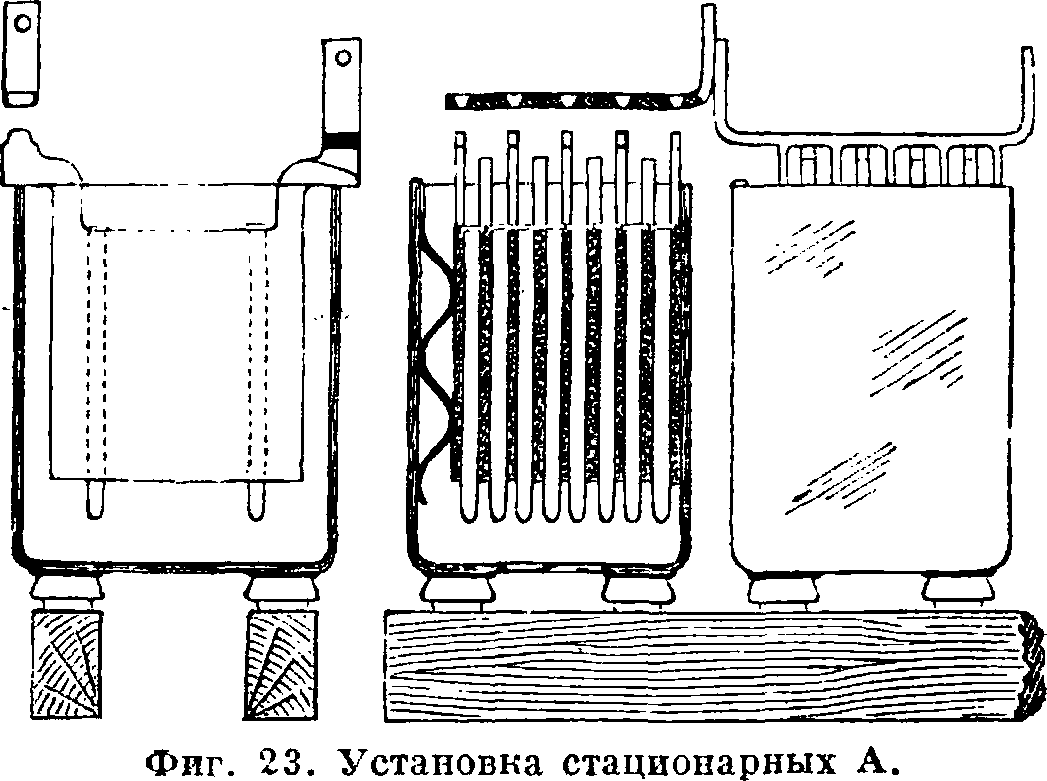
постоянной мощности. Первый случай в чистом виде для больших батарей применяется редко, т. к. обычно после газообразования сила тока должна уменьшаться. Недостаток способа заключается в требовании широкого изменения напряжения во время зарядки, для чего необходима специально рассчитанная шунтовая динамо или вольтодобавочная машина .(смотрите). Зарядка при постоянной силе тока с уменьшением последней в конце ее — наиболее распространенный способ. Зарядка при постоянном напряжении в чистом виде тоже редко применяется, т. к. сила тока при этом в начале зарядки чрезвычайно велика; чаще при этом способе поддерживается вначале постоянное напряжение, меньшее, чем конечное, и т. о. получают 2 или 3 ступени силы тока. Зарядка при постоянной мощности требует регулировки динамо по ваттметру. Конечное напряжение А. при зарядке 2,5—2,75 V находится в зависимости гл. обр. от силы тока. У свинцовых А., кроме специальных типов, максимальная скорость полной зарядки— 4 часа, у щелочных — значительно меньше. У больших батарей зарядка производится иногда по группам. Малые А. можно заряжать от осветительной сети постоянного тока через ламповый реостат, а от сети переменного тока — через выпрямители (смотрите). Для переносного свинцового А. зарядный ток обычно равен 10-часовому разрядному и продолжается 12 ч., если А. был вполне разряжен. Неизвестная зарядная сила свинцового А. с решетчатыми положительными пластинами определяется делением на 125 произведения из высоты пластины в сантиметров на ширину и на число положительных пластин; для поверхностного А. можно допустить в 2—2г/2 раза больше. Приблизительная емкость получится, если умножить вычисленную, как указано выше, зарядную силу тока решетчатого А. на 10, а поверхностного—на 3. Эти цифры, конечно, грубо ориентировочны, т. к. емкость зависит от типа пластин. Для суждения о состоянии большой батареи из многих А. выбирают несколько контрольных, за к-рыми наблюдения ведутся тщательно и регулярно. Наблюдения при зарядке и разрядке, а также в случае ремонта, должны записываться в аккумуляторный журнал. Первая зарядка производится обычно значительно дольше нормальной (в 2—3 раза). О состоянии разряда свинцовой батареи А. можно судить по плотности электролита в контрольном А., если ведутся регулярные записи. Почти все болезни свинцового А. сопровождаются уменьшением плотности электролита ниже нормы.
23. Очистка А. от осадка и смена электролита. У свинцовых А. при постоянной работе надо по истечении двух первых лет, а позже—раз в год, очищать баки от осадка; к этому времени приурочивают подробный осмотр пластин, частичную их замену и другие ремонтные работы. В больших стационарных А. осадок выкачивается специальной помпой, а в остальных требуется вынуть пластины, слить электролит в запасный сосуд и сполоснуть бак. Между пластина ми промывкой или палочкой удаляют «мостики» из отложений осадка. Перед очисткой аккумулятор разряжается. Если положительные пластины очень разрыхлены, промывку делать нельзя. Осадок больших батарей покупают аккумуляторные заводы. Если электролит очень загрязнен посторонними примесями, его надо заменить новым. У щелочных А., при постоянной работе, каждый год и при понижении плотности электролита ниже 1,16 следует заменять электролит новым, плотностью 1,21. Юнг-неровские А., потерявшие с течением времени емкость, «оживляются» зарядкой в специальном электролите. Отстающий А. в батарее, у которого напряжение при замкнутом разрядном токе и плотность ниже других, который позже закипает при зарядке и не доходит до нормального напряжения, нужно осмотреть для выяснения причины неисправности (например короткое замыкание между пластинами); по устранении причины — зарядить отдельно или специальной маловольтной дииамомашиной, или выключением его во время разрядки и включением на время зарядки. Если даже со значительной зарядкой А. не восстанавливается, то надо подвергнуть его обработке, как во всех случаях сульфирования пластин: уменьшить плотность электролита до 8° Вб и дать длительную зарядку в слабом электролите. При продолжительном бездействии свинцовая батарея А. должна оставаться или в сухом виде, или в ослабленном электролите. В первом случае батарей разряжают до конца и промывают пластины, во втором случае батарее дается перезарядка в ослабленном электролите. Щелочные А. могут оставаться в бездействии сколько угодно времени в любом состоянии, но обязательно в электролите. с. купель.
Лит.: Грюнвальд, Устройство и употребление электрич. аккумуляторов, СПБ., 1895; Карпов В. А., Элементы и аккумуляторы, 1927; Флоренский, П., «Электричество», 6, 1923; Наставл. по уходу за свинц. телеграфн. аккумуляторами, НКПС, М., 1922; Комаров В. С., Аккумулят. генерат. установки связи, «Связь», М., 1926; Александровский С. И., Аккумуляторы Эдисопа, Николаев, 1913;×вольсон О. Д., Курс физики, т. 4, стр. 61 7, ГИЗ, Берлин, 1923; Plant 6 G., Recherches sur 1’dlectricitd de 1859 5,1879, P., 1884; PI ant 6 G., Untersuchung iiber Elektrizitat, Wien, 1886; Dolezalek F., Die Theorie d. Bleiakkumulators, Halle, 1901 (франц. перевод: Dolezalek F., La thdorie de 1’accumulateur au plomb, P., 1902); Jumeau L., Etude rdsumde des accumulateurs dlectriques, P., 1924; Strecker K., Jahrbiicher d. Elektrotechnik, Munchen; J u me a u L., Revue gdn. de l’dlectricitd, t. 16, SO, SI, P., 1924; F d г у Ch. et Chdneveau Ch., Revue gdn. de l’dlectricitd, t. 19, 8, S3, 1926; Теория двойной суль-фации: Graetz L., Handbuch d. Elektrizitat u. d. Magnetismus, В. 1, Lpz. 1912—18; Brown H. G., The Leadstorage Battery, L., 1922; Le Blanc M., Lehrbuch der Elektrochemie, Lpz., 1896; F d г y. Chdneveau, Paillard, Piles primaires et accumulateurs, P., 1925; Heim C., Die Akkumu-latoren f. stationare elektr. Anlagen, 6 Aufl., Lpz., 1923; Kretzschmar, Die Krankheiten d. Bleiakkumulators, 2 Aufl., Mtinchen, 1922.