 > Техника, страница 11 > Алюминий
> Техника, страница 11 > Алюминий
Алюминий
Алюминий, самый распространенный, третий после кислорода и кремния, элемент земной коры (8% всей земной массы). А.— серебристый металл с легким синеватым оттенком. Уд. в 2,7; по своей тягучести уступает только золоту и серебру. Плавится при 657° и кипит при 1 800°. Хорошо проводит тепло и электричество. Чистый А. почти не изменяется на воздухе, покрываясь лишь тонкой пленкой окисла, предохраняющей металл от дальнейшего воздействия кислорода. С щелочными, щелочноземельными и металлами редких земель А. образует группу наиболее электроположительных металлов, обладающих большим стремлением переходить в ионное состояние (смотрите Алюминия соединения). Характерно для А. его огромное сродство к кислороду; большинство металлич. окислов восстанавливаются им в металлы при высокой ί°, и эта реакция сопровождается выделением большого количества тепла (смотрите Алюминотермия). А. соединяется также энергично с галоидами, а при высокой t° и с азотом, фосфором и серой. В разбавленной соляной или серной к-те А. растворяется с выделением водорода. Едкие щелочи легко растворяют А. с образованием алюмината: 2А1 + 2КОН + 2Н1!0=2КАЮ2+ЗН2. Чистый А. не действует на воду (даже и при 100°), но в виде ртутной амальгамы он разлагает воду с образованием гидрата окиси А. и выделением водорода. А. хорошо поддается прокатке, штамповке и ковке как в горячем, так и в холодном состоянии. Удовлетворительного припоя для А. до сих пор не существует, и для соединения двух кусков А. в одно целое их приходится сваривать расплавленным А.
Применение А. многообразно — как в виде чистого металла, так и в виде сплавов с медью, марганцем, никелем, цинком, магнием, кремнием, известных под названием бронз, дуралюминия, силумина и т. д. (алюминий употребляемый для этой цели, должен обладать надлежащей чистотой: хороший металл не должен содержать более 0,01% натрия, 0,3% железа и 0,5% кремния). Обладая большим сродством к кислороду (при образовании А1203 на 1 килограмм А1 выделяется 7 041 Cal), А. находит применение в алюминотермии для получения тугоплавких, трудновосстановимых металлов из их окислов—хрома, марганца, железа, никеля, кобальта, титана, молибдена, вольфрама, ванадия и др.,—а также в сталелитейном деле в качестве раскислителя. Обнаруживая значительную стойкость против разъедающего действия многих хим. реагентов и растворов, А. находит все возрастающее применение в различных областях хим. промышленности как конструктивный металл. Широко распространены изделия из него для нужд домашнего обихода и военного снаряжения. Обладая значительной легкостью и хорошей электропроводностью (уд. эл. сопротивление при 20°=2,828μΩ; эл.-проводимость единицы объёма составляет0,6 от эл.-провод, чистой отожженной меди, а эл.-провод, ед. веса алюминия в 2 раза выше таковой для меди), металлич. А. приобретает большое значение в качестве материала для изготовления проводников электрич.тока. Вследствие низких механич. качеств (тв. по Бри-неллю 25; вр. сопр. разрыву ~ 8,5 килограмм/мм“ пр. пропорц. ~ 5,8 килограмм/мм2 и удлин.~20%) А. в чистом виде находит ограниченное применение в качестве конструктивного металла в машиностроении, но его легкие сплавы типа дуралюминия широко распространены в авио- и моторостроении (вр. сопротивление их ^36 килограмм/мм“) пр. поопорц. ^5 22кг/мм“; удлии. Ξ3* 14%; уд. в ^ 3,3).
Впервые в 1827 г. Велер получил А. в виде серого порошка, блестящего при полировке, действием металлич. калия на безводный хлористый А. (А1С13). В 1854 г. Бунзен и Девиль получили А. электролизом расправленного хлористого А. Работы английских исследователей выяснили возможность получения А. из естественного криолита, незадолго перед тем открытого в Гренландии, действуя на него металлич. натрием. На основании этих работ Девиль предложил действовать металлич. натрием на смесь хлористых соединений натрия и А. с иек-рым количеством криолита. С этим видоизменением способ Девиля сохранил доминирующее положение в технике до появления современного электрического способа получения А. Металлический А., получавшийся способом Девиля. не был чист: он содержал от 0,1 до 0,5% Na. от 0,3 до 0,4% С, кроме того, Si от 0,04 до 2,87% и Fe от 1,6 до 4,88%.
Производство А. состоит из двух самостоятельных операций: получения чистого глинозема (А1,03) и электролиза его способом H6roult-Hall.
I. Получение А1203. Исходным материалом для получения глинозема служит боксит (смотрите) — продукт выветривания горных пород в условиях тропического или субтропического климата, содержащий в значительных количествах гидратпые формы глинозема А1203-ЗН20 (гидраргиллит, гиббсит) и А1203-Н20 (диаспор). Наряду с последними в боксите всегда находятся большие или меньшие количества глины, различных форм соединения Fe203, Ti02 (обычно 0,5—2,0%) и в незначительном количестве SiO>, MgO, CaO и другие примеси. Для переработки на глинозем идут в особенности малокремнеземистые красные бокситы с содержанием А1203 не ниже 50%, Fe203 — до 15% и несколько выше (последнее менее жела тельно), SiO 2 — по старым нормам не свыше 3%. В настоящее время содержание Si02 в бокситах допускается более высокое, до 7—10%, а в некоторых случаях оно может быть даже и выше.
В технике распространены гл. обр. два способа переработки бокситов: прокаливание с содой и обработка крепким раствором NaOH при повышенных t° (под давлением). В обоих случаях перед обработкой боксит б. ч. подвергают обжигу для удаления конституционной воды и затем измельчению. Оба способа переработки боксита основаны на образовании растворимого в воде алюмината натрия при взаимодействии щелочи с А1203 боксита. Полученные растворы алюмината отделяются на фильтр-прессах от нерастворимого остатка, содержащего всю Fe203 и большую часть Si02, заключавшихся в боксите. Si02 находится в нерастворимом остатке в форме алюмосиликата Na20·Al203-2Si02. Из вышедших в фильтр-прессы и просветленных алюминатных щелоков выделяется глинозем действием С02 или прививкою кристаллов А1(ОН)3.
1) Способ обработки бокситов содой при высоких t° был впервые разработан во Франции Ле-Шателье (первый патент появился в 1858 г.). По этому способу тонко измельченные боксит и сода смешиваются в таких количествах, чтобы на каждую молекулу А1203 и Fe203приходилось 1,0—1,2 молекулы Na20. Смесь после прокаливания в печи при 1 100 — 1 200° (пирогенный способ) быстро выщелачивается водой (гораздо лучше раствором щелочи, так как иначе, в случаях незначительного содержания в бокситах Fe203, могут произойти значительные потери в нерастворимом остатке А1203). При выщелачивании водой, по данным практики, в растворимое состояние переходит 2/3—8/в, в среднем 3/4, всего А1203. Горячий алю-минатный щелок, отделенный от нерастворимого остатка, содержит в л около 170 г А1,03 и 182 г Na20, то есть молекулярное отношение А1203: Na20=l : 1,8. В нек-рых случаях содержание Na20 в щелоках понижается, но, повидимому, в нормальных случаях не падает ниже значений след, отношения: А1203: NaaO=l : 1,3. Выделение гидрата глинозема из щелоков производится углекислотой, получаемой в известково-обжигательной печи специальной конструкции; концентрация С02 в 20—25% вполне достаточна. Отделенный от маточного раствора и промытый на фильтр-прессе гидрат глинозема, прокаленный около 1 200°. представляет белый легкий порошок.
2) По способу Банера (Петербург, 1892 г., Тентелевский завод) обработка крепким раствором NaOH (45° Be) производится в железных аппаратах, пои перемешивании под давлением 5—6 atm (~160°) в течение 2—8 ч. Полученный в автоклаве алюминатный щелок разбавляется водою до уд. в 1,23 (26,9° Be) и поступает на фильтр-прессы для отделения от нерастворимого остатка. Из полученного просветленного алюминатного щелока с молекулярным отношением А1203: Na20=lj;: 1,8 гидрат глинозехма выделяется при постоянном помешивании по прибавлении нек-рого количества свежеосажденного кристаллического А1(ОН)3. Выделение глинозема считается законченным, когда в щелоке молекулярное отношение А1203 : Na20 достигнет величины 1:6. Операция выделения глинозема занимает до 60 ч.; первые 70% А1203выделяются в течение 36 ч.
Получаемые на з-дах алюминатные щелока всегда содержат в себе нек-рое количество кремнекислоты, присутствие которой в них представляет нежелательное явление, т. к. при выделении А1203 выпадает Si02, загрязняя этим глинозем. Как показывает практика, при осаждении первым выделяется гидрат окиси алюминия, и лишь позднее начинает осаждаться и кремнекислота. Благодаря этому, производя фракционированное осаждение, можно получить глинозем, удовлетворяющий необходимым требованиям в отношении содержания в нем Si02. Полученный глинозем после прокаливания показывает следующий состав: гигроскопич. воды 0,33%, конституцион. воды 0,50%, Si02 0,15%, Fe2Os 0,007%, Na20 0,30%, CaO 0,013%, A1203 (по разности) 98,70%. Обычно содержание A1203 колеблется от 98 до 99,5%. Обычный состав нерастворимого остатка таков: гигроскопич. воды 39,42%, конституцион. воды 4,24%, Si02 3,52%, Fe203 37,57%, ТЮ2 4,55%, А1203 7,00% и Na20 3,67%. Полученный остаток подвергается выщелачиванию водой для удаления из него Na20. Промытый остаток находит различные применения: в качестве очистит, массы в производстве светильного газа, как материал для изготовления красок (охр).
Ход производства явствует из схемы завода сернокислого алюмммя (фигура 1). Исходным материалом служит, например, французский боксит с содержанием 25% окиси железа. После предварительного измельчения он подвергается обжигу (350—400°) во вращающихся барабанных печах d для удаления органич. веществ и воды и для облегчения дальнейшего тонкого помола. При помощи ленты транспортера и элеватора е прокаленный боксит попадает в шаровую мельницу /. Чрезвычайно тонкое измельчение весьма важно для хорошего выхода алюмината. Подготовленный т. о. к извлечению глинозема боксит хранится в силосоподобном ящике д, откуда его берут по мере надобности. Отвешенное количество боксита замешивается в особом сосуде г с возвращенным из производства и доведенным упариванием вгдо46°Вё щелоком и подается в стоящие ниже автоклавы к емкостью в 3—4 м3, снабженные мешалками и обогреваемые паром. Реакция продолжается около 6 ч., причем извлекается до 95% содержащегося в боксите глинозема. Полученный в автоклавах алюминатный щелок крепостью в 50° Вё разбавляется затем в сосудах I для смешивания до 30° Вё, после чего идет на фильтр-прессы т и п. Остаток на фильтрах содержит гл. обр. окись железа. Прозрачный щелок подается из сборника с помощью центробежного насоса о в цилиндры для разложения р, где под действием взвешенного гидрата окиси алюминия, при сильном перемешивании, происходит распад алюмината на гидрат окиси алюминия и едкий натр. Операция эта требует строгого соблюдения определенных условий: t°, скорости перемешивания, концентрации щелока и прочие, и продолжается 36—48 ч., после чего около 70% растворенного глинозема переходит в осадок. Перемешивание прекращают, декантируют жидкость и отжимают и промывают гидрат окиси алюминия на фильтр-прессе д. Маточный раствор сгущается в выпа-ривательном аппарате до 46° Вё и служит для нового разложения боксита.
Преимущества способа Байера перед пирогенным заключаются в большой чистоте продукта (содержание кремнезема при мок ром способе 0,02%, при пирогенном 0,3%), в более полном извлечении глинозема из боксита, в меньшем расходе топлива и рабочей силы и, наконец, в отсутствии, благодаря применению гидрата окиси алюминия
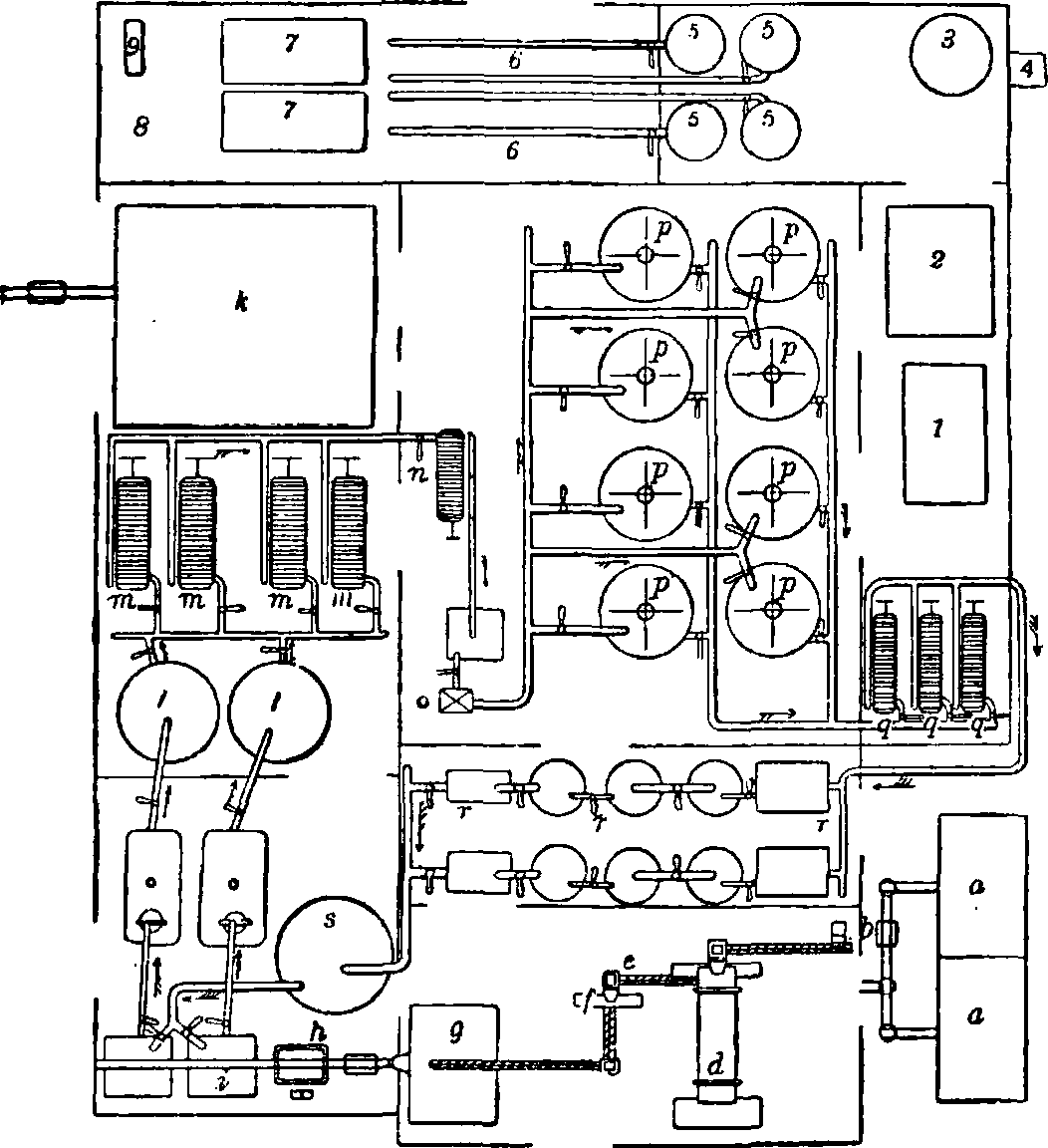
Фигура 1. Схема завода сернокислого алюминия: а—склад боксита, Ь—вагон, h—весы, s—резервуар для едкого натра, г—упариват.чаши, 1—установка для сушки, 2—склад глинозема, 3—бак для кислоты, 4—подъемник, 5—чаны для растворов, 6—кристаллизационная мастерская, 7—склад Al2(S04)a,
8 — упаковочное отделение, 9 — дезинтегратор. Стрелками обозначен последовательный ход обработки боксита (сырой бокситный щелок -> алюминатный щелок -> разбавл. раствор едкого натра -» концентр, раствор едкого натра).
для осаждения, побочного продукта—кристаллической соды, которая не всегда находит сбыт. Качество сернокислого алюминия, полученного по обоим щелочным способам (путем растворения гидрата окиси алюминия в серной кислоте), примерно одно и то же. Что же касается глинозема для производства алюминия, то, в виду низкого содержания кремнекислоты, преимущество на сто1 роне способа Байера. Кроме этих методов, нек-рое применение получил способ, предложенный Пеняковым. Для разложения боксита этим способом вместо соды служит сернокислый натр с прибавлением пирита. При сплавлении пирита с бокситом и сульфатом образуются алюминат натрия, окись железа и,сернистый газ: 11А1203 + + 2FeS2 + llNa2S04=UNa20 · А1203 + -j- Fe203 -f 15S02. Выделяющийся сернистый газ употребляется для получения из поваренной соли сульфата натрия и соляной кислоты (способ Хергривса). Алюминатный щелок перерабатывается углекислотой на гидрат окиси алюминия и соду. В последнее время усиленно разрабатывается проблема получения глинозема из глины. Так, на заводе Грисгейм-Электрон испытывается опытная установка для получения глинозема из глины с помощью соляной кислоты. Проблему эту, имеющую огромное техническое значение и для СССР, однако, нельзя считать еще разрешенной.
II. Получение А. электролизом. Электролиз раствора глинозема в криолите ведется с угольными электродами. Необходимое для поддержания ванны в расплавленном состоянии тепло сообщается электрическим током. Разложению подвергается гл. обр. окись алюминия, которая обладает более низким потенциалом разложения (2,8 У),чем фтористый А. (4,6 V) и фтористый натр (5,9 V). Выделяющийся на катоде А. накопляется на дне ванны, а кислород соединяется с углем анода в окись углерода А1203+ЗС=2А1+ЗСО, (1)
сгорающую далее за счет кислорода воздуха в углекислоту. Из того, что расход угля при благоприятных условиях меньше вычисленного по ур-ию (1), явствует, однако, что^ча-стично процесс идет также по схеме:
2А1а03+ЗС=4А1+ЗС02. (2)
Содержание глинозема в растворе колеблется от 10 до 20%. При обеднении раствора глиноземом усиливаются побочные реакции—выделение фтористых соединений (CaFa, SiF4) на аноде и натрия на катоде, что сильно понижает качество А. Чтобы держать состав смеси постоянным и избежать побочных реакций, в ванну через короткие промежутки времени добавляют глинозем, а иногда и немного криолита. С целью понижения 1°пл. ванны и уменьшения уд. в электролита прибавляют еще различные количества нек-рых солей, гл. обр. плавиковый шпат (CaF2), фтористый А. и хлористый натр. Смесь глинозема и криолита, содержащая до 20% глинозема, плавится ок. 1 000°; прибавление фтористого А. понижает ί°πΛ. до 800—850°,если же добавить еще поваренной соли, то ί°ηΛ. падает до 700°. Хлористый натр, однако, быстро улетучивается. Поэтому с постоянным добавлением хлористого натра не работают, а пользуются им часто для пуска в ход пришедшей в неисправность ванны или новой. Обычная t° ванны при нормальной работе—800—900°. При более низких t° выход А. ухудшается. Для поддержания нужной t° анодную плотность тока держат в границах 70—100 А/дм“. При таких условиях напряжение на клеммах, при к-ром достигается наилучший выход А., составляет 7 — 8 У. При нарушениях в электролизе вольтаж возрастает до 8—10 V. Существенную роль играет прибавление плавней также и в понижении уд. в электролита, к-рый должен быть всегда несколько меньше уд. в расплавленного А. Разность эта, однако, невелика, а при повышении t° она становится еще меньше; благодаря этому уже при небольшом изменении состава ванны или при быстром подъеме t° наблюдается всплывание А.; такая ванна не дает, конечно, никакого выхода А. Весьма важную роль играет чистота исходных материалов—глинозема, плавней и угольных электродов, т. к. все их загрязнения попадают в А., последующая рафинировка которого представляет трудности. Главнейшим исходным материалом служит глинозем, полученный почти исключительно вышеописанными щелочными способами из боксита. Некоторые алюминиевые з-ды (например французские) готовят для себя глинозем сами; другие по лучают его от специальных з-дов по производству глиноземных препаратов; поступающий на алюминиевые заводы глинозем отличается большой чистотой; содержание кремнекислоты в нем не превышает 0,1%. Габер приводит следующий анализ глинозема одной из крупных германских фирм (в процентах):
А1203. .. 99,594 NaaO.. . 0,050
Fe203. .. 0,032 Si02. .. 0,056
CaO. .. 0,018 H20. .. 0,250
Растворителем для глинозема служит природный или искусственный криолит. В настоящее время алюминиевые заводы применяют б. ч. искусственный криолит, который по стоимости не выше гренландского, но отличается большей чистотой. Наиболее целесообразными материалами для получения угольных электродов являются ретортный графит и нефтяной кокс от сухой перегонки нефти с содержанием золы не более 1,5%.
Электролитические ванны (фигура 2) представляют, клепаные железные ящики (из ко- ‘ inii тельного железа), ft -Η~ι|γ ty и скрепленные угольниками .Размеры ванн различны, в зависимости от числа анодов: в среднем, 2,4 ж дл., 1,3 ж шир. и 0,8 ж вышины, глубина же рабочего пространства обычно не превышает 0,3 ж. Для уменьшения потерь тепла стенки ванны облицовывают сначала огнеупорной кладкой, а затем стенки и дно выкладывают проводящей ток угольной набойкой А, в которую пропущена железная шина, соединенная с отрицательным полюсом источника тока. В целях улучшения электропроводности набойка впоследствии была заменена угольными плитами, изготовленными из такого же материала, как и аноды (фигура 3). Размеры и количество анодов
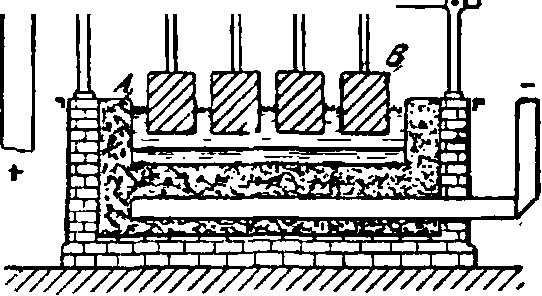
Фигура 2. Электролитическая ванна: А—угольная набойка, В—электроды.
| 1щт | S
1 |
ZEp
fi | |
77^!77P777777777777Z77Z^777?
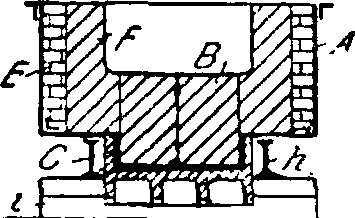
777777777777777777,
Фигура 3. Электролитическая ванна с угольными плитами: А—ящик из котельного железа, В— электродные плиты из угля, С—шипы для подводки тока, Е—огнеупорная кладка, F—масса для тепловой изоляции, h—балки, г—кирпичи. изменяются в широких пределах. При анодах небольшого поперечного сечения (например 8x10 см) их располагают четырьмя рядами, по 8 шт. в ряду. В настоящее время предпочитают, однако, более крупные аноды, весом в 45—90 килограмм, число которых соответственно уменьшают. Аноды В подвешены при помощи медных стержней к плоским медным шинам, расположенным на некоторой высоте над ванной (фигура 2). Сила тока при пользовании крупными ваннами составляет 15 000—20 000 А. Анодная плотность тока—70—100 А/0ж2. Состав применяемого электролита неодинаков на различи, з-дах и считается главным секретом производства. На нек-рых франц. з-дах, по литературным указаниям, растворителем служит гл. обр. криолит, иногда с небольшой примесью плавикового шпата. Другие з-ды пользуются смесью из 36% криолита, 44% фтористого А. и 20% фтористого кальция,что отвечает примерно составу AlF3-3NaF+3AlF3-(-3CaF2. Большого внимания требует пуск ванны в ход. Для этого с помощью небольших угольных стержней коротко замыкают аноды с катодным дном, засыпают нек-рое количество криолита и плавней и затем включают ток. По мере расплавления добавляют смеси, постепенно поднимая аноды и следя за равномерным распределением тока по всей ванне. Лишь после полного расплавления криолита приступают к прибавлению глинозема. Пуск ванны продолжается обычно два дня; для ускорения иногда прибавляют поваренной соли. При установившейся работе уход за аппаратами сводится к периодическим добавкам глинозема и иногда плавней, к регулированию и смене анодов и к выпуску накопившегося на дне ванны А. Последнюю операцию производят каждые
2—3 дня. Обычно А. вычерпывается железными ложками, причем часть металла оставляют в ванне, что облегчает собирание новых количеств. Иногда выгрузку производят также через выпускное отверстие в стенке ванны, выливая металл в чугунные формы. Полученный А. большей частью еще раз переплавляют в пламенных печах или тиглях, после чего он содержит от 98 до 99% А1. Некоторые з-ды выпускают еще более чистые продукты с содержанием А. до 99,5%. Выход А. теоретически равняется 0,337 г/Ah. При среднем рабочем напряжении в 8 У на 1 kWh должно получаться 42,1 г А. На практике степень использования тока колеблется от 58 до 76%. Расход энергии на 1 килограмм А. равен т. о. 30—40 kWh. Один kW-год дает 210 — 275 килограмм А. Расход материалов на 1 килограмм А. выражается на практике следующими цифрами: глинозема 2 килограмма, угольных анодов 700 —1 000 г, криолита 60—100 г и фтористого А. фтористого кальция 100 —150 г. Расход рабочей силы на изготовление электродов, электролиз и переплавку составляет от 0,04 до 0,045 чв-д. на 1 килограмм А.
Цены на А. сильно менялись с развитием способов его получения. В самом начале появления металлич. А. стоимость 1 килограмм металла была ок. 500 р. При установлении процесса Девиля цена 1 килограмм упала с 375 р. до 20 р. Эта цена держалась с незначительными колебаниями до 1887 г. В 1888 г., когда только что возникло электролитическое получение алюминия, металл хим. получения продавался около 16 р. 65 к. за 1 килограмм; в 1890 г. цена упала уже до 7 р., в 1891 г.—до 3 р. 70 к., а в 1900 г. она дошла до 1 р. До войны 1 килограмм металла стоил 56 — 75 к. Параллельно с падением стоимости алюминия возрастает и спрос на него. Перед возникновением электро-химического способа производительность алюминия была ничтожной, затем она быстро растет, что видно из следующей таблицы:
| Мировая | Мировая | ||
| Годы | производит. | Годы | производит. |
| в т | в т | ||
| 1885. | не > 3 | 1918. | 134 868 |
| 1890. | 193 | 1919. | 127 248 |
| 1895. | 1 835 | 1920. | 133 400 |
| 1900. | 7 300 | 1921. | 74 900 |
| 1905. | 11 500 | 1922. | 91 800 |
| 1910. | 43 800 | 1923. | 140 719 |
| 1913. | 68 200 | 1924. | 166 853 |
| 1916, | 93 227 | 1925. | 179 800 |
| 1917. | 120 304 |
Производство А. объединяется следующими финансовыми группами: 1) The Aluminium" С° of America, обнимает все производство С.-А. С. Ш. и Канады (Northern Alum. С° Ltd.) и часть Норвегии (Norsk Aluminium С°); 2) L ’Aluminium Framjaise— производство французское, итальянское и часть нор-вержекого; 3) Die Aluminium-Industrie Akt. Gesell-schaft с заводами в Швейцарии, Германии и Австрии; 4) The British Aluminium С° с заводами в Англии и Норвегии; 5) The Aluminium Corporat. Ltd.—с рудниками боксита в департаменте Var на юге Франции. В конце 1926 г. европейские концерны, а именно: L’Alum. Frang., Die Alum.-Ind. Akt. Ges., The Brit. Al. CJ и проч. мелкие европейские объединения организовали всеевропейский Алюминиевый синдикат для регулирования алюминиевого рынка Европы. Возникновение этого синдиката является попыткой европейской промышленности успешнее бороться с конкуренцией Америки, промышленность которой объединена в один концерн с производством около 50% мировой продукции.
О размерах спроса русского рынка на металлич. А. не в изделиях можно судить по количеству ввезенного металла за последние перед войной годы: с 1900 по 1911 гг. было ввезено последовательно: 327, 360, 704, 507, 819, 1 146, 909, 360, 422, 557, 606 и 1 359 т—числа колеблющиеся, но с явной тенденцией к возрастанию. В представленные данные совершенно не вошло количество А., ввезенного в изделиях, к-рое на основании статистики ввоза за 1913 г. составляло свыше 59% от количества А., ввезенного не в изделиях. Т. о. приведенные числа ввоза металлич. А. на самом деле следует значительно увеличить, почти вдвое, чтобы приблизиться к реальным потребностям русского рынка на этот металл в довоенное время. Во время войны ввоз А. сильно возрос: в 1915 г.—6 372 т, в 1916 г.— 5 028 тонн и в 1917 году — 3 636 тонн Современная потребность в А. исчисляется различно, в пределах от 3 000 до 10 000 тонн в год. На ближайшее пятилетие принимается цифра в 25 000 тонн Если принять увеличение потребности на каждое пятилетие, примерно, на 30%, то вся потребность на ближайшие 15 лет выразится в следующих цифрах: на пятилетия 1927—31 гг., 1932—36 гг. и 1937 — 42 гг. соответственно — 25 000 т, 33 000 тонн и 42 000 т, а всего 100 000 тонн Несмотря на значительную потребность в металлич. А., до сих пор в СССР нет ни добычи боксита, ни производства металлич. А. Такое положение“ дел объясняется гл. обр. тем, что только с 1917 г. на территории СССР стали известны месторождения бокситов. Вторая причина—высокая стоимость у нас электрич. энергии. Лишь детальные разведки в Тихвинском уезде (Череповецкой губернии), произведенные в период 1921—26 гг., с несомненностью установили присутствие здесь промышленных бокситовых месторождений. Как показывают химическ. исследования, состав тихвинских бокситов, как и всех вообще бокситов, очень разнообразен. Поэтому для подсчета запасов геологом
С. Ф. Малявкиным была предложена следующая их классификация:
Сорт прима SiO,< 10%; ΑΙ,Ο, > 50%;
I сорт ΑΙ,Ο, : SiO,> 3; AI,О, > 50% и SiO,<15%
II » AI,О, : SiO,> 2; ΑΙ,О, > 40%и SiO,<20%
III » А1,0, : SiO,> 1; AI,О, > 35%.
На основании этой классификации запасы бокситов тихвинского района представляются в следующем виде: сорт прима 373 000 т,
1 сорт 600 600 т, II сорт 703 100 ж, III сорт
2 420 700 ж. Помимо этого, есть указания на нахождение бокситов в Рязанской губернии (Раненбургский уезд) и в пермском районе (Журавлинское месторождение). Оба эти района пока остаются неисследованными. В виду этого развитие алюминиевой промышленности в СССР может планироваться лишь на использовании бокситов тихвинского района, примерно, следующего среднего состава: А12О3<<30% и Si02i>13%, чему будет отвечать смесь первых трех сортов бокситов. Т. к. тихвинские бокситы показывают сравнительно низкое содержание А1203 и высокий % Si02, то алюминиевое производство в СССР прежде всего будет зависеть от применения рационального, с экономической точки зрения, способа переработки их на глинозем. В этом направлении ведутся работы в Ленинградском горном ин-те (исследование электротермического способа, состоящего в восстановительной плавке боксита на 25%-ный ферросилиций и алюминат бария, с последующей переработкой алюмината на А1203), в Ленинградском политехническом ин-те и в Ин-те прикладной химии (исследование известково-натрового способа, состоящего в спекании боксита с СаС03 и Na2C03, с последующим выщелачиванием массы и осаждением из щелоков А1203). Выбор того или другого способа определяет и местоположение глиноземного завода: в первом случае—у Днепростроя (и тогда транспорт туда боксита), во втором—вблизи месторождения бокситов, в обоих случаях—электролитный завод у Днепростроя. Помимо этого, для установления алюминиевого производства необходимы организации производств фтористых соединений и электродов.
Лит.: Федотьев Π. П., Электрометаллургия, вып. 2, П., 1923; Курдюмов А. П., К вопросам создания в России алюминиевого производства, «Труды Ин-та прикл. минералог, и пегрогр.», вып. 6 и 23, М., 1923 и 1926; Труды I Всесоюзн. совещ. по цветным металлам, М.,1925; Левенштенн, Алюминий. Его производство и применение, «Журнал хим. пром.», 4. М., 1927; Grard С., L’aluminium et ses alliages, P., 1920; AndersonRob. J., Metallurgy of Aluminium a. Aluminium Alloys, N. Y., 1925; Mortimer G., Aluminium, L., 1920; Debar R., Die Aluminium-Industrie, Braunschweig, 1925.