 > Техника, страница 12 > Анализ газов
> Техника, страница 12 > Анализ газов
Анализ газов
Анализ газов, определение качественного и количественного состава газовой смеси. А. г. выделен в отдельную главу ана-литич. химии в виду значительного отличия применяемых в нем методов сравнительно с общей методикой хим. анализа. А. г. применяется: при изучении физиологии, газообмен а в организме животных и растений; при контроле отходящих газов заводских топок, а также генераторного газа и водяного газа (смотрите); при производстве серной к-ты, азотной к-ты, синтетич. аммиака, хлора; при исследовании газов минеральных источников (смотрите); при изучении боевых отравляющих газов; при определении гелия (содержащегося в некоторых минералах, в нефти), могущего быть использованным для наполнения аэростатов и т. д.
А. г. осуществляется: а) путем сжижения газов при помощи их охлаждения и последующей фракционировки; б) путем последовательного хим. поглощения отдельных составных частей смеси газов и измерения общего объёма смеси в результате такого поглощения; в) путем сожжения со ом ингредиентов смеси газов после прибавления к смеси определенных объёмов кислорода (или водорода); г) путем измерения показателя преломления смеси газов и сравнения его с показателем преломления газовой смеси заранее известного состава; д) путем измерения электрич. Фигура 1. Запаивающийся сопротивленияпла-сосуд для отобрания пробы, тиновой проволоки, протянутой в камере с тем или иным газом или со смесью газов, в зависимости от большей или меньшей отдачи проволокой теплоты Джоуля окружающему ее газу.
Чрезвычайно важное значение в А. г. имеет правильный отбор пробы. Для газа,

Фигура 2. Сосуд с притертыми пробками.

протекающего по трубам и каналам, правильнее всего отбирать пробу в том месте трубы, к-рое имеет наиболее узкое поперечное сечение. При анализе отходящих газов в топках целесообразнее всего отбирать пробу в том месте, где кончается видимая часть пламени, ибо далее, вследствие пористости каменной кладки дымоходов, газы в значительной степени разбавляются воздухом. В это место дымохода для изъятия пробы газа вводится короткая железная труба, к концу которой припаяна тонкая свинцовая трубка. При А. г. минеральных источников или шахт исследуемые газы пропускаются через особые сосуды, которые либо запаиваются, либо могут быть закрыты кранами с притертыми пробками (фигура 1, 2 и 3). Обычно при массовых технических А. г. качественный состав смеси газов бывает известен, и задача сводится к выработке методики быстрого и по возможности точного количественного определения содержания всех или некоторых входящих в газовую смесь ингредиентов.
При А. г. приходится чаще иметь дело с измерениями объёма, реже — с измерениями веса (например при определении С02). Измерения объёма газов производятся с учетом условий t°, давления и упругости паров воды (если сосуды, содержащие газы, замкнуты водой), и результаты этих измерений приводятся по известным ф-лам к нормальным условиям t° и давления (то есть к 0° и 760 миллиметров). Если V—наблюдаемый объём газа, В — показание барометра и f—давл. упругости паров воды при 1° наблюдения,

Фигура 3. Сосуд для отобрания пробы в минеральных источниках. то объём газа V, приведенный
- _ v(B—f)273 π
условиям, будет равен: V= 7b()QZf^+ty ПРИ
точных определениях пользуются в качестве замыкающей жидкости ртутью.
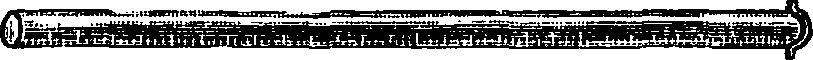
Фигура 4. Эвдиометрическая трубка.
Из методов и приборов следует назвать: 1) метод Бунзена—с измерением объёма исследуемых и поглощаемых газов в точно калиброванных путем наполнения ртутью, разделенных на миллиметров эвдиометриче-ских трубках (фигура 4); 2) газовые бюретки Бунте и Темпе л я, в которые можно ввести раствор реактива, поглощающего определенный газ из смеси, после чего можно произвести отсчет, показывающий уменьшение объёма газовой смеси (фигура 5 и 6); 3) аппарат О р с а, состоящий из газовой бюретки в 100 см3, находящейся в цилиндре с водой, и из нескольких абсорбционных сосудов, заполненных отрезками стеклянных трубочек, смоченных в каждом сосуде раствором реактива, связывающего хими-
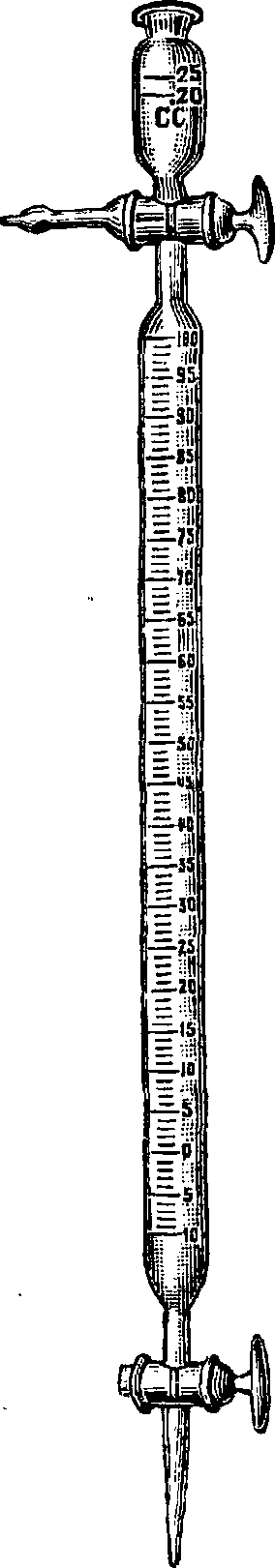
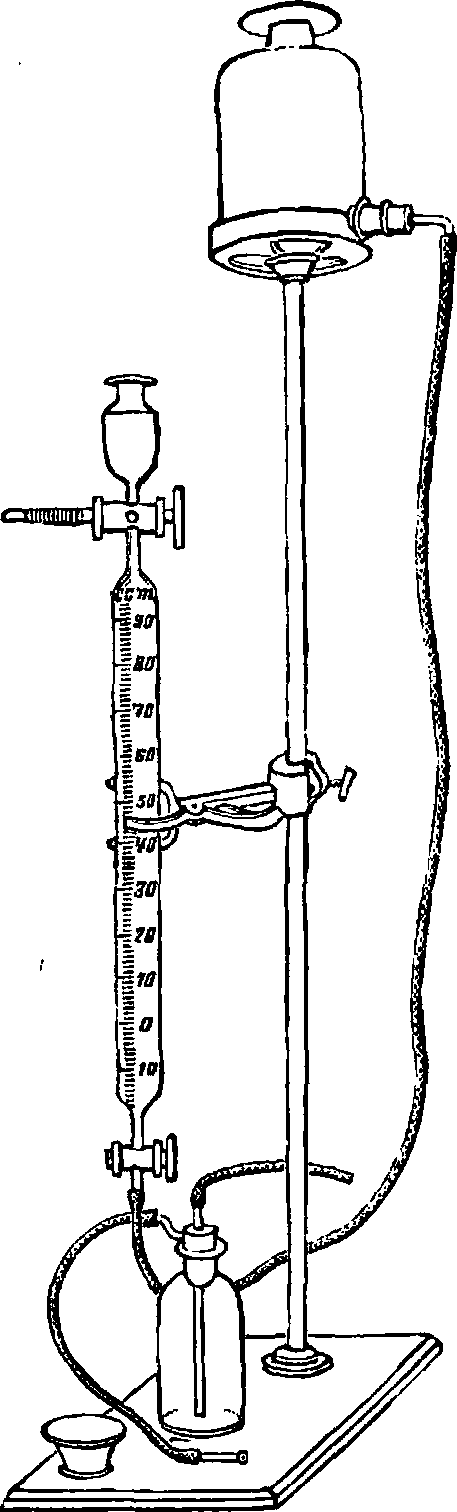
Фигура 5. Газовая бюретка Бунте. чески тот или иной газ; бюретка и все сосуды укреплены в общем переносном ящике-штативе; при помощи стеклянных кранов газовая смесь из бюретки м. б. пропущена последовательно через сосуды, в которых из смеси поглощаются те или иные ингредиенты, в зависимости от характера поглотителя. В видоизмененном аппарате
I
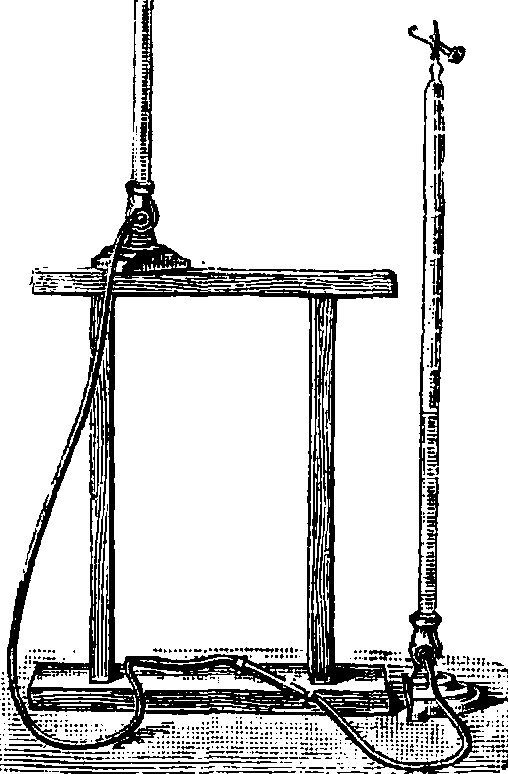
Фигура 6. Газовая бюретка Гемпеля.
Орса-Луиге имеется капиллярная трубка d (фигура 7)", выполненная платинированным асбестом для фракционированного сжигания водорода. Для более полного поглощения газа при действии на него поглощающего раствора пользуются газовыми пипетками (фигура 8), в которых можно удобно взбалтывать газ с раствором поглотителя. В тех случаях, когда содержание определяемого газа в исследуемой смеси очень незначительно (например содержание СО г в воздухе), приходится продувать через поглощающий прибор значительный объём испытуемой газовой смеси и измерять прошедйшй через поглотитель объём при помощи газовых часов, реометров и других приборов, измеряющих объём протекшего газа. В качестве методов поглощения различных газов можно указать: а) для кислорода 02: с Н2, поглощение металлической медью при накаливании, поглощение закис-ным хлористым хромом, поглощение влажным фосфором, поглощение щелочным раствором пирогалловой кислоты (в последнем случае приготовляются два раствора: 180 г КОН в 300 см3 Н20 и 12 г пирогалловой кислоты в 50 см3 Н20; сначала всасывают 5 см3 пирогалло-вого раствора, затем 30 см3 раствора КОН); б)для озона 03: пропускание газа через раствор KJ и оттитро-вывание иода гипосульфитом; в) для азота N2: за азот обыкновенно принимается остатох^ от поглощения всех прочих газов; если нужно отделить от азота аргон, то смесь пропускают через трубку с раскаленным Mg или Са: оба эти металла соединяются химически с азотом, но не действуют на аргон; г) для водорода Н2: водород определяется путем сожжения при действии палладиевого асбеста. При 100° Н2 прекрасно поглощается метаЛлич. палладием. По Паалю, коллоидальный раствор Pd с примесью пикрата натрия превосходно поглощает Н2. Закись азота N20 сжигается
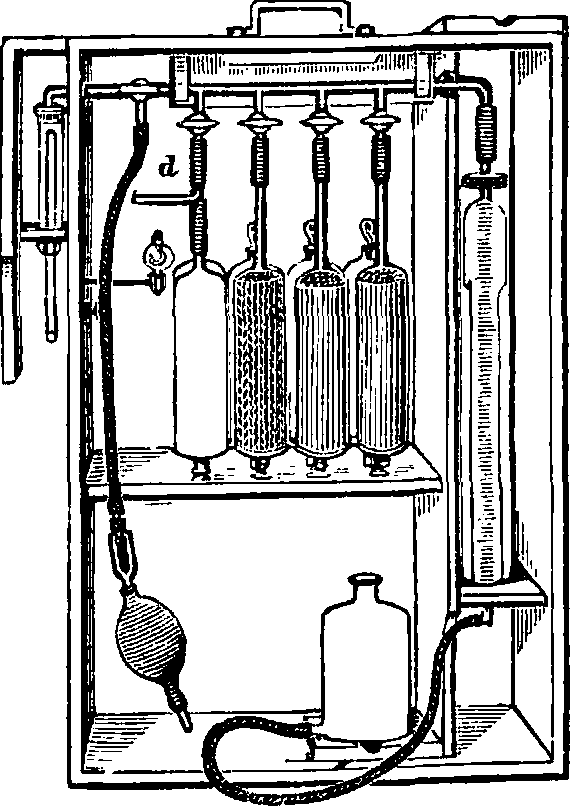
Фигура 7. Аппарат Лунге.
Орса-
с примесью Н2. Окись азота NO поглощается солями закиси железа. Углекислый газ СО а поглощается конц. раствором едкого кали или в трубках, наполненных пористыми кусками натронной извести. Раствор едкого кали содержит 100 г КОН в 200 см3 воды. Окись углеро-д а СО поглощается аммиачным или кислым раствором хлористой меди. В небольших количествах СО поглощается кровью и обнаруживается по спектру поглощения крови после прибавления восстанавливающих
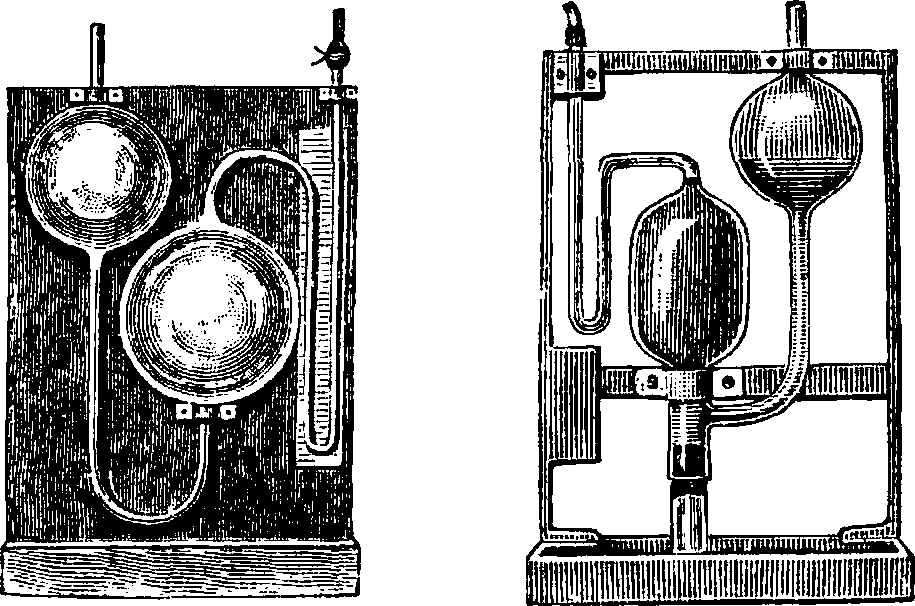
Фигура 8. Газовые пипетки. веществ .Болотный газ СН4 сжигается в кислороде; дает 1 объём СО2, для чего требует двух объёмов 02 по ур-ию: СН4+202==С02+2Н20. Этилен С2Н4 поглощается H2S04 или Вг. Ацетилен С2Н2 поглощается аммиачным раствором записной хлористой меди или аммиачным раствором серебра. Сероводород H2S поглощается солями РЬ или оттитровывается иодом. Сернистый газ S02 поглощается Вг или окисляется перекисью марганца, а затем осаждается солями Ва в виде BaS04.×л о р С1 вытесняет J из KJ. после чего Л оттитровывается гипосульфитом. При необходимости сожжения со ом или медленного сожжения нек-рых ингредиентов газовой смеси применяются особые ные толстостенные Пипетки, чтобы затем по уменьшению объёма сделать заключение о %-ном содержании сгоревшего газа, либо пипетки с накаливаемой электрич. спиральной проволокой (фигура 9). Еще проще и быстрее это сожжение горючих составных частей газовой смеси можно осуществить при помощи пропускания газа через нагреваем, платиновый капилляр Дреш-мидта. Газ из пипетки В (фигура 10) в присутствии необходимого количества воздуха или кислорода, заполняющего бюретку d, прогоняется через платиновый капилляр аb, нагреваемый газовой горелкой. При этом все горючие составные части газовой смеси сгорают. Возможность а предотвращена тем, что в припаянных к платиновому капилляру медных
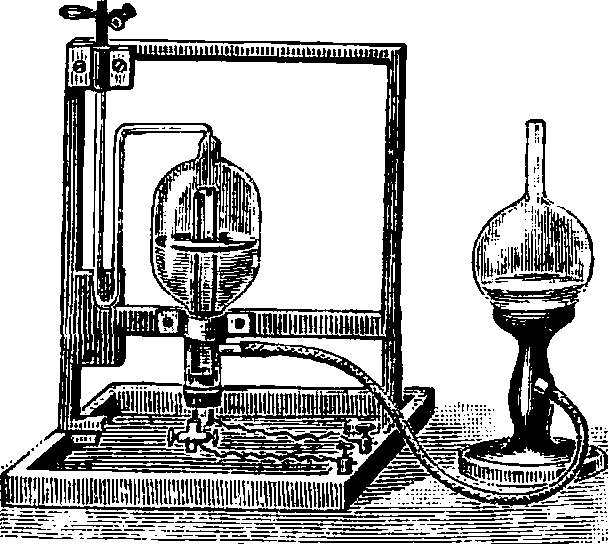
Фиг.
9. Сожигательная пипетка Кокильона. трубках а и b находятся отрезки платиновой проволоки, задерживающей распространение а в пипетку и бюретку. Окисление таким образом происходит медленно и без.а.
Весьма точная и быстрая методика А. г. основана на использовании для аналитич. целей физич. констант различных газов и их смесей. Зная константы тех или иных физич. свойств для отдельных газов и определив значение того же свойства для смеси этих газов, можно косвенным путем вычислить %-ное соотношение составных частей смеси газов. Для этого необходимо: 1) чтобы закон изменения данного физич. свойства смеси газов находился в простой и хорошо изученной зависимости от того же
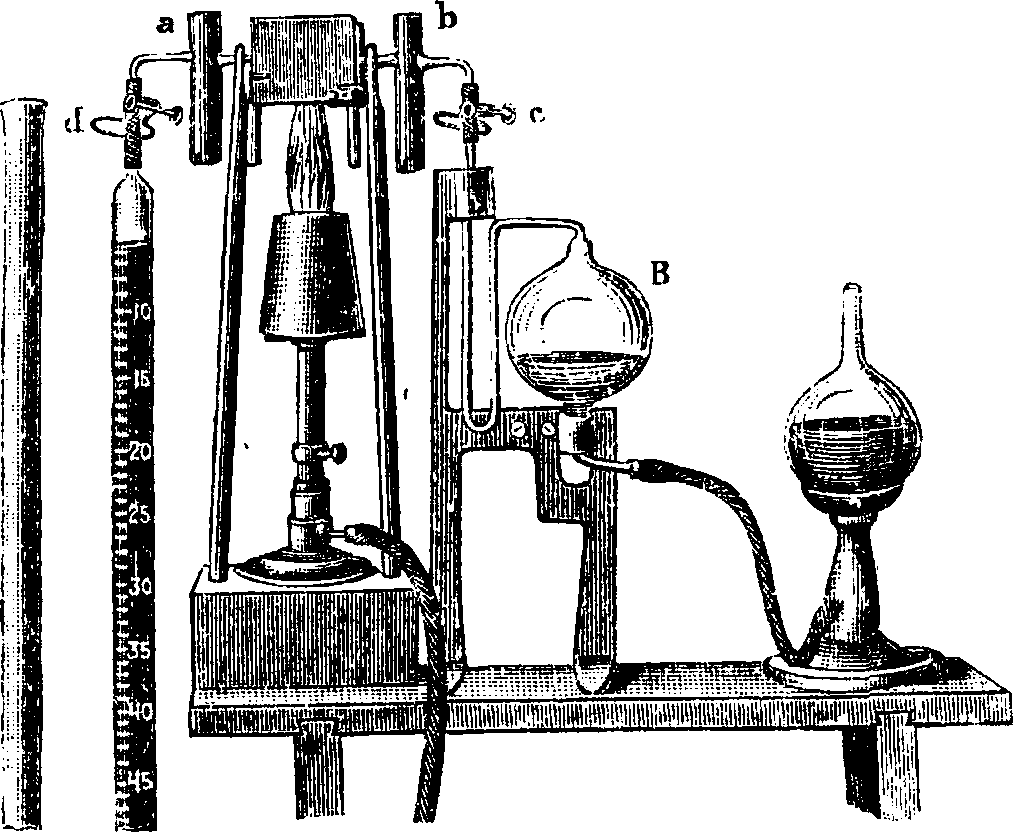
Фигура 10. Платиновый капилляр Дрешмидта-Виклера. физич. свойства отдельных ингредиентов этой смеси и 2)чтобы изменение (dA) данного свойства смеси в зависимости от изменения содержания в этой смеси определяемого ингредиента (наир, при увеличении концентрации этого ингредиента от С до C+dC) давало достаточный эффект и могло служить чувствительной количественной реакцией, сравнительно с обычными количественными аналитич. определениями.
В качестве примера приведем метод определения содержания углекислоты в газовой смеси на основании изменения ее теплопроводности в зависимости от содержания СО2. Нагревая в замкнутой камере метал-лич. проволоку при помощи электрич. тока, мы по величине сопротивления проволоки, нагретой в б. или м. степени в зависимости от теплопроводности наполняющей камеру газовой смеси, можем точно вычислить %-ное содержание СОг в смеси, имея предварительно цифровые данные для опытов с газами определенного состава и с определенным содержанием СО 2. (Прибор для испытания топочных газов фирмы Сименс и Гальске в Берлине. В виду того, что в этом приборе теплопроводность газов, а следовательно и содержание С02, определяется чисто электрич. путем, он имеет много преимуществ перед другими приборами — не требует затрат на химич. реактивы, отсчет м. б. производим через проволочную проводку вдали от самой топки, в которой уста-новлеп анализирующий прибор). Этот метод применяется также в физиологии, например для определения содержания С02 в выдыхаемом из легких воздухе.
Равным образом можно воспользоваться для количественных аналитич. определений при исследовании газовой смеси показателем преломления отдельных газов. На этом принципе основан метод «интерферометрии». Два параллельных пучка света от одного и того же источника пропускаются через две трубки, из которых одна наполнена испытуемой смесью газов, а другая—газом заранее известного состава; затем эти пучки сводятся под очень острым углом в одно место; в этом месте образуются, благодаря разным показателям преломления газов в обеих трубках, интерференционные полосы. Изменяя давление газа в одной из трубок (с газовой смесью заранее известного состава), можно компенсировать смещение интерференционных полос. Того же результата можно достигнуть при помощи зеркальца также и прямым смещением направления одного из сходящихся пучков. Это смещение м. б. измерено в предварительно градуированном приборе; на основании этих данных можем сделать заключение о показателях преломления обеих газовых смесей, которые, в свою очередь, дают возможность вычислить %-ный состав испытуемой газовой смеси (при помощи интерферометра Габера и Лёве).
Иногда количественный газовый анализ производится по дифференциальному методу, например анализ крови по методу Бар-крофта. Из двух совершенно одинаковых замкнутых сосудиков, соединенных между собой капиллярной трубкой, в один наливается определенный объём крови, а в другой — такой же объём раствора углекислой соды. Сосудики устроены т. о., что в оба м. б. одновременно введено равное количество к-ты. На середине капиллярной трубки имеется подвижная капелька ртути или какой-либо окрашенной жидкости. При действии кислоты на кровь и на соду из обеих трубок выделяется СО2, так что с обеих сторон на капельку в капилляре направлено газовое давление. По отсчету того места в капилляре, на к-ром остановится капелька, можно вычислить давление, а следовательно, и количество выделившегося углекислого газа из крови и из соды. Т. о. можно микрохимически произвести довольно точно газовый анализ С02 в крови.
Для постоянного контролирования полноты сгорания топлива в фабрично-заводских топках сконструирован целый ряд саморегистрирующих аппаратов, отмечающих в виде кривой содержание С02 в отходящих газах. Конструкция одного из таких приборов (Адос) показана на фигуре 11. Бля годаря тяге в трубе приводится в движение колокол, к-рый через каждые 3—5 мин. автоматически набирает в бюретку Л определенный объём отходящих газов и перекачивает их через раствор щелочи в сосуде А. СО г поглощается щелочью, а остаток газов попадает в сосуд В, замкнут, водяным колоколом К. Двшкеиие колокола передается рычагу Н, к-рый, в свою очередь, передает это движение еамопишущ. острию пера J, вычерчивающему кривую на бумаге вращающегося барабана. Сосуд N, соединенный с бюреткой I) длинной каучуковой трубкой О, непрерывно поднимается
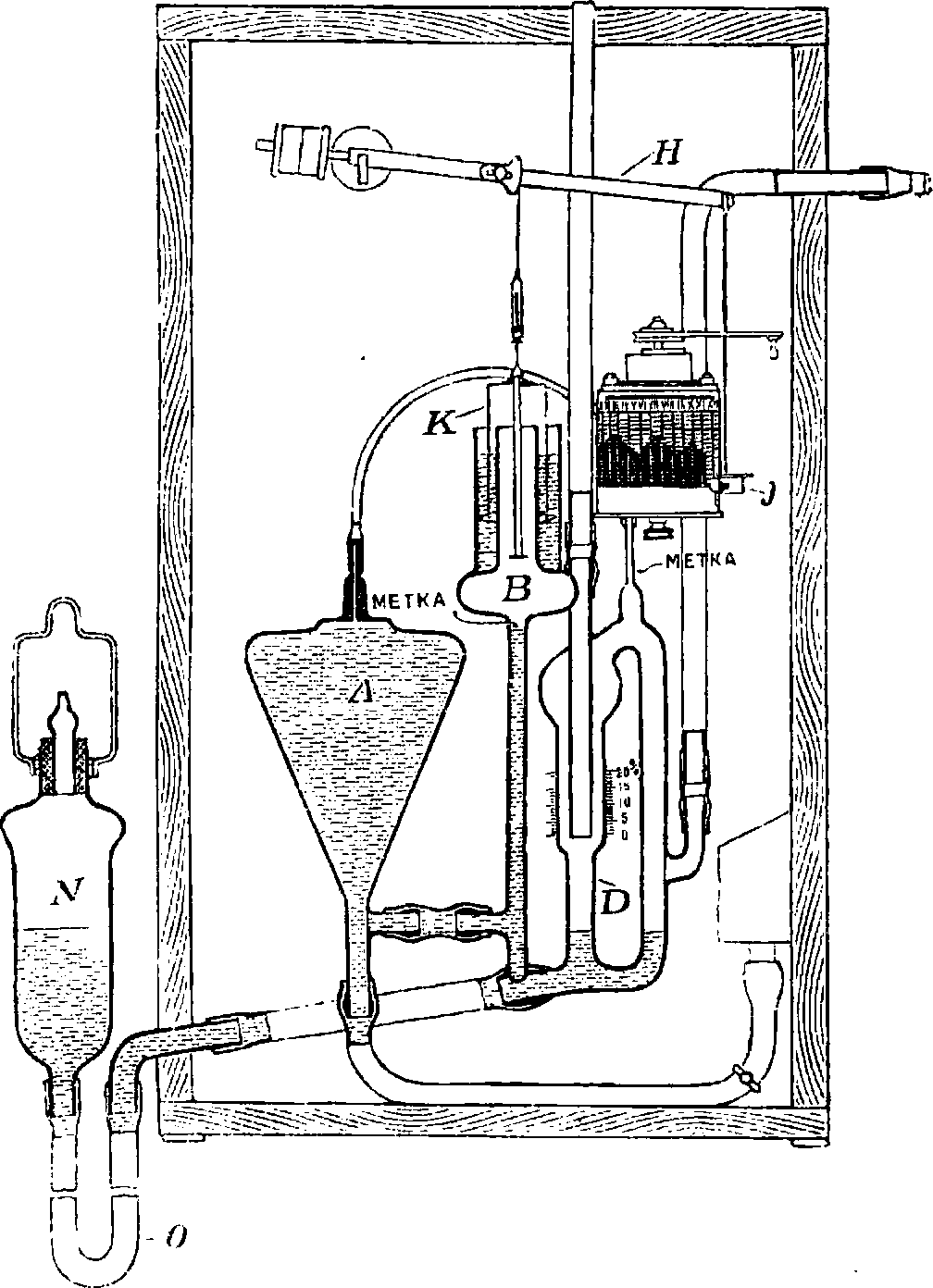
Фпг. i 1. Схема устаиомм саморегистрирующего газоанализатора Адос. и опускается благодаря действию газового насоса. Если в сосуде А щелочь заменить палочками фосфора, то тот лее прибор Адос может быть применен для определения кислорода в отходящих газах. Общий вид аппарата Адос изображен на фигуре 12.
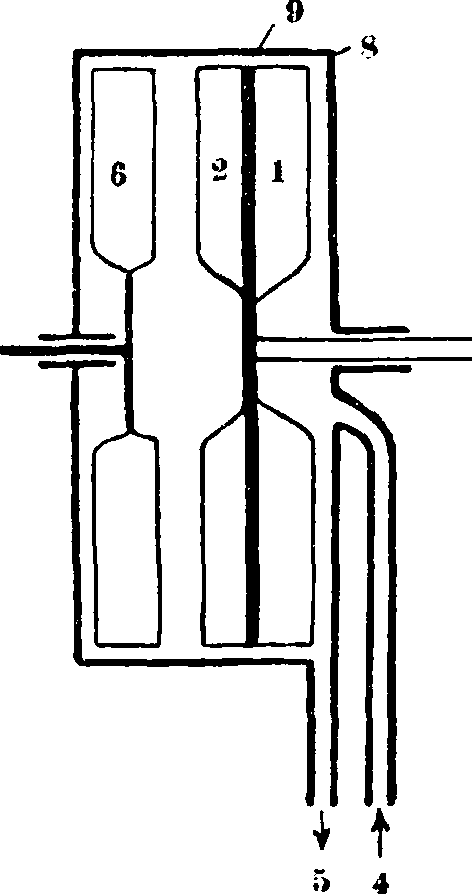
В других приборах содержание С02 устанавливается по уд. весу отходящих газов, легко обнаруживаемому при помощи «газовых весов» Люкса или же «эконометра» Арндта. В СССР акц. об-во «Тепло и сила» выпустило в продажу автоматический саморегистрирующий газоанализатор Раиа-рекс. Действие этого прибора понятно из схемы фигура 12.
Лопасти вентилятора, посаженного на оси 3 и приводимого в движение электромотором постоянной силы, засасывают в камеру 8 дымов [.к: газы через трубу 4. Затем газы через щель 9 попадают в измерительную часть камеры. Здесь, благодаря отбрасывающему действию лопастей 2, газы устремляются на лопасти вертушки 6 и приводят т. о. в движение ось 7, после чего через трубку 5 газы выходят наружу. Скорость вращения оси 7 при определенной силе мотора, приводящего в движение ось 3. зависит от уд. в газов. При этом, благодаря значительной скорости вращения оси, вс· динамические явления, пропорциональные, как известно из аэродинамики, квадрату этой скорости, приобретают весьма значительные выражения. При движущей силе мотора в 25 W момент вращения вертушки б приобретает благодаря такой мультипликации следующие значения:
350 гхсм для чистого воздуха,
365 » » воздуха с 10% СО.,
380 » » » » ‘2 0 % С О,.
Прибор Ранарекс (фигура 14), построенный на изложенном принципе, калиброван так, что он непосредственно показывает %-нос содержание С02. Кроме того, он снабжен автоматически регистрирующим приспособлением, облегчающим производство контроля топки.
То же акц. об-во «Тепло и сила» изготовляет автоматический газоанализатор системы Сименс и Гальске, действие которого основано на неодинаковой теплопроводности различных газов. «Если пропускать ток через два одинаковых провода, помещенных в разные газы, то вследствие различной теплопроводности этих газов один провод окажется более, а другой менее нагретым. Т. к. благодаря этому сопротивление первого будет больше сопротивления второго, то. соединив оба провода через мостик Уитстона, можно легко определить эту разность сопротивлений помощью гальванометра. Приемник газоанализатора Сименс-Гальске сконструирован соответственно вышесказанному. Два платиновых провода, представляющих собою две ветви мостика Уитстона, помещены: один—в струю воздуха, а другой— дымового газа. Т. к. теплопроводность

Фигура 13. Схематич. разрез через камеру прибора Ранарекс. воздуха почти вдвое больше теплопроводности СО 2, а остальные составные части дымового газа по своей теплопроводности очень близки к воздуху, то с достаточной степенью точности можно принять, что разность сопротивлений, полученная в ветвях мостика Уит-з стона,пропорциональ-з на содержанию С02 в газе. При соответствующей градуировке гальванометра получим указание %-ного содержания С02 в газе. Определение содержания СО +Н2 в дымовых газах основано на сходном принципе: два платино вых провода, представляющих ветви мостика Уитстона, помещены: один — в воздушную струю, а другой— в газовую струю, причем через них пропускается электрический ток, достаточный для такого нагревания провода, чтобы СО + + Н2, находящиеся в дымовых газах, воспламенились и сгорели в С02+Н20. При этом t° провода в соответствующей ветви мостика сильно повысится, и получится разность сопротивления, к-рую учитывают гальванометром, граду и р ов а н и ым в % содержания СО + Н2. Анализаторы Сименса снабжаются самопишущим электро магнитным прибором, соединенным проводами с ветвями обоих приемников анализатора и записывающим в виде диаграммной кривой все изменения сопротивлений в ветвях обоих мостиков Уитстона. Запись прибора производится кажд.
37 ск., точность его показаний равна ± У2%· Приборы Сименс и Гальске следует применять в тех случаях, когда желают знать не только содержание С02 в дымовых газах, но и СО-рН2, и когда регистрацию показаний желают централизовать» (смотрите проспект акц. об-ва «Тепло и сила» № 1, 1926 г.).
Из других приборов, сконструированных для быстрого и непрерывного анализа отходящих топочных газов и автоматического контроля топок, можно указать на следую
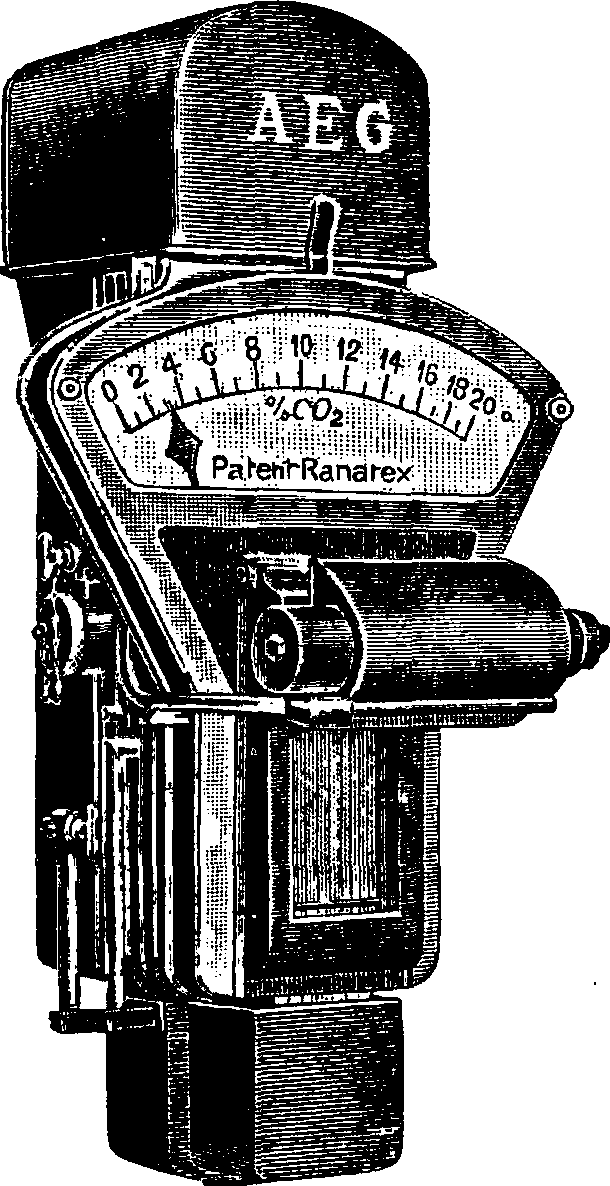
Фигура 14. Газоанализатор Ранарекс. щие: дымовой анализатор Крель-Шульце (G. A. Schultze, Berlin — Scharlottenburg); автоматический анализатор Адос (смотрите выше) фирмы Ados, G. ш. b. Н., Aachen: аппарат для контроля топок Апи (Aci), Gesell. fur Kohlenersparniss, Koln; аппарат Эккарда (J. C. Ekkard, Stuttgart—Cannstadt); монодуплекс—аппарат для одновременного определения С02 и СО (Gebr. Maybach, A. G., Hamburg). См. Отходящие газы.
Лит.: Францен Г., Газовый анализ, М.—П., 1923 (методика газового Анализа; приборы описаны весьма подробно, даются указания относительно источников ошибок; описания новых приборов, имеющих технич. значение, не приведено); Bunsen R., Gasometrische Methoden, Braunschweig, 1877; Berth ё 1 о t M., Trait6 pratique de 1’analyse des gaz, P., 1906; Zsigmondy und J a n d e r, Kurzer Leit-faden d. teclinischen Gasanalyse, Braunschweig, 1920; Winkler Cl., Anleitung z. ehem. Untersuchung d. Industriegase, Freiburg, 1877; Winkler Cl. und Вгипск, Lehrbuch der technischen Gasanalyse, Lpz., 1919; Hempel W., Gasanalytische Methoden, Braunschweig, 1900; Travers M., Experimentale Untersuchung von Gasen, Braunschweig, 1905; Liti n s k y, L., Messung grosser Gasmengen, Lpz., 1922; Hempel W., Gasanalyse, Handworterbuch der Naturwissenschaften, B. 2, 1912. Б. Беркенгейи.