 > Техника, страница 55 > Красящие вещества
> Техника, страница 55 > Красящие вещества
Красящие вещества
Красящие вещества, красители, органические соединения, обладающие способностью сообщать тот или иной цвет волокнистым материалам. В процессах крашения (смотрите) находят применение как естественные К. в., добываемые из животных и растений, так равно и синтетические, являющиеся продуктами промышленного органического синтеза.
Красящие вещества естественные.
Естественные К. в содержатся в растительных и животных организмах либо в виде готовых красителей, либо в виде бесцветных, легко переходящих в краситель соединений, либо в виде продуктов сочетания тех и других с углеводами, дубильными кислотами и другими веществами. Естественные К. в были известны еще в глубокой древности; их применение и значение в мировом хозяйстве было очень велико вплоть до конца 19 в., когда они начали вытесняться синтетическими К. в В наст, время лишь небольшое число естественных красителей сохранило свое промышленное значение и способно конкурировать с синтетич. продуктами.
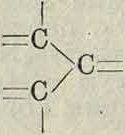
Классификация К. в Принципиальной разницы между К. в растительного и животного происхождения нет: например хлорофилл (К. в растений) и гемоглобин (К. в крови животных организмов) являются производными одного и того нее сложного тела— этиопорфирина. Точно так же пурпур древ них (продукт животного происхождения) есть дибромпроизводное индиго—красителя растительного происхождения. Иногда бывает даже трудно установить точное происхождение К. в.; так например, эйксантиновая кислота, добываемая из мочи травоядных, является продуктом соединения эйксантона (из дерева манго) и глюкуроновой кислоты. В силу этого основывать деление естественных К. в по их происхождению не представляется целесообразным. Попытки классифицировать их по морфологическим признакам также не достигают цели, так как К. в встречаются во всех частях растений, причем в одних и тех же частях растений различных видов м. б. весьма различные красители и, наоборот, весьма родственные К. в часто находятся в морфологически отдаленных частях растений. Естественные К. в бывают различных цветов, среди которых преобладают оттенки желтого и красного. Большинство из них обладает способностью давать лаки с металлич. протравами и лишь один краситель (куркумин) обладает субстантивными свойствами. Среди естественных К. в имеются представители различных карбоциклич. и гетероциклических соединений. Несмотря на широкое разнообразие их все эти формы можно подвести под нек-рые закономерности, связанные вероятно с самим генезисом К. в организме. Основываясь на химич. составе, можно выделить прежде всего большую группу естественных К. в., содержащих в основном скелете молекулы только три органогена: углерод, водород и кислород; другая, менее обширная, группа К. в характеризуется содержанием азота. Безазотистые вещества в большинстве представляют собой различные продукты замещения винилфе-нилкетона, то есть производные ацетофенона, в которых алкильный углерод двукратно связан с замещенной метиленовой группой, что можно представить следующей структурной формулой
ζ У~ СО—CH=CH-R,
где R—любой углеводородный остаток. Т. о. эти красители м. б. отнесены к п о л и м е-тиновым и в частности к метин-ацетофенонным красителям (в связи с последними работами Кенига это строение получает особый интерес). В м е-тинацетофенонных красителях можно отметить 2 подгруппы, значительно отличающиеся друг от друга. Первую из них можно назвать хновой подгруппой, т. к. все принадлежащие к ней К. в могут быть получены из оксихнов (смотрите ниже). Всю хновую подгруппу разбивают на 5 отделов: собственно хновые красители и 4 производных из них цикла: флаво-новые, флавилиевые, кетокумароновые и ка-техиновые К. Вторая подгруппа метинацето-фенонных красителей отличается наличием _ в ней бензофенонной группировки. К этой подгруппе относятся также производные ксантона и антрахинона; к метин-ацетофенонным красителям можно отнести также инафтохинонные красители. Полиметиновые производные содержат ряд конъюгированных двои-
ных связей, которые соединяют свободные или замещенные метановые остатки типа R-(—СН : СН—)n-R- К ним следует отнести куркумин,а также производные кроцетина— красящего вещества шафрана—и производные группы каротина. К азотсодержащим К. в относятся хинолиновые производные (берберин), генетически близкие к хновым красителям, пирроловые (хлорофилл, гемоглобин) и индолов ые (индиго).
В дальнейшем естественные К. в будут рассматриваться согласно следующей классификации.
I. Безазотистые соединения.
А. Метинацетофенонные красители.
1. Хновые красители:
а) собственно хновые красители,
б) флавоновые красители,
в) флавилиевые красители,
г) кетокумароновые красители,
д) катехиновые красители.
2. Бензофенонные красители:
а) оксибензофенонные красители,
б) ксантоновые красители,
в) антрахинопные красители.
3. Нафтохинонные красители.
Б. Полиметиновые красители:
а) куркумин,
б) группа кроцетина,
в) группа каротина.
II. Азотистые соединения.
A. Хинолиновые красители,
Б. Пирроловые красители,
B. Индоловые красители.
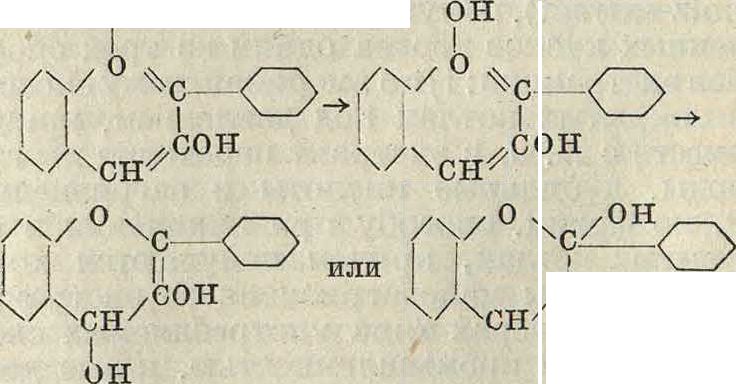
I. Безазотистые соединения. А. Метинацетофенонные красители. 1)Х ал-коновые красители являются по-лиоксипроизводными хна (бензилидена-цетофенона), строения
<^>-со-сн=сн-<^>
Хнами С. Костанецкий назвал полученные им при синтезе флавоновых красителей продукты конденсации ароматических альдегидов с ацетофеноном
(1 /СНЗ+ /О^СЗч /СН=СН-И ацетофенон бензальдегид хн
В виду того что присутствие как альдегидов, так и ацетофенона в растительных организмах можно считать доказанным, можно допустить и образование различных производных хна в самом растительном организме, тем более что некоторые из этих производных выделены и представляют также красители (смотрите ниже). Хновые К. в за редкими исключениями не имеют прак-тич. применения и представляют главн. обр. теоретический интерес как генетически связанные с большинством естественных растительных красителей. Чаще всего они являются спутниками флавоновых и подобных им красителей в растительных организмах, где содержатся в виде глюкозидов. Многие из них, как нарингенин (триоксихн), гесперетин (метиловый эфир пентаоксихал-кона), флоретин (тетраоксидигидрохн) и бутеин (тетраоксихн), выделены в чистом виде из растений и идентифицированы с полученными синтетически продуктами конденсации соответствующих оксипроиз-водных ацетофенона и бензальдегида. Наибольшее значение имеет бутеин, до сих пор применяемый для окраски тканей жителями Индии. Бутеин встречается в виде глюкозида в цветах дерева Butea frondosa, растущего в С. Индии и Бирме вплоть до подножия Гималаев. Строение бутеина (III) было подтверждено его синтезом из резаце-тофенона (I) с пирокатехиновым альдегидом (И) по ур-ию:
но
Ч,
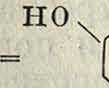
| он | Л/0Н |
| 1 + | /1 “ |
| ЧС0-СН3 о^сн | /ч^чон |
| I. | и. |
| )/0Н с | у он
1 +11.0 |
| 4 со— сн^си/^ | хон |
III.
При действии разбавленных к-т на бутеин он переходит в бесцветное соединение
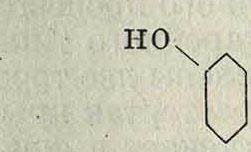
,он
u
?н—О
4 со сна
чон являющееся триоксифлавононом и называемое бутином, Последний всегда сопутствует бутеину, выделенному из растения, причем до сих пор неизвестно, содержится ли он в самом растении или получается из бутеина в процессе выделения последнего. В то время как бутеин способен окрашивать ткани в непрочный желтый цвет, бутан этим свойством не обладает; зато протравленную шерсть как бутеин, так и бутан окрашивают вполне одинаково, откуда можно заключить, что при действии протрав бутин переходит обратно в бутеин. Оба они по протравленной шерсти дают следующие оттенки: по Сг-протраве—кирпичнокрасный, по Fe-протраве—коричнево-оливковый, по А1-протраве—коричнево-оранжевый, по Sn-протраве—желтый. Легкость перехода бутеина в бутин и обратно служит ярким примером генетич. связи между хал-коновыми и флавоновыми К. в., так как последние легко получаются синтетически из флавононов.
Флавоновые красители, являющиеся полиоксипроизводными флавона (α-фенил-у-фенопирона) и флавонола,
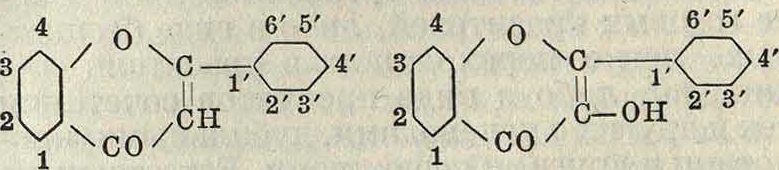
флавон флавонол не потеряли своего практич. значения и в наше время. Для рационального наименования этих красителей углеродные атомы в молекуле флавона и флавонола нумеруют и перед рациональным названием красителя указывают номера занимаемых окси-группами мест. В растительных организмах флавоновые красители содержатся преимущественно в виде глюкозидов и могут быть выделены путем экстрагирования последних из растения и их расщепления. Некоторые флавоновые красители представляют собой не оксипроизводные флавона и флавонола, но их метиловые эфиры. Ниже приведены наиболее известные представители флавоновых красителей. Строение почти всех этих красящих веществ можно считать установленным работами С. Костанецкого и его школы. Большинство из них было также получено синтетически.
Флавоновые красители Эмпирическое _
Рациональное название
1, 3-диоксифлавон 3, 3, 4-триоксифлавон 1, з, 3, 4-тетраоксифлавон i, 3, 2, 4-тетраоксифлавон », 3, 4-триоксифлавонол 1, 3-диоксифлавонол 1, 3, 4-триоксифлавонол 1, з, 2, 4-тетраоксифлавонол 1, з, 3, 4-тетраоксифлавонол 1, 3, 3, 4, 5-пентаоксифлавонол Монометиловый эфир кемпферола » » кверцетина название Хризин.
Аливенин.
Лутеолин.
Лотофлавин Физетин.
Галангин.
Кемпферол Морин.
Кверцетин.
Мирицетин Кемпферид Рамнетип.
Изорамнетин Рамназин·. Диметиловый » т>
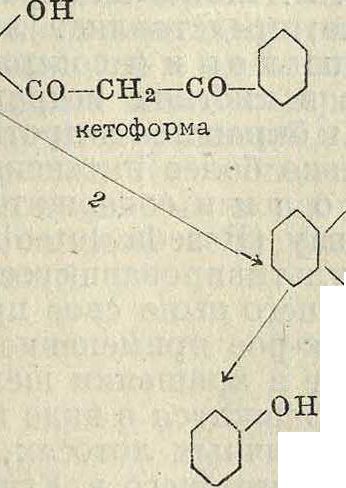
Химическое строение флавоновых и флаво-ноловых красителей было доказано как анализом продуктов распада, так и синтезом. Для анализа наиболее удобным оказался метод щелочного расщепления красителей, при котором в первую очередь следует допустить распад пиронового ядра с присоединением воды. Полученный продукт в кетотаутомер-ной форме представляет собой /3-дикетон, который далее расщепляется в двух направлениях, по обе стороны от центральной метиленовой группы. Полученные при этом продукты способны давать дальнейшие продукты распада с выделением уксусной кислоты и углекислоты. Для флавона процесс может быть изображен приведенной ниже схемой. При распаде в направлении 1 получаются фенол, ацетофенон и СОг; в направлении же fi—фенол, уксусная к-та и бензойная к-та. Для различных производных флавона получаются соответственные оксипроизводные фенола, бензойной кислоты и ацетофенона. По расположению в них оксигрупп можно судить о положении последних и в исходном красителе. Следует также отметить, что все красители хновой подгруппы метин-ацетофенонных красителей дают при щелочном распаде аналогичные продукты; последнее служит лишним доказательством их
-О
водные, а их метиловые эфиры, и лишь по завершении всего синтеза удаляют метиловые группы действием HJ. Оксихн при действии разбавленных кислот способен к замыканию шестичленного кольца с образованием дигидрофлавона, т. н. флавонона. При введении в последний этиленовой связи (что достигается бромированием и последующим отщеплением НВг гольным КОН) получается непосредственно флавон. При окислении же флавонона в соответствующий кетон (действием амилнитрита и омылением полученного оксима) получается флавонол. При несколько иных условиях оксихн способен к замыканию не шестичленного, а пятичленного кольца, образуя фенил к е-токумаро н. Единственным существенным условием является наличие в хне окси-группы в орто-положении к карбонильной, а не к виниленовой группе. Все вышеизложенные превращения м. б. для простейшего случая изображены в следующих схемах: он Λ ЮН
со—сн—сн-Д~
оксихн 4—
+ /I
ЮО-СНз осш о-оксиацетофенон бензальдегид
О
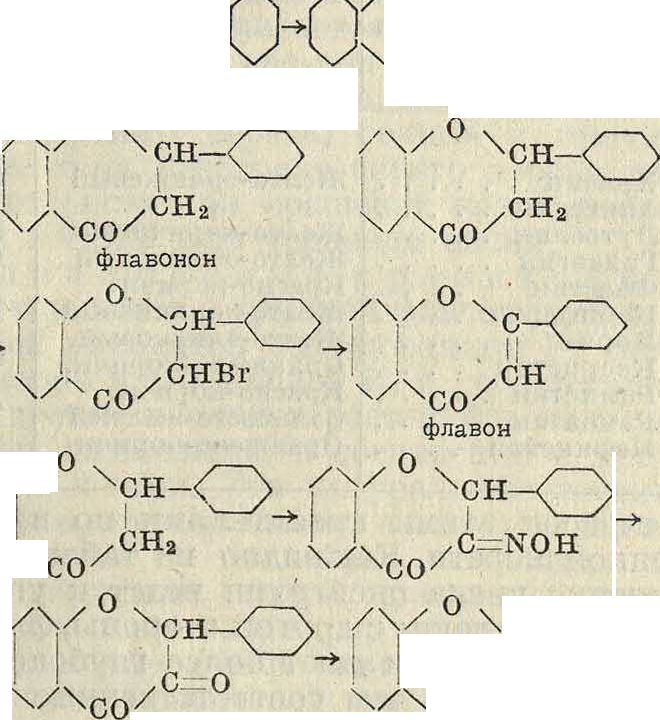
ir€>
,С—ОН СОХ флавонол
Если вместо о-оксиацетофенона и бензаль-дегида в подобном синтезе для образования хна взяты их полиоксипроизводные, то получаются соответственные оксипроизвод-
СН
+ Н20 ·
| ОН - | Vfl |
| СО—СН- СОн · | |
| энольная форма |
ОН
^СООН СН3—со он
+ С0г
он
СО-СНз ноос7
родства. Синтез флавоновых и флавоноловых красителей подтвердил выводы анализа их по продуктам распада. Из целого ряда синтезов наибольший интерес представляет следующий синтез, подробно разработанный С. Костанецким и имеющий исходным продуктом соответствующий лолиоксихн. Для удобства работы берут не оксипроиз-
т. э. ш. XI.
+СН3СООН
ные флавона и флавонола, то есть флавоновые красители с вполне определенным положением оксигрупп. Приведенная выше реакция для получения флавоноловых производных еще более упрощается, если оксипроизводные бензальдегида заменить соответственными оксипроизводными эфира бензойной к-ты. При этом непосредственно по-
13
лучается флавоноловый краситель. Все фла-воновые и флавоноловые красители способны за счет своих оксигрупп давать ацетильные и алкильные производные, чем пользуются для количественного определения оксигрупп. Лишь оксигруппа в орто-поло-жении к карбонильной группе обладает способностью только ацсгилироваться, но не алкилироваться. Все флавоновые красители способны к галохромии (смотрите) и дают соединения как с кислотами, так и с их солями. В силу наличия двух гидроксильных или гидроксильной и карбонильной групп, стоящих в орто-положении, эти К. в могут давать лаки с многовалентными металлами и находят поэтому применение в химической технологии волокнистых веществ. Наиболее важными К. в этой группы являются мо-рин и кверцетин. В табл. 1 приведены цвета с дубильными веществами в физетовом дереве (Rhus cotinus), кустарнике, произрастающем на побережье Средиземного моря. Кроме того физетин сопутствует дубителям в квебраховом дереве и содержится в кве-браховом экстракте, находит нек-рое применение в крашении кожи и шелка. Кем-п ф е р о л содержится в виде мономети-лового эфира кемпферида в корне галанги и вместе с кверцетином в виде глюкозида дирамнозида-кемпфэритрина, в живокости (Delphinium consolida), растущей в диком виде в Европе. Морин содержится либо в свободном виде либо в виде кальциевой соли в желтом дереве (Chlorophora tincto-ria или Maclura aurantiaca) в смеси с маклу-рином—пентаоксибензофеноном (смотрите ниже). Применяется главн. обр. в виде экстракта, обычно в смеси с другими красителями, и
Таблица 1 .—О краски флавоновы ми красителями по протравам.
| Название красителя | П р о т | р а в а | ||
| Сг | Ре | А1 | Sn | |
| Хризин.
Анигении. Лутеолин. Галантин. Физетин. Кемпферол. Морин. Кверцетин. Рамнетин. Рамназин. Мирицетин. |
Желто-оранжевый
» Желто-коричневый Желто-оливковый Красно-коричн. Желто-коричневый Желто-оливковый Оранжево-коричы. Красно-коричн. Золотисто-желтый Ораншево-коричн. |
Светлошоколадный
» Коричнево-оливк. Оливковый Темнооливковый Коричнево-оливк. » Темнооливковый » Коричнево-оливк. Темнооливковый |
Светлошелтый
» Желтый Желто-оранжевый Оранжевый Желтый » Коричнево-оранж. » Желто-оранжевый Коричнево-оранж. |
Светложелтый
» Оранжево-красный •Лимонно-желтый » » Оранжевый » Лимонно-желтый Оранжевый |
выкра.сок этими красителями по протравленной шерсти. Как видно из таблицы, увеличение числа оксигрупп ведет к углублению цвета лака; с другой стороны, флавоноловые красители дают более глубоко окрашенные лаки, чем соответственные флавоновые красители, что объясняется вероятно наличием в их пироновом кольце лишней оксигруппы, способной проявлять кето-энольную таутомерию.
Хризи н—простейший краситель этого ряда содержится в почках различных видов Populus, гл. обр. Р. monolifera, растущего в Сев. Америке; представляет лишь теоретич. интерес. Апигенин содержится в виде глюкозида в листьях петрушки (Apium petroselinum) и окрашивает протравленные ткани несколько более интенсивно, чем хризин. Лутеолин содержится в листьях цервы или вау (Reseda luteola)— растения, прежде культивировавшегося в Ср. Европе и потерявшего ныне свое практическое значение. Нек-рое применение лутеолин иногда находит в крашении шелка. Лотофлавин содержится в виде глюкозида лотузина в различных лотосах, например Lotus arabica, растущего в Египте. Интересно, что в этом глюкозиде кроме двух молекул глюкозы содержится также и одна молекула синильной к-ты, HCN. Галантин содержится в виде монометилового эфира в корневище галанги (rhizoma Ga-langae), растения Alpinia officinarum, сопутствуя кемпферолу. Физетин содержится в виде глюкозида фустина в соединении кроме синтетических красителей конкурирует с грушкой и кверцитроном (смотрите ниже). Кверцети н—один из наиболее распространенных естественных красителей, содержащийся в виде глюкозида (кверцитри-на) в кверцитроне—коре нек-рых пород дуба, гл. обр. Quercus tinctoria, произрастающего в С. Америке. В свободном виде находится в луковой шелухе. Кроме того кверцетин содержится в виде различных глюко-зидов его метиловых эфиров (рамнетина, изорамнетина и рамназина) в незрелых плодах различных пород крушины (грушки), например немецкой грушки, персидской грушки,авиньонской ягоды и других. Кверцитрон поступает в продажу в виде измельченной коры, грушка же—чаще в виде экстракта. Кверцитрон обладает большей красящей способностью, чем желтое дерево. Из метилированных производных кверцетина наибольшее применение имеет грушка. Мири-цетин содержится в некоторых видах сумаха (Rhus), где сопутствует дубильным веществам, и главным образом в растении Myrica nagi, растущем в Индии, где имеет только местное распространение; мирицетин интересен как единственный краситель этого ряда, дающий при щелочном распаде галловую кислоту.
Как видно из вышесказанного, наибольший практич. интерес представляют лишь морин и кверцетин с их метиловыми эфирами, красящие начала желтого дерева, кверцитрона и грушки, применяемые и в настоящее время в текстильной промышлек-
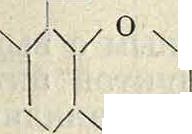
ности. К флавоновым красителям можно отнести и красящие начала красного и синего дерева—бразилин и гематоксилин, так как их получение из метилхнов связано с получением флавоновых красителей из хнов; лишь дальнейшая, вторичного порядка, реакция в силу наличия удобной конфигурации ведет к замыканию инденово-го кольца. По исследованиям В. Перкина, бразилин и гематоксилин, а равно и красители бразилеин и гематеин, являющиеся продуктами их окисления, имеют строение но. сн3
I
но. сн он сн2
/-
X_
I
он бразилин
ОН
! у с
СНаI /ОН
СН2
“X
ОН О
бразилеин
ОН
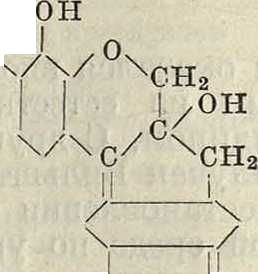
но
СН2
НО,
,ОН
/С
СН7 ХСН2
/“
_
ОН
гематоксилин
“
.
Г
ОН
ОН о гематеин
Как видно из этих формул, гематоксилин и гематеин отличаются от бразилина и бра-зилеина лишь одной лишней оксигруппой, и если последние являются производными метинрезацетофенона, то первые являются производивши галацетофенона. Б р а з и-л и н—красящее начало красильного красного дерева (Caesalpinia, сем. Leguminosae), растущего в Ост-Индии, Южной Америке и Африке; различные виды его, в зависимости от места их произрастания, дают сильно отличающиеся по качеству красильные препараты. Наилучшие сорта дает фернамбуко-вое дерево, растущее в Бразилии и на острове Ямайке. Несколько меньше содержание К. в сортах из Южной Америки и Ост-Индии. Низшие сорта дает мексиканское красное дерево. К. в содержится в дереве в виде легко разлагаемого глюкозида и применяется главным образом в виде экстракта (Rot-holz-extract), получаемого из сильно измельченных кусков дерева одним из трех способов экстракции: 1)по американскому способу в закрытых котлах под давлением, причем вместе с К. в экстракт переходят и углеводы, дубильные кислоты и загрязнения;
2) по франц. способу при кипячении в открытых котлах, причем получаются хорошие выходы малозагрязненного экстракта;
3) в диффузорах типа употребляемых свеклосахарной промышленностью, которые дают наиболее чистые экстракты, но рентабельны лишь при массовом производстве. Непрочность выкрасок к мылу, поту и т. и. послужила одной из главных причин вытеснения этого К. в синтетическ. красителями. Все же бразилин применяется для протравного крашения и печатания растительных волокон, для крашения протравленных жи вотных волокон и дает по хромовой протраве фиолетово-коричневые окраски, по железной—фиолетово-серые, по алюминиевой— синевато-красные и по оловянной—оранжево-красные. Гематоксили н—красящее начало синего или кампешевого дерева (Haematoxylon campechianum, сем. Caesal-piniaceae), растущего главным образом в Мексике, Гаити, Гондурасе, на Ямайке и Антильских островах. Лучшие сорта поставляет Мексика. Из дерева получается экстракт (Blauholzextract)—синий сандал, или кампеш. В продаже имеются и иные препараты синего дерева, из которых нужно отметить так называемым Indigoersatz, или Noir-reduit, получаемый при окислении гематоксилина хромовой к-той с последующим частичным восстановлением солями сернистой кислоты, в силу чего в нем содержится наравне с красящим началом и протрава. Экстракт синего дерева применяется в настоящее время для крашения и печатания растительных волокон и крашения животных волокон. Наиболее прочным считается хромово-медный лак, дающий при некоторой подцветке желтыми красителями (грушка, кверцитрон, экстракт желтого дерева) сочные и прочные черные тона. Экстракт синего дерева применяют также при крашении кожи, в частности в СССР при чернении овчин.
Флавилиевые красители. В тесном родстве с группой флавоновых красителей находятся исследованные Р. Виль-штеттером и его школой К. в., содержащиеся в цветах и плодах растений в виде различных глюкозидов и соединений с металлами и к-тами. Эти натуральные соединения Вилынтеттер назвал антоцианами. Выделенные из последних глюкозиды минеральнокислых солей красителей названы антоцианинами; самые же минеральнокислые (чаще всего солянокислые) соединения красителей, являющиеся красящим началом антоцианов, названы анто-цианидинами. Так например, окраска цветов василька обусловлена красителем цианидином, глюкозид к-рого, ц и а-н и н, находится в растении в смеси с калиевой солью и фиолетовой модификацией основания красителя. Сочетание этих форм придает васильку голубую окраску. Тот же цианин, но в ином сочетании в форме минеральных солей содержится в цветах розы и других растений, придавая им красные окраски. По исследованиям Вилынтеттера, антоцианины являются оксипроизводными оксониевой соли флавилия (фенилфенопи-рилия)
он з/у г! L
ЧСН
^сн
6 5
SO’
2 3
(углеродные атомы перенумерованы аналогично флавоновому скелету). Солянокислый флавилий, неизвестный в природе, был получен синтетически действием магний бром-фенила на кумарин в присутствии НС1 по следующему уравнению:
" со
I + BrMg·^^ + НС1 -
UxCH^ ^
сн
Cl
I
0
СН-
γο
^CH
+ MgO + HBr
с другой же стороны, он был получен при конденсации салицилового альдегида (I) с ацетофеноном (II) в присутствии НС1
/ОН
+ /с°-0 хсно сн3 4—/
II.
+ НС1 -
С1
юн
х/хсн^"
III.
со-^ I
сн
0 X,
+ HC1-
/,сн
Если принять во внимание, что промежуточным продуктом при этой реакции является оксихн приведенного строения (III) и что изомерный оксихн, в к-ром окси-группа находится в орто-положении не к виниленовой группе СН СН, а к карбонильной группе СО, дает при действии к-т фла-вонон,—то станет вполне ясной генетич. связь между флавоном и флавилиями, что и легло в основу принятой выше классификации. Флавоновые красители кроме того удалось непосредственно перевести во фла-вилиевые. При всем богатстве оттенков цветов и плодов удалось выделить из них лишь три основных красителя и показать, что только ими обусловлены все столь разнообразные окраски; изменения же оттенков зависят от формы, в которой краситель присутствует в растении, и иногда от примеси флавоновых красителей. Эти три антоциа-нидина названы пеларгонидином (I), цианидином (II) идельфини-д и н о м (III) и являются, соответственно, тетра-, пента- и гексаоксифлавилиями следующего строения:
С1
-О
CH
С1
I
сон
но /0 хс_
он юн и.
-О-он
Х|/ХСН^
он сон ноч
С1
/ОН
III.
I
О-0Н
Х|/ХСН^
он сон
чон
При щелочном распаде они дают: флороглю-
цин и первый—и-оксибензойную к-ту, второй—пирокатехиновую к-ту и третий—галловую к-ту, что дало возможность выяснить их строение и положение оксигрупп; окончательно же строение их было подтверждено синтезом. Так, пеларгонидин был получен, подобно первому синтезу флавилия, из три-метоксикумарина (I) и и-метоксибромбензо-ла (II), с последующим отщеплением метиловых групп, по ур-ию: сн3оч /. О
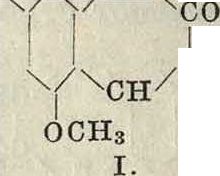
ноч
СОСНз
С1
I
- о
.+ Вг-
-ОСН3 +
II.
+ НС1-
ухсн^
он
οι
сон
ОН
он оказался вполне идентичным с выделенным из естественных продуктов антоциа-нидином. С другой стороны, цианидин был получен Вилынтеттером из кверцетина при восстановлении последнего магнием в кислой среде по ур-ию
/ОН
Н0 4 - - - -ОН
+ Mg + HCl-
| ч /0 с | |
| II - ii
1 λ /С-он γ хсох |
v_ |
| он | С! |
| но | Ь |
| MgO + j | CH^ |
/ОН
с---
I
с-он он он.
В последние годы были синтетически получены не только все антоцианидины, находимые в природе, но и ряд их изомеров, не найденных в растениях.
Антоцианидины представляют собой оксо-ниевые соли кислот, которые при действии разбавленных щелочей переходят через ги-потетич. флавилиевые основания в соответствующие псевдооснования согласно схеме
С1
.с- он
Последние способны давать соли с щелочными металлами, чем и объясняются индикаторные свойства этих К. в Не исключена и возможность того, что в силу наличия во флавилиях оксониевого кислорода в данном случае имеет место и резко выраженная галохромия, тем более что антоцианидины сами по себе не содержатся в цветах, а являются только составными частями анто-цианов. Получение антоцианидинов в чистом виде и их изучение представляли громадные трудности: для получения Юз чистого красителя приходилось подвергать обработке сотни кз цветочных лепестков. По методике, выработанной Вилыптеттером, осторожно высушенный исходный материал экстрагируется ом, содержащим до 2% НС1, с последующим выделением красителя эфиром и перекристаллизацией его из метилового а, содержащего НС1, или из ледяной уксусной кислоты; т. о. получается чистый глюкозид — антоцианин. Последний расщепляется на углевод и антоцианидин действием 20%-ной соляной к-ты; антоцианидин перекристаллизовывается из 2%-ной соляной к-ты. Все эти красители дают яркие, но непрочные окраски по шерсти и по таннированному хлопку (табл. 2). Будучи
Таблица 2.—Окраска антоцианидинами.
| Цвет, даваемый красителем | |||
| Краситель | шерсти | шерсти, протрави. оловянными солями | хлопку |
| Пеларгонидин | — | Пурпурово красный | Сине красный |
| Цианидин. | Розовый | Сине-фиоле товый | Фиолето вый |
| Дельфинидин | Фиолето вый | Фиолетово синий | Сине-фио летовый |
| Миртилидин. | — | » | Фиолето вый |
| Онидин. | — | » | * |
вполне безвредными, они находят применение гл. обр. для окраски пищевых продуктов (последние два красителя представляют собой эфиры природного дельфинидина— моно- и диметиловый).
Катехиновые красители. Ок-сихн способен к замыканию не только шестичленных, но и пятичленных пироновых колец. Частным случаем последнего является к а т е х и н, красящее начало катеху, кашу, гамбира, в которых ему сопутствуют в-различных соотношениях дубильные к-ты, кверцетин и углеводы. Катехин, по последним исследованиям Фрейденберга, имеет строение
но 0 /он I СН—СН(ОН)— <^Voh
UL.
у хсн2он генезис его может быть проведен от пента-оксихна
НОч /ч /ОН
СН -СН—С о—<У>—о н он или от вторичного а, соответствующего этому кетону. Краситель катеху содержится в соке растений Acacia mimosa, А. Catechu, A. Suma и поступает в продажу в

виде высушенного сока. В чистом виде катехин является бесцветным веществом, но, окисляясь, переходит в темноокрашенное соединение. Он применяется в крашении и печатании протравленных растительных волокон и главным образом в крашении шелка с одновременным отяжелением последнего.
2)Бензофенонные красите-л и. Простейшим представителем о к с и-бензофенонных красителей является маклурин (пентаоксибензофенон)
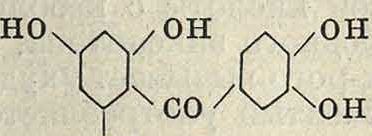
он содержится в желтом дереве Chlorophora tinctoria и Maclura aurantiaca, в свободном виде или в виде Са-соли, и сопутствует мо-рину. При щелочном распаде он образует флороглюцин и пирокатехиновую к-ту, чем и доказывается его строение; практич. применения не имеет.
К бензофенонным красителям следует отнести иксантоновые красители—производные ксантона, к-рый можно рассматривать как ангидроформу диокси-бензофенона с двумя оксигруппами в ортоположении к СО-группе в обоих ядрах оОо о-о-диоксибензофенон
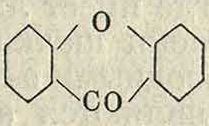
ксантон
Сюда относятся эйксантон (2, 6-диокси-ксантон) с эйксантиновой кислотой и генти-зин (монометиловый эфир гентизеина). Э й-ксантон был получен синтетически при действии 2, 4-диоксибензойной кислоты на гид-рохинонкарбоновую к-ту по ур-ию соон
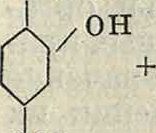
он но ч,
СООН7
/ч соон
i /ОН ноч
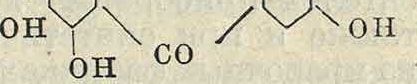
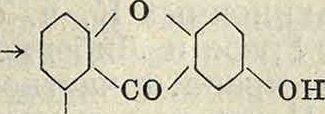
он и, с другой стороны, конденсацией 6-мет-окси-2-хлорбензойной кислоты с монометиловым эфиром гидрохинона по ур-ию
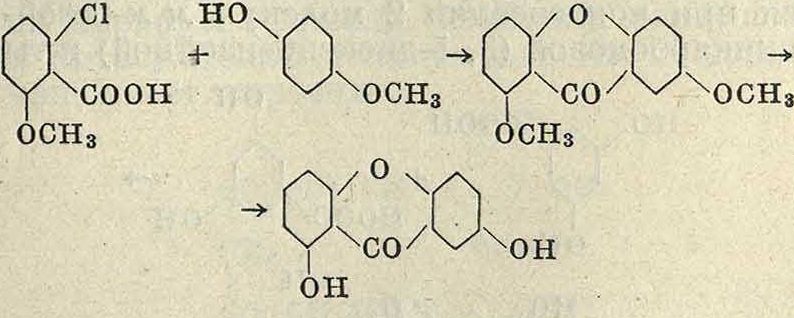
так что его строение можно считать вполне установленным. Гентизеину же свойственна одна лишняя оксигруппа, и он может быть получен аналогично. Эйксантон содержится в виде эйксантиновой кислоты, Ci9H18Ou (соединения эйксантона с глюкуроновой к-той,
СООН-(СНОН)4-С^° V в моче коров, пи-
тающихся листьями мангового дерева (Мап-gifera indica), растущего в Бенгалии. Пови-димому эйксантон или весьма близкие ему продукты, содержащиеся в листьях манго, связываются в животном организме с глю-куроновой кислотой и удаляются из организма в моче. При нагревании такой мочи из нее выделяется осадок, который поступает в продажу под названием Piuri, или индийский желтый. Лучшие сорта его содержат кальциевые и магниевые соли эйксантиновой кислоты с небольшим количеством свободного эйксантона, увеличение количества которого вызывает ухудшение К. в Индийский желтый употребляется главным образ, как очень ценная акварельная краска, но не применяется в текстильной промышленности, хотя и обладает способностью окрашивать протравленные ткани в желтый цвет. Производство его: 5—7,5 тонн в год. Гентизин, монометиловыйэфир 2, 6, 8-триоксиксантона, содержится в корне Gentiana lutea, способен давать лишь весьма слабые желтые оттенки по протравленным тканям и потому не находит технич. применения. Датисцети н—диметил овый эфир тетраоксиксантона—содержится в виде глюкозида датисцина в корнях и листьях JDatisca cannabina, растущего в Лагоре в Индии, где имеет лишь местное применение для окраски шелка в желтый цвет.
Производными о-карбоновой кислоты бензо-фенона являются антрахино иные к р а с и т е л и, т. к. сам антрахинон образуется выделением молекулы воды из этой к-ты, согласно схеме соон
/со
чсо/
Хсо бензофенон-о-карбоновая к-та антрахинон
Этот наиболее вероятный в растительн. организме путь образования антрахинонных красителей приобретает все большее значение также и при синтетическом получении их на красочных фабриках. Современная химия и технология антрахинонных К. в основываются на работах Гребе и Либермана над естественными К. в крапа, в частности над ализарином (смотрите). Некоторые оксиантрахи-нонные К. в получаются по методам, вполне соответствующим предполагаемому пути их природного синтеза. Так например, антрахри-зон (1,3,5,7-тетраоксиантрахинон) получается при конденсации 2 молекул ж,ж-резор-цинкарбоновой (3, 5-диоксибензоцной) к-ты он но
V
/СООН
он но. ноос
У
он
/С°х
он
[ со/^ ν·οη
он
Среди естественных антрахинонных К. в необходимо отметить К. в крапа (Rubia), К. в корней семейства Rheum и К. в., получаемые из насекомых Coccus. К. в крапа—корня марены (Rubia tinctorum), куль тивировавшейся прежде весьма широко в Средней Европе, Южн. России, на е, а в настоящ. время разводимой в Турции и Индии, представляют собой ализарин и его производные. Ализарин содержится в крапе в виде глюкозида—рубэритриновой кислоты; ему сопутствует следующий ряд метиловых эфиров, оксипроизводных и карбоновых
Рациональное название 1, 2-диоксиантрахинон
1- метоксп-2-оксиантрахи-нон
1, з-диоксиантрахинон
2- метокси-З-оксиантрахи-нон
1, З-диокси-4-метилантра-хиноп
1, 2, 4-триоксиантрахннон
1, з-диметокси-2-оксиан-трахинон
1, 2-диметокси-З-оксиан-трахинон
1, 3-диоксиантрахиыон-карбоновая к-та
1, 2, 4-триоксиаптрахинон-карбоновая к-та
Продажный крап представляет собой измельченный корень марены; до развития синтетической химической промышленности он имел громадное значение. В настоящее время синтетические антрахинонные К.в. почти целиком вытеснили естественные. Краповые препараты продолжают еще применяться лишь в кустарной промышленности. Из таких препаратов наиболее употребительный краплак, или гарансин, получаемый путем обработки крапа крепкой серной кислотой и промывания полученного осадка водой. При этом рубэритриновая кислота разрушается, а углеводы и другие примеси отмываются водой; полученный остаток, обогащенный ализарином, имеет красящую способность, которая в 4—6 раз выше, чем у крапа.
В близком родстве с краповыми красителями находятся К. в корня ревеня (Rheum) и сока алоэ (Aloe), имеющие лишь фармацевтическое применение в виду присущих им слабительных свойств. Все они содержатся в растениях преимущественно в виде глюко-зидов и представляют собой хризазиновые производные /J-метилантрахинона; например:
Хризофановая к-та. з-метил-l, 8-дионсиантра-хинон
Алоээмодин. З-океиметил-1, 8-диоксиан-
трахинон
Рейн .. 1, 8 - диоксиантрахинон-3-
карбоповая к-та
Франгулоэмодин. з-метил-1, 8, 6-триоксиан-трахинон
Кроме того в корнях растений сем. Rubi-асеае содержатся глюкозиды других поли-оксиантрахинонов, иногда применяемые для окраски косметических препаратов, например мориндон (триоксиметилантрахинон) в Morinda citrofolia и алканнин (диоксиметил-антрахинон) в Lawsonia alba.
Несколько особняком стоят К. в., получаемые из насекомых семейства Coccus. К ним относятся карминовая к-та, кермесо-вая к-та и лаккаиновая к-та. Исследования
АЬ A CAV А ААОAi. АХСЬ.
Эмпирическое название
Ализарин.1.
Метиловый эфир ализарина ..
Ксантопурпурин. Монометилов, эфир ги-стазарина.
Рубиадпн.
Пурпурин.
Диметилов, эфир антра-галлола..
Диметилов, эфир антра-галлола..
Ксантопурпуринкарбо-новая к-та.
Пурпуринкарбоновая кислота ..
Димрота показали, что они являются производными антрахпнона и имеют следующее строение (строение остатка С6Н1306 еще не выяснено):
сн3 он гЛ/С°ч[Л-СвН11о.5
но/у со/У-он
соон он карминовая к-та
| СН3 | ОН |
|
О о -с |
1 /СО-СНз |
| V4o | Y хОН |
| соон | он |
| кермесовая | к-та |
Вопрос о происхождении этих К. в еще не вполне решен. В виду родства растений, к-рыми питаются насекомые Coccus, с растениями рода алоэ можно допустить, что основной скелет К. в воспринимается насекомыми из растения и в животном организме он получает лишь окончательное завершение. Карминовая кислот а—красящее вещество кошенили, высушенных самок насекомых Coccus cacti, живущих на мексиканских кактусах. Из кошенили получается ряд препаратов, представляющих либо чистую карминовую кислоту либо ее лаки с А1 и Са; последние называются кармином (смотрите) и находят применение в качестве весьма ценной акварельной краски. Карминовая кислота в виду ее безвредности- широко применяется для окраски пищевых продуктов. Раньше она применялась и для получения -алых оттенков по протравленной солями •олова шерсти. Кермесовая кислот а— К. в кермеса, высушенных самок насекомых €occus ilicis, живущих в различных породах дуба, преимущественно в Персии; имеет то же применение, -что и карминовая к-та. Лаккаиновая кислота, С20Н14О10,— К. в лакдея (Lac-Dye), затвердевшего сока различных фикусов и мимоз, растущих в Индии и на о. Цейлоне. На этих растениях живут самки насекомых Coccus laccae, уколы которых вызывают выделение смолистого сока, окрашиваемого содержащимся в них К. в Смола, освобожденная от красителя (экстракцией), представляет собой шеллак <см.), остаток же (лакдей) содержит до 10% К. в Применение—то же, что и для карминовой кислоты.
3)Нафтохинонные красители имеют типичную метинацетофенонную группировку, замкнутую в хинонное кольцо. Среди естественных К. в имеются следующие представители этой группы: юглон, ла-пахол и. ломатиол
| ОН
А/СО. { у хсн |
/соч /СНз ( у хс-сн2-сн =с< |
| II | 11 СНз |
| IJv /СН ч/хсо7 | 1 L /С—он
х/чсох |
| юглон (нуцин) | лапахол |
| /ч | СОч /СНз ХС-СН-СН-С< |
| II 1ХСН3/СОН он сох
ломатиол |
Юглон, или нуцин (1-окси-а-нафтохинон), К. в скорлупы и зеленых частей лесного ореха, Juglans regia, представляет· большой теоретич. интерес как родоначальник хро-мотроповых азокрасителей, содержащих в своем составе хромотроповую к-ту (1, 8-ди-оксинафталин-3, 6-дисульфокислоту).
SOaH/χ/χ^ xS03H
переходящую при окислении (что имеет место при последующем хромировании этих красителей в текстильном деле) в юглоно-вую кислоту но о
М -
S03H/X-/j-j/XS03H
ό
Л а п а х о л (З-окси-2-амилен-а-нафтохи-нон) содержится в лапаховом дереве, семейства Bignoniaceae, и в других деревьях, растущих в Африке и Ю. Америке. Наличие в лапахоле амиленовой группы делает возможными различные перегруппировки в ней, ведущие к изомерам лапахола. К продуктам окисления последних относится ломатиол (оксиизолапахол). В близком родстве с приведенными выше К. в находится эллаговая кислота, получаемая конденсацией двух молекул галловой кислоты и имеющая вероятное строение /СО-О /ОН
но-О---О~он
но о со7
Она служит протравным красителем желтого цвета, получается синтетически окислением галловой кислоты и поступает в продажу под названием «ализаринового желтого». В растительных организмах естественная эллаговая кислота сопутствует различным дубильным веществам.
Б. Полиметиновые красители содержат ряд свободных или замещенных виниленовых групп (СН : СН), в силу чего их можно называть и поливиниленовы-ми красителями. Работы Кенига, Куна и Каррера показали связь между винилено-вым строением и окраской органических соединений. Простейшим представителем этой группы является к у р к у м и н—К. в корня куркумы (Curcuma tinctoria), растущей в Китае, Индии и на острове Яве. Курку-мин имеет строение осн3
со · I
сн2
СН : СН
-о он
ОСН3
СО · СН: СН-<^>-ОН
и м. б. получен конденсацией мономети-лового эфира пирокатехинового альдегида с ацетилацетоном, что генетически роднит куркумин и с хновыми К. в Курку мин является субстантивным К. в., что, по исследованиям Рупе и Порай-Кошица, вообще свойственно полиметиновым красителям.
Он получается экстрагированием измельченного корня ом и осаждением экстракта уксуснокислым свинцом. Выпавший осадок разлагается серной к-той и из осадка извлекается ом чистый куркумин. Кур-кумин в настоящее время применяется лишь для подкраски пищевых продуктов и как индикатор в аналитич. химии (смотрите Куркума).
К полиметиновым красителям относится также ряд естественных К. в., природа которых исследована лишь в недавнее время, как то: К. в шафрана, томатов, яичного желтка и хлоропластов высших растений. Многие из них, например каротин, содержат лишь углерод и водород, имея состав С4оН5в. Воль- штеттер выделил пек-рые из этих красителей, сопутствующих хлорофиллу в зеленых частях растепий (каротин, ксантофилл), и предположил в них наличие сложной системы циклов. Более поздние работы показали, что непредельность этих соединений очень высока и некоторые из них, как каротин, способны при каталитич. гидрировании присоединять до 22 атомов водорода, что противоречит допущению циклич. строения. Значительный интерес эти К. в приобрели благодаря последним исследованиям, роднящим их свойства е свойствами витаминов, в силу чего можно допустить их большое физиологии, значение в питании и жизни растений. Наиболее простыми представителями этих продуктов являются К. в шафрана (Crocus sativus L·.), представляющие смесь α-, β-и у-кроцетинов, CioHi402, выделенных в чистом видо Каррером и отличающихся друг от друга наличием карбоксильных групп. В шафране кропетины содержатся в виде глюкозидов (к р о ц и н) и м. б. разделены благодаря их различной растворимости, что обусловливается возрастанием числа карбоксильпых групп от а-до у-кроцетина. С кроцетинамп идентичен также и б и к с и н.
Более сложные полиметиновые красители—к аро-т и н о и д ы—были исследованы Любименко, Каррером и Кулином. Последний, применяя метод капиллярного анализа, который основан на различной растворимости каротиноидов в е, нашел в хло-ропластах высших растений ряд новых К. в., которые можно разделить на три класса. Первый класс— оранжево-красные красители, второй—желтые, третий—остальные, е особыми свойствами.
Каротиноидные красящие вещества.
I. Группа ликопина
Ликопин Капсумин а Арумин Капсумин β Родоксантин Таксородин Капсумин у
Оранжево-красн. красители. Растворимость возрастает от ликопина до капсумина у • Дает три спектра поглощения, из них первый между D и Е фраун-гоферовых линий
II. Группа каротина Фисалин "i Желт, красители. Растворимость Сорбузин I в голе возрастает от фиса-Каротин > лина к филлоксаитину
Ксантофилл I Спектры поглощения сдвинуты Филлоксантин) больше к фиолетовой части
III. Группа календулина Календулин Филлородин
Каротин (С40Н56) содержится вместе с хлорофиллом в зеленых частях большинства растений и имеет, по Карреру, строение полиметинового красителя, составленного из ряда групп
—сн=сн-с=сн-
СНз
Ксантофилл (С4оН5602)—повидимому продукт окисления каротина, сходный с ним по спектральным свойствам и сопутствующий ему. Ликопин— К. в томатов, содержащееся также и в яичном желтке; отличается от каротина оранжево-красной окраской.
Промежуточное положение между азотсодержащими и безазотистыми К. в занимают красители, получаемые из некоторых лишайников, наир, орсейль и лакмус. В лишайниках (Roceella tinctoria и др.) содержатся производные орсина (диоксиа), как то: орселиновая к-та, ее эфир—пикро-эритрин и диорселиновая(леканоровая)к-та, причем последняя преобладает. сн,
I
орсин
СН3
JL /Соон орселиногая к-та
СНз !
Л
НО
ООН
чО-СН2—(СНОН)2-СН2ОН
пикроэритрин
СНз ноосч 1 но.,
он
ro/^Ni-co/y
СНз леканоровая к-та
При окислении в присутствии Са(ОН)2 и аммиака эти продукты, переходя через орсин, дают красители неизвестного строения, содержащие азот. Главным из них является орсейль, широко применявшийся в средние века для окраски шелка в красный цвет. Более длительная обработка вышеприведенных продуктов приводит к лакмусу (смотрите), применяемому гл. обр. в качестве индикатора. Строение лакмуса также неизвестно.
II. Азотсодержащие естественные К. в Этот класс естественных К. в характеризуется наличием представителей шестичленных пиридиновых и пятичленных пирроловых циклов. К первым относится изохиноли-новый краситель, берберин, ко вторым же— индиго, хлорбфилл и гемоглобин. Вопрос о получении в растительном организме изо-хинолинового цикла, связанный с образованием и других азотсодержащих циклов в растительных ах, требует еще разъяснения. Берберин, красящее вещество корня барбариса (Berberis vulgaris), на
J
сн2
N
сн2
Н2С:
,он
С"
К
НС
*сн
i—О СНз —ОСНз ходит нек-рое применение в крашении шерсти и кожи, аналогично основным хинолиновым красителям. Наличие в берберине двух конфигураций пирокатехиновой кислоты или пирокатехинового альдегида роднит его с целым рядом предыдущих К. в и возможно, что генезис их во многом сходен. Индиго содержится в виде глюкозида индикана в листьях и стеблях индигоносных растений; на юге России и в Ср. Германии до конца 19 в культивировалось растение Isatis tinctoria (вайда); виды Indigofera tinctoria и Polygonum tinctorium культивируются еще и в настоящее время в колониальных странах. Лучшие сорта естественного индиго (бенгальский индиго) содержат до 90% основного К. в.·—индиготина, худшие же сорта (эквадорский или индиго из вайды)—до 10—15%. Из индигоносных растений краситель получается путем разложения индикана и окисления образующегося при этом индоксильного производного (смотрите Индиго). Из индигоидных К. в осо-
€ого интереса заслуживает так называемый пурпур древних
Br /NH /NH ^/Br
х с Ч с /О
II (|
о о представляющий собой диброминдиго и выделяемый моллюсками Murex purpurea. Этот краситель, очень ценившийся в древности, был получен синтетически из 4-бром-2-ни-тробензальдегида по методу Байера-Древ-сена и оказался вполне идентичным с естественным пурпуром. В настоящее время он никакого применения не имеет.
Наиболее важными по своему физиологическому значению из всех естественных К. в являются хлорофилл (К. в зеленых частей растений) и г е-моглобин (К. в крови позвоночных животных). В основе строения обоих веществ леяшт одно и то же пирроловое ядро и сложное производное последнего—э тиопорфирин. Вилынтеттеру удалось выделить хлорофилл в чистом виде и детально исследовать продукты его разложения, вплоть до общего родоначальника хлорофилла и гемоглобина—этио-яорфирина. В листьях растений содержатся:
хлорофилл А
(C31H29N3Mg) (NHCO) (СООСНз) (С20Н39СОО),
хлорофилл В
(CsiH2,ON3Mg) (NHCO) (СООСН3) (С20Н39СОО), каротин и ксантофилл. Вилынтеттер разработал способы разделения этих К. в., доказал присутствие в хлорофилле Mg и дал методы его удаления, а равно и обратного внедрения. При действии к-т хлорофилл теряет Mg и переходит в феофитпн. Последний является эфиром сложного а, фитола и карбоновых к-т различного строения (в зависимости от условий распада), называемых фитохлоринами (для хлорофилла А) и фитородинами (для хлорофилла В). Известно 17 различных фитохлоринов и фитородинов; существование их Вилынтеттер объясняет различными лактамообразными группировками—т. н. алло-меризацией. При действии щелочей фитохлорины и фитородины теряют С02, переходя через фвллопор-фирин в этиопорфирин, C3iH3eN4. Во все промежуточные продукты, действуя CH3MgJ, можно ввести вновь Mg и получить таким образом их Mg-производные (филлины).
Гемоглобин находится в венозной крови, артериальная же кровь содержит его оксипроизводное (ок-сигемоглобин). Оксигемоглобин имеет молекулярный вес ~17 000 и м. б. расщеплен на две составные части: белковое вещество—глобин и красящее—гематин, (C28H24N4)(FeOH)(COOH)2(CH:CH)2, которое дает хлорид, гемин, (C28H24N4)(FeCl)(COOH)2(CH:CH)2. В ге-мине и его производных содержится железо. Гоппе-Зейлер, удалив из тематика железо, получил гемато-порфнрин, (C2sH26N4)(COOH)2(CH2-CH2OH)2, в котором им было обнаружено присутствие ненасыщенных ввниленовых групп СН:СН. При восстановлении последних может быть получен либо мезогемин, (C28H24N4)(FeCl)(COOH)2(CH2-CH3)2, либо мезопорфи-рив, (C28H26N4)(COOH)2(CII2-CH3)2,a мезопорфирипо-ген для лишенных Fe молекул. Из гематопорфирина действием КОП в метиловом е Вилынтеттер получил гемопорфирип, (C3iH34N4)(COOH)2, из которого по удалении С02 получился тот же этиопорфирин, (C3iH36N4), что и из хлорофилла. В молекуле этио-порфирина предполагают наличие четырех пиррольных ядер.
Билирубин, продукт распада К. в крови, образуется в печени и имеет состав 032Η380βΝ4. При действии щелочи он дает гематиновую к-ту, то есть должен содержать оксипиррольное ядро. Энергичное восстановление билирубина дает замещенные нирро-лы, наряду с билирубиновой к-той. В силу этого билирубин по строению своему должен быть близок к гемину. К этому же типу веществ близки нек-рые красители, содержащиеся в моче, а также К. в., обусловливающие окраску волос и перьев животных.
Лит.: Rupe Н., Chemie d. natiirlichen Farbstof-fe, T. 1—2, Brschw., 1900—09; Brigl P., Chemi-sche Erforschung d. Naturfarbstoffe, Brschw., 1921; Willstatter R. u. Stoll A., Untersuchun-gen liber Chlorophyll, В., 1913; Willstatter R. u. Stoll A., Untersuchungen liber die Assimilation der Kohlensaure, B., 1918; KSster, Zur Kenntnis d. Hamins, «Arcb. d. Pharmazie u. Ber. d. Deutsch. Pharmaziegesellschaft», Berlin, 1915, В. 253, p. 457;
Fischer F., Zur Kenntnis d. Porphyrine, «Lleb. Ann.», 1917—29; Willstatter R., tlber Antho-cyane, ibid., 1915, В. 408, p. 1—163; 1917, В. 412, p. 113—231; D i m г о t h О., «B», 1920, B. 53, p. 971; Freudenberg K., ibid., p. 1416; G e о r g i e-v i c s Indigo v. praktischen u. theoretischen Stand-punkt, Leipzig—Wien, 1892; Karrer P., «Helvetica chimica acta», Basel, 1926—29; К 6 n i g W., «Journ. prakt. Chemie», Lpz., 1926, p. 1; Robinson J., «Journ. of the Chem. Society of London», 1927, v. 121, p. 15; H e i 1 b о r n J., ibid., p. 1203; К y-1 i n H., «Zeitschrift fiir phvsiolog. Chemie», Berlin, 1926, B. 15 7, p. 148; К у 1 i n H., ibid., 1927, B. 163, p. 229. И. Иоффе.
Красящие вещества синтетические.
К. в (красители) синтетические—органич. цветные вещества, способные в процессе крашения сообщать тот или иной цвет волокнистым материалам (текстильным волокнам, бумаге, дереву, коже, меху, соломе и тому подобное.). Подавляющее большинство синтетич. К. в принадлежит к соединениям ароматич. ряда; исходными материалами для синтеза их служат ароматич. и гетероциклическ. соединения, добываемые из каменноугольной смолы или коксовальных газов (смотрите Коксобензольное производство). Поэтому такие красители называют иногда каменноугольными, или смоляными, или д е г т я р н ы-м и. Иногда их называют также а н и л и-новыми красками, по первым представителям их, которые готовились из анилина. Термин «краска» в применении к синтетич. красителям, хотя и очень распространенный, является неправильным, т. к. краской называют обычно смесь К. в с другими веществами (загусткой, олифой, камедной водой и тому подобное.), наносимую на окрашиваемый предмет; красителем же, или К. в., является лишь один из ингредиентов этой смеси, именно тот, который сообщает цвет краске и окрашиваемому предмету. Прежде синтетич. К. в называли пигментами, опять-таки неправильно, т. к. пигмент ы—лишь небольшая группа красящих веществ, нерастворимых в воде и служащих для поверхностного окрашивания.
Кроме крашения (смотрите) волокнистых материалов синтетич. К. в находят применение для окраски жиров и других пищевых веществ, лаков, искусственных смол и пластин. масс, всевозможных поделочных материалов, для производства цветных карандашей, чернил, тушей, копировальной бумаги, в косметике, в фотографии (в качестве сенсибилизаторов), для изготовления светофильтров и для окраски микроскопии, препаратов. Некоторые К. в служат в физиологии и медицине для целей диагностики, другие же применяются как лекарственные вещества (преимущественно антисептического характера).
Теория цветности и строения К. в При прохождении сложного белого света через слой какого-либо вещества некоторые из составляющих свет колебаний затухают или, как говорят, поглощаются, абсорбируются веществом. Если поглощеп какой-либо из видимых лучей спектра, то поглотившее его тело кажется окрашенным в цвет, дополнительный к поглощенному, а в спектре прошедшего через него света обнаруживается темная линия или полоса (или же несколько полос, если поглощено несколько лучей). Если поглощаются только ультрафиолетовые лучи, то тело кажется бесцветным, но, фотографируя его спектр поглощения, обнаруживаем полосу на месте поглощенных лучей. Бесцветными кажутся также тела, имеющие поглощение лишь в инфракрасной части спектра. Правильнее было бы называть тела, погло-
тающие какие-либо участки ультрафиолетовых или инфракрасных лучей, не бесцветными, а невидимо д в е т н ы м и.
При сравнении ряда цветных тел всякое передвижение полосы поглощения от фиолетового конца спектра к красному называют углублением ц в е-т а (батохромией), обратное же передвижение—п о-вы шепнем (гипсохромией). Наиболее «высоким» из видимых цветов является желтый, так как ему соответствует поглощение в фиолетовой части спектра; затем идут: оранжевый, красный, фиолетовый, синий и наконец наиболее «глубокий»—зеленый, дополнительный к поглощаемому красному. Эти термины экстраполируют и на ультрафиолетовую и инфракрасную части спектра, так что углублением света называется всякое передвижение поглощения в сторону лучей с большей длиной волны, а повышением— обратное. Все факторы, способствующие углублению цветй, называются батохромными, а противоположные—г ипсохромными. Поглощение света каким-либо телом можно представить в виде кривой (абсорбционной диаграммы), если, отложив на оси абсцисс длины волн, откладывать на ординатах соответствующие им степени освещения, определяя последние в каждом участке фотометрически. Такие кривые будут иметь минимумы в тех местах, где находятся наиболее поглощаемые данным телом лучи.
К. в с волокнистыми материалами дают комплексы видимоцветные, то есть имеющие поглощение в видимой части спектра. При этом многие красители имеют в субстанции или в растворе иной цвет, чем на волокнах; некоторые красители дают на разных волокнистых материалах различного оттенка окраски; цвет многих окрасок зависит от состава примененной при крашении протравы; наконец имеются единичные случаи, когда краситель сам по себе кажется бесцветным, но на волокнах по протравам дает видимую окраску. Т. о., вообще говоря, К. в не должны быть обязательно видимоцветными телами, но во всяком случае каждое К. в должно иметь спектр поглощения, близкий по своему расположению к видимой части спектра или лежащий в ней. Б последнем случае оно само будет видимоцветным, во втором же—невидимоцветным.
Не всякое цветное тело будет представлять собой К. в Известно много цветных органических (а также минеральных) соединений, которые никакого цвета волокнистым материалам не сообщают. Несомненно, что цветность какого-либо химич. соединения и его способность окрашивать волокна теснейшим образом связаны с химическим строением.
Вполне законченной и научно обоснованной теории цветности до сего времени не существует. Однако имеется много отдельных наблюдений относительно влияния строения органических соединений (и в частности К. в.) на их цвет. Вначале это относилось лишь к видимоцветным телам и к цвету, определяемому наглаз, но с развитием спектроскопии (Хартлей, 1879 г.), а в последнее время спектрофотометрии цвет всякого видимо или невидимо окрашенного соединения может быть твердо установлен по положению максимумов поглощения им световых лучей. Если ограничить круг рассматриваемых органических соединений теми, которые имеют полосы поглощения в пределах от 300 до 850 πιμ, то есть лежащие в видимой или в ближайших к ней ультрафиолетовой и инфракрасной частях спектра, то среди этих органич. соединений мы не найдем ни одного предельного соединения. Для того чтобы органич. соединение имело избирательное поглощение в указанных пределах, оно должно иметь кратную (двойную) связь. На это обстоятельство указал еще в 1868 году Гребе. Спустя 8 лет О. Витт развил положение Гребе подробнее в своей т. н. хромофорной теории цветности и строения красителей.
По О. Витту, носителями цветности—х р о м о ф о-рами—являются ненасыщенные группы, папр.
—СН=СН-, у С~0, /C=S, ^>С—N—, — N-0,
—Nf, —N:N—
в соединении с ароматическими радикалами они дают т. н. хромогены, которые м. б. и цветными и бесцветными (по нашим теперешним понятиям—невидимоцветными) телами. При введении в молекулу хро-
/R
могена групп —ОН, или— NH«, или вообще —Nr,
Ri
названных Виттом а у к с о х р омными (помогающими цветности), цвет сильно углубляется, и в то же время соединение делаетея настоящим красителем. Кроме этих ауксохромных групп свойства красителей цветным соединениям придают группы
—S03H и —СООН, не углубляющие цвбта, или, вернее, в разных случаях действующие различно—то ба-тохромно (углублятоще) то гипсохромно (повышаю-ще). Группы —S03H и —СООН называются с о л е-образующими. Теория Витта сыграла громадную роль как прекрасная схема для классификации К. в., но в настоящее время известно много фактов, не укладывающихся в ее рамки. Прежде всего число ауксохромных групп сильно разрослось: к ним причисляют и группы —OR (где R—алкил или арил), и сульфогруппы, и ациламидные, п даже атомы галоидов. Сейчас в значительной степени стерлась граница между хромофорами и ауксохромными группами.
Второй распространенной теорией цветности была теория х иной дного строения, основоположником которой должен считаться Р. Нецкий; определеннее формулировал ее Армстронг. Исходя из того, что большая часть К. в и других цветных тел заключает в своей молекуле хинонные или хиноид-ные кольца, сторонники этой теории принимают, что все видимоцветные тела должны иметь хиноидное строение. При этом очень многие соединения, которые по способу их получения и по химическим реакциям не имеют хиноидных колец, считаются таутомерами, способными существовать и в хиноидной форме. Эта теория дала возможность еще удобнее классифицировать синтетич. К. в., но не могла объяснить всех случаев цветности органич. соединений. Следует заме-. тить, что она явилась отнюдь не опровержением, а лишь расширением теории Витта, так как и хромофоры и ауксохромы Витта находят себе место в хиноидных кольцах. Однако с течением времени было найдено немало соединений, в которых шестичленных хиноидных колец заведомо не может быть, как например цветные фульвеновые углеводороды типа НС^-СНЧ ✓R
I >С=С<
ΗΟ=ΟΗχ xRi
Пришлось расширить теорию хиноидного строения цветных тел в том смысле, что причиной цветности служат не сами хиноидные кольца, а наличие в химич. соединении большего или меньшего количества «конъюгированных» (согласно представлениям Тиле) двойных связей, чередующихся с простыми, причем особое расположение этих связей, наблюдаемое в хино-нах, особенно благоприятствует появлению видимой цветности. Так. обр. причиной цветности в фульвенах служит наличие группировки
имеющейся в удвоенном виде и в n-хинонах; в молекуле индиго носителем цветности является группировка-
/с^с
—с 4 с—
II. II
имеющаяся тоже в n-хинонах; в а-дикетонах—группировка
!
С
I
с
I
свойственная также о-хипонам, и т. д. При этом все известные практически применимые синтетич. К. в., с допущением в них возможности таутомерии, удавалось подвести под тот или иной хиноидный или полу-хиноидный тип. Опять-таки и при таком расширении теории хиноидного строения виттовские хромофоры и ауксохромы находили себе место как части «полу-хинонных» группировок или же как группы, дающие начало таутомеризации соединений в полухиноид-яые тела. Подобно теории Витта и теория хиноидного строения красителей не затрагивала физической сущности причин цветопоглощения органическими соединениями, констатируя лишь связь этого цветопоглощения с присутствием хиноидных (или полухиноид-иых) группировок атомов.
Первой попыткой глубже проникнуть в сущность явлений была осцилляц ионная теория Бэ-• ли, сущность которой заключается в следующем. Простейшими соединениями, обнаруживающими избирательное поглощение ультрафиолетовых лучей вблизи видимой части спектра, являются таутомеры кето-энольного типа—ацетоуксусный эфир (смотрите), ацетил-ацетон и тому подобное. При каждом перемещении двойной связи происходит перемещение валентных электронов; следовательно внутри молекулы имеется непрерывное колебание электронов, синхронное с известной группой электромагнитных волн, представляющих собою ультрафиолетовые лучи. При прохождении белого света через такие тела те волны ультрафиолетовых лучей, колебания которых синхронны с происходящими внутри тела, интерферируют с последними и затухают: получается поглощение света определенной длины волны. Аналогично этому в ароматических ядрах (например бензольном), если принять теорию осцилляции двойных связей
/%
I- II £ II -I %
происходят непрерывные ритмические колебания электронов, синхронные с определенными ультрафиолетовыми лучами. Этим объясняется и невидимая цветность, присущая всем ароматич. соединениям.
Другой тип осцилляции связей—и зорропе-з и с—существует в α-дикетонах, хинонах и их производных. Например строение α-дикетонов, о-хиио-нов и их производных колеблется между дикетонной и перекисной формами такого типа R—C=0 R—С—О
I £ II I
Ri—С=0 R,—С—О
строение п-хинонов также колеблется между дипетон-ной и перекисной формами
.СН^гСН.,
О—С
/Л
ЧСН -сн
—I
С-0 О-С,
сн—сн с—о
Эти колебания медленнее, чем осцилляция кетоэноль-ных таутомеров или ароматических соединений, и синхронны б. ч. уже с лучами видимой части спектра. Поэтому большинство хиноидных тел являются вп-димоцветными. В частности этим объясняется цветность красителей, построенных по типу хинона.
Положения этой теории впоследствии были развиты на основе очень распространенной среди окрашенных тел таутомерии, в которой виттовские ауксо-хромы играют важную роль, и приведены в согласие со взглядом Ад. Байера на строение трифенилмета-новых красителей, считавшего, что ион хлора в основных красителях этого ряда осциллирует между амидными ауксохромами, попеременно образуя с ними солеобразные группировки, что иначе можно выразить так: амидированные ядра основных трифенилмета-иовых красителей попеременно принимают хиноид-ную форму; осцилляция связей (или, что то же, электронов), происходящая при этом, является источником поглощения света этими красителями
N(CH3)2
N(CII3h
схема Байера
.(CH3)2N-<^)-C=;<^)-N(CIl3)2Cl:
£ Cl(CH3)2Nr_<^ -;C-<^>-N(CH3)2хиноидная схема
Хотя эта гипотеза являлась уже попыткой связать строение цветных тел с физич. природой светопогло-щения, однако она, по крайней мере в области красителей и вообще видимоцветных тел, базировалась попрежнему на хиноидной их структуре. Между тем приблизительно одновременно с ее возникновением были открыты явления, повпдимому в корне противоречившие теории хиноидного строения, даже со всеми внесенными в нее поправками: это—видимая цветность свободных радикалов и явления галохромии (смотрите). Все химические свойства свободных радикалов (трифенил-метила и тому подобное.) наиболее согласуются с принятием в них трехвалентного центрального углерода, например <С6Н5)3С—, то есть с высшей степенью ненасыщенности аакого рода соединений. Т. о. в качестве основной причины цветности выступает ненасыщенность соединений и известная пропорциональность, наблюдаемая (при прочих равных условиях) между степенью этой непа-
сыщенности и глубиной цвета. Т. к. ненасыщенность соединения связана с наличием некоторого запаса свободной энергии в его молекулах, то гипотеза эта примыкает к современным теориям строения материи. В последнее время получил значительное распространение взгляд на красители (по крайней мере па нек-рые группы их) как на комплексные соли, в которых анион (или соответственно катион) находится во второй координационной сфере. Например основные трифенил-метановые красители формулируются Фирц-Давидом
N.
R
Nis
-о-
С1
л
N xRi
как карбониевые соли (I), а Кермаиом—как хшюид-ные комплексные соли (II)
/R N<
И Ri
II.
.Ν·
-о-
Cl
l/tt
I- XRi
Подобные же конфигурации Керман придает и ф-лам азинов, оксазинов, тиазинов и т. д. Соли (лаки) протравных красителей еще со времени работ Л. А. Чугаева и Вернера рассматриваются как внутренние комплексные соли.
При взгляде на видимоцветные тела как на комплексные или молекулярные соединения и при объяснении цветности их большей или меньшей ненасыщен-иостыо получает объяснение и глубокая цветность хингидронов, солей Вурстера, а также становится понятным, почему -нет цветных тел среди вполне насы-.щепных соединений. Тем не менее для глубокоцветных тел многие исследователи все же принимают часто, наряду с комплексным строением, также и хино-идное строение хотя бы некоторой части их молекул. Таков например приведенный выше взгляд Кермана на строение основных трифенилметановых, азиновых и других красителей.
Осцилляционная теория цветности м. б. согласована с теорией ненасыщенности как причины цветности: во время осцилляции электронов внутри молекулы связи между атомами оказываются периодически на некоторое время порванными, следовательно атомы в этот период являются ненасыщенными, то есть обладают повышенным уровнем энергии.
Дальнейшим развитием и до известной степени синтезом всех приведенных выше теорий цветности является формулированная в последнее время В. Кенигом, а частично еще и раньше В. А. Измаильским теория полиметинового строения цветных тел. Выше было отмечено, что избирательное поглощение в видимой и близких к ней частях спектра имеется у всех тел с «конъюгированными» двойными связями. В простейших случаях это будут углеводороды, которые содержат по нескольку мети-новых (—СН=) или виниленовых (—СН=СН—) групп. Недавно Куну L1] удалось получить ряд углеводородов с длинными цепями таких виниленовых групп, до 1,18-дифенил-октадекапонаена
<^>—СН=СН—[СН=СН]7-СН=СН-<^>
включительно. Цвет этих углеводородов, начиная от видимобесцветного стильбена
0СН=СН-0
последовательно углубляется с прибавкой каждой виниленовой группы, переходя к желтому,оранжевому и наконец к меднокрасному с синеватым оттенком. Цвет подобных соединений еще значительно углубляется при введепии в них ауксохромных групп.
Кениг в своих изысканиях исходит именно из таких соединений—например солей оснований общей формулы Вч ,R
/N—(CH)2n—i—N
в I xRi
X
где R и Ri—любые радикалы, а X—какой-либо анион, например С1. При п=3 имеем следующее соединение (изображая его строение классической структурной Формулой)
Rv ’ /R
>N—СН=СН—СН=СН—СН= N<
R I XRx
X
Подобного рода соли образуются присоединением например галоидного алкила RiX к импдооснованиям. Так как подобные соли проводят электрический ток, то, согласно теории Вернера, анион×должен лежать отдельно от Rlf во второй координационной сфере
^N—СН=СН—СН=СН—сн—n Х Ф Х
+
R Ri
X
На обоих концах цепи получаются так. обр. совершен-/R
но идентичные группы —N, то есть ауксохромы. По-
xRi
следние же способны обнаруживать, сверх нормальной валентности их центрального атома, одинаковые количества положительной и отрицательной дополнительной валентности, то есть имеют характер диполей. Анион X, обладающий отрицательным зарядом, должен быть связан с остальной частью молекулы (комплексным катионом) ослабленной связью, на которую затрачивается неполная его валентность
R -
zN—СН=СН—СН~СН—СН—N^“. X
Rj/---.---XR!
L +
Предположим (произвольно), что×связан неполной связью с правым (в ф-ле) атомом N. Последний, переходя из трехвалентного состояния в пятивалентное, обнаруживает, еверх нормального, одинаковые количества положительного и отрицательного сродства (равные по величине заряды + и -). Положительный побочный заряд нейтрализуется отрицательным зарядом аниона, но не полностью, т. к. анион связан лабильно. Остаток этого положительного заряда связывает часть остающегося у азота отрицательного заряда, остальная же часть последнего затрачивается на образование второй связи между N и метиновой группой; эта вторая связь является тоже ослабленной (неполной). Со стороны первой метиновой группы на образование этой связи расходуется также неполный положительный заряд, часть которого, оставаясь неиспользованной, оттягивает на себя часть отрицательного заряда второй метиновой группы и т. д. Таким образом в конце-концов индуцируется частичный положительный заряд у пятой метиновой группы, берущий на себя часть побочного отрицательного заряда атома N второго ауксоз^рома (левого в формуле). У азота этого ауксохрома также останется следовательно нек-рая свободная часть положительного заряда, которая может быть затрачена на нейтрализацию остаточного отрицательного заряда аниона. Иными словами, получается замкнутая цепь подвижных гете-рополярных связей, изображаемая следующей ф-лой, в которой ослабленные связи представлены волнистыми линиями, а остаточные частичные заряды соответственных атомов—знаками -f- и —
R4 — + — 4* — + _ /R
>N—СН—СН—GH—СН—СН—N< RiX+ 5 4 3 2 1 +XR!
Внутри этой цепи, вследствие лабильности частичных связей, происходит постоянное смещение валентных электронов с одной орбиты на другую, вызывающее эффект светопоглощения. Чем длиннее цепь, то есть чем большее число отдельных силовых полей этих электронов частично перекрывает друг друга, тем большее влияние оказывают колебания одних электронов на другие, взаимно замедляя друг друга. Поэтому для неремещения электронов на их крайние внешние орбиты требуются такие кванты энергии, которые м. б. получены лишь от световых лучей с достаточно большой длиной волны. Соответственно, с удлинением цепи конъюгированных метиновых групп,абсорбциясве-та перемещается все больше в область лучей красной части спектра. Сопряжение с анионом двух крайних ауксохромов, представленное на приведенной выше ф-ле, соответствует максимуму поглощения, лежащему всего ближе к красному концу спектра; однако можно допустить, что частичные отрицательные заряды аниона м. б. нейтрализованы частичными положительными зарядами всякой другой пары групп, паир. зарядами одного из ауксохромов и метиновой группы 1-й, 3-й или 5-й. В последнем случае образуются две (или более) замкнутые цепи, служащие причиной абсорбции света с меньшими длинами волн, например:
R ч — + —
>N—СН—СН-
L
+ — + _ /R
СН—СН—СН— N(
+ XRi
Возможность замыкания более коротких цепей дает начало новым абсорбционным полосам в спектре. Поэтому существуют тела с 2, 3 и более максимумами поглощения света.
Аналогично трактуются Кенигом соли с катионами во внешней сфере; например соединение
О=СН—СН=СН—СН : изображается так
: CH-ONa
+ - + - +
о—сн—сн—сн—сн—сн— о и
Na
При разнозначных крайних ауксохромах может происходить внутреннее замыкание и без помощи аниона или катиона, например
+ — + — 4- — /R
О—сн—СН—сн—СН—СН—N<
7 + xRi
Перенося эти воззрения на более сложные цветные соединения, Кениг приходит например к следующей формуле для основных трифенилметановых красителей
R
Ri
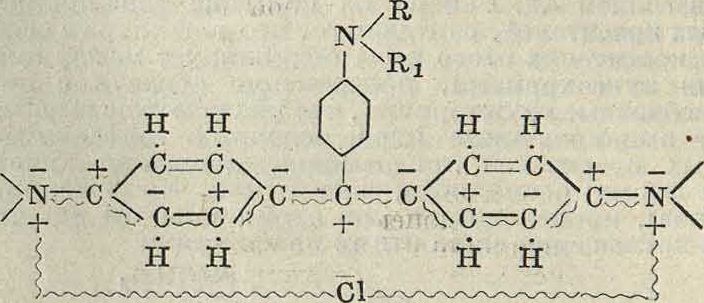
Теория Кенига, наиболее согласованная с теорией строения атома и с современными воззрениями на природу светопоглощения, хорошо объясняет многие явления в области цветности органич. соединений, но не получила еще полного развития в приложении ко всем цветным телам.
Классификация красителей. Так как большинство красителей, при условии допущения таутомерии их, можно считать хиноида-ми, то представляется весьма удобным классифицировать синтетич. К. в по типам заключающихся в них хиноидных колец. Эта, хотя и не вполне точная, классификация представляет большие удобства для запоминания и для обобщений в области синтеза; она м. б. легко перестроена как на более старую классификацию по хромофорам, так и на классификации по типам комплексов, по осцилляционным типам и на кениговскую (смотрите выше).
Все синтетич. К. в можно разделить на следующие классы.
I. Хинонные красители, характеризуемые присутствием в их молекуле п-или о-хинонного кольца (или половины последнего)
0=0°
или
bс=с с/
II
о
хс
II
1) Индиго и индигоиды. 2) Нафтохинонные красители. 3) Антрахинонные красители.
0-Ο=:
NOH или
II.×и н о н о к с и м н ые, характеризуемые наличием п- или о-хиноноксимной группировки
>°
J—NOH
1) Нитрозокрасители (хиноноксимы). 2) Пи-трокрасители.
III. Хинонгидразонные, характеризуемые присутствием группировок
0=O=N-NHKhhhQ^Nhr
И
-NRi
;=n-nhr
1) Гидразонпиразолоновые красители.
2) Азокрасители. 3) Стильбенов. красители.
IV. Хинонимидные и хинон-диимидные, характеризуемые присутствием группировок
R!N=<^)-N-NHR ИЛИ
о
NR или или RxN ^>=NR
ИЛИ 0=NB
1) Индамины и индофенолы. 2) Азины и азонии, черный анилин, оксазины и тиази-ны. 3) Сернистые красители.
V. Метиленхинонные и мети-ленхинонимидные, характеризуемые присутствием групп
R. у—. V =iO /®·
^CXR,
R;
R
к>
О или
=NR°XRi
1) Трифенилметановые. 2) Акридиновые.
3) Ксантеновые. 4) Оксикетонные и кетони-мидные (дифенилметановые) красители. 5) Хинолиновые красители.
Класс I. Хинонные красители.
Группа I. И н д и г о и д н ы е К. в (красители полухинонного типа). Они получили свое название от старейшего представителя этой группы—синего индиго (смотрите)
О
/NH
С—с
/NH,
CO чсо и заключают всю свойственную его молекуле «полухинонную» группировку атомов
II о=с с=о с=с
Подобно тому как w-хинон по своим химическим свойствам м. б. отнесен одинаково как к у-дикетонам, так и к перекисям и принимается б. ч. за’соединение таутомерное, существующее в обеих этих формах:
о—:
-/=.
=
П
=/“
-о так же ииндигоиды м. б. представленьГв двух таутомерных формах
Y. " /Z
х. bс=с<
О
С-С:
И.
i
и
Существованием перекисной формы (II) естественнее всего объясняется свойство всех индигоидов легко восстановляться в лейко-соединения (смотрите), имеющие след, строение:
чс>с
I
он
/Z
Чс/”
он
Подобно гидрохинону, являющемуся лейко-соединением хинона, и щелочные растворы лейкосоединений индигоидных К. в легко окисляются в красители, нерастворимые в воде. На этом основано и крашение ими различных волокон (смотрите Крашение). Что касается цветности этих красителей, то между ними встречаются вещества всех цветов видимого спектра, но лишь немногие из них дают окраски ходовых оттенков. Цветность индигоидных красителей, по теории Витта, зависит от присутствия в них трех хромофорных групп: двух групп=С=0 и одной -CR=CR-, соединенных с двумя ароматическими ядрами, и ауксохромных групп —NH—, —S—, —О—, внедренных между хромофором и ароматич. ядром.
Теория хиноидного строения приписывает цветность индигоидов наличию полухи-нонной группировки (включающей все три хромофора Витта) и связанных с ней ауксохромных групп. По Кенигу, можно было бы представить например индиго в следующем виде:
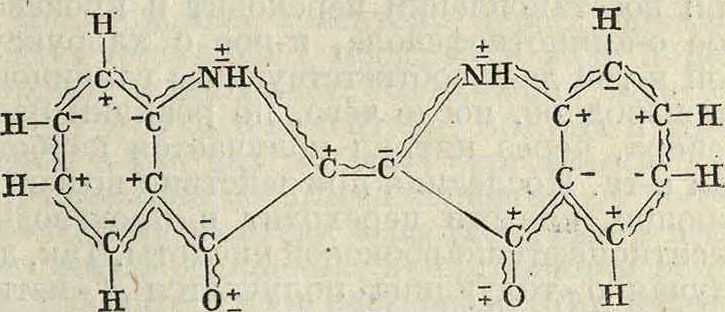
что в упрощенном виде выражается и таутомерной ф-лой индигоидов, приведенной выше. Рациональная классификация индигоидов приведена в ст. Индигоидные красящие вещества.
По строению и методам получения индигоидные К. в могут быть разделены на симметричные и несимметрич-н ы е. Первые обычно получаются окислением двух молекул одного и того же вещества, вторые же—конденсацией двух различных компонентов. К первым следует отнести 2, 2-бис-индодиндиго, 2, 2-бис-нафт-индолиндиго, 2, 2-бис-антриндолиндиго, а также соответствующие тионафтеновые и другие производные. Второй отдел охваты-. вает несимметричные индигоиды, как 2, 3 -бис-индолиндиго (индирубин), 2-тионаФтен-3 -индолиндиго (тиоиндиго алый R) и другие. Среди, индигоидных красящих веществ доминирующее значение имеют красители, содержащие по два пятичленных цикла; но существуют и такие, которые имеют только один пятичленный цикл либо вовсе не имеют такового. При получении как симметричных, так и несимметричных индигоидов необходимо заранее синтезировать промежуточные продукты, содержащие замкнутые, характерные для ^ этих ^красителей циклы: индоксил, изатин, изатинанилид, 3-окситионафтен и тому подобное. В промежуточных циклических соединениях, служащих для получения индигоидов, является характерным наличие кетоэнольной таутомерии. Целый ряд соединений, способных к кетоэнольной таутомерии, м. б. применим в качестве промежуточных продуктов для синтеза индигоидов. Наиболее важными исходными веществами являются α-нафтол (I), оксиантра-цен (II), оксиантрахинон (III) и ряд хинонов он он
О
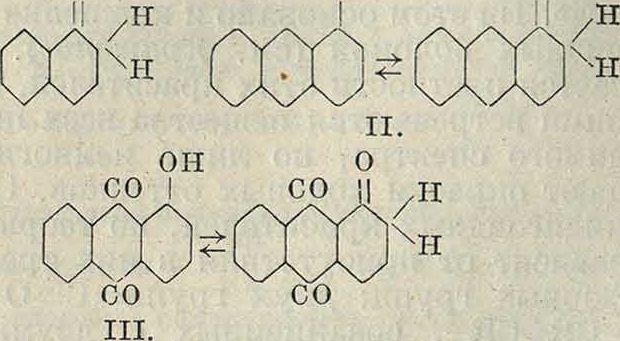
О получении индоксила, изатинанилида и изатина см. Индиго, тиоиндоксила—см. Индигоидные красящие вещества. 3-окситионафтен, важный полупродукт синтеза индигоидов, получают по способу Фридленде-ра, исходя из антраниловой кислоты, или, по способу Герца, исходя из анилина и двухлористой серы, причем происходит как хлорирование анилина, так и внедрение в бензольное ядро серы. Полученный продукт при восстановлении переходит в производное о-аминотиофенола, к-рое с хлоруксус-ной к-той дает соответствующее глициновое производное, после чего, по реакции Занд-мейера, через нитрил получается карбоновая к-та. Последняя при действии водоотнимающих средств переходит в производное окситионафтенкарбоновой кислоты. Так, для случая о-толуидина получается 4-метил-
6-хлор- 3-окситионафтенкарбоновая кислота, важный продукт для синтеза гидрона розового, по схеме сн, сн3
I
I—νη2
+S2Cl2-i-
сн3
-ΝΗ»
01
сн
I
X4·.
SO1-
/Ч J—SH С17ч С17
СНз
-NH,
-S-CIT2-COOH
С1У
СНз
CN
I—S-CH2-COOH
СУ
1-СООН
S-CH2-COOH
СН,
С17
I-CIOH^C.COOH-
СН I
,-с о
СНз сн
чс=с
S
СО-,
S-
ЧС1
гидрон розовый
Существует много аналогичных способов синтеза производных 3-окситионафтена [2]. Интересен также способ получения изомер ного продукта из того же о-толуидина по следующей схеме:
СНз СНз СНз
I
I
-NHa
СН
-NH2
СНз
I
С!7"
(с ксантогенатом) СНз
i—S—CS —ОС2Нг.
СИ
-SH
СНз
СИ
-S-CH2-COOH
Cl
Cl
—S^CH--C(OH)7"
-С!
s "Чз-
I i
СНз СНз гелиндоновый красный ЗВ
Для получения индигоидов кроме вышеперечисленных продуктов могут служить и их нафталиновые и антраценовые аналоги, получаемые общими методами. Для нафталиновых и антраценовых производных возможны по три изомера, например для нафт-индоксида
С(ОН)=СН NH—сн
I
,-С(ОН)^ -NH
СН
-NH
-С(ОН)
а также и пери-производное сн
УЧ
(НО)С NH I I
дающие различные изомеры нафтиндиго. В последние годы изучение подобных нафталин- и антрацениндигоидных К. в приобретает все большее значение. Из других продуктов для синтеза индигоидов применяются оксипроизводные—нафтолы, нафтохино-ны, аценафтенхиноны, антранолы, оксиан-трацены и др.; сочетая их с различными производными индола и тионафтена, можно получать различные индигоиды как симметричные (окислением двух одинаковых молекул), так и несимметричные (при сочетании двух различных молекул); в последнем случае один из компонентов представляет собою обычно α-дикетон или о-хинон (вернее его производное), второй же—какое-либо циклическое оксипроизводное, способное к кетоэнольной таутомерии. Так, краситель типа о I!
СФ><0
м. б. получен либо конденсацией изатинанилида с нафтолом, реагирующим в кетоформе о
I—со,
н
-nh/c-n°6H5+ н7
СвНкКНа + краситель либо путем конденсации индоксила (реагирующего в кетоформе) с 1,2-нафтохиноном о
I С04зн2 + 0—11 I—NH
* Н2 О + краситель
1. Симметричные индигоиды, Важнейший представитель—индиго, 2,2-бис-индолиндиго—см. Индиго. Тиоинди-го красный, 2, 2 -бис-тионафтенинди-го, получается при окислении двух молекул 3-окситионафтена или непосредственно, по Мюнку, замыканием колец в ацетиленди-тиофенол-о-карбоновой кислоте, по схеме
2 0~соон+С1-СИ:СН·01-~>0-с<Зон CHl=CH ноос-0^ 0^со>Сг=с<со-0
Индигокармин, 5, 5-дисульфокис- лота индиго, получается при действии концентрированной H2S04 на индиго или на фе-нилглицин; применяется мало, как кислотный краситель и для титрования при анализе гидросульфита (См.). Индиго 2R,5,5 -ди-броминдиго, получается при умеренном бро-мировании индиго или синтезом из бром-индоксила; обладает несколько более красным оттенком, чем обыкновенный индиго. Индиго 4В, 5,7,5, 7-тетраброминдиго, получается при бромировании индиго в кипящем нитробензоле; более чистый по оттенку и более прочный краситель, чем индиго. Индиго 6В, 4, 5, 7, 4, 5, 7-гексабром-индиго, получается при действии избытка брома на индиго под давлением; применяется иногда в печатании, дает зеленовато-синие оттенки. Яркий индиго различных марок—хлор- и хлорбромпроизводные индиго, получаемые при хлорировании дегидроиндиго Кальба (смотрите Индиго). Индиго Т, 7, 7-диметилиндиго, получается аналогично индиго,синтезом из о-толуидина или из о-нитрометилбензальдегида; окрашивает ткани в более зеленый цвет, чем индиго. Циба красный разных марок — гало-идопроизводные тиоиндиго, получаемые при галоидированиитиоиндиго. Г и д р о н розовы й—смотрите выше. Тиоиндиго оранжевый, 6,6 -диэтокситиоиндиго, получается при окислении 6-этокси-З-окситиона-фтена. Кроме того в продаже имеется ряд различных галоидо-, окси-, амино-, этокси- и метоксипроизводных различных симметричных индигоидов, получаемых обычными путями. Ряд производных индиго и тиоиндиго,-содержащих вместо бензольных ядер нафталиновые и антраценовые, находится в настоящее время в стадии изучения; из получивших практич. применение представителей этого ряда необходимо отметить тиоиндиго зеленый G, дибром - бис-нафтиндолиндиго строения
В г
-г
i Г
/‘
_ I I
-СО р_р/СО— -NH/C c nh—
-В г он получается при бромировании нафтиза-тина и обработкой бромопродукта по байе-ровскому способу превращения изатина в индиго.
2. Несимметричные индигоиды. Простейший из них — индирубин, 2,3-бис-индолиндиго, сопутствует индиго-
тину в естественном индиго и м. б. получен синтетически при конденсации изатина с индоксилом. Практич. применение имеет его
5, 7, 5, 7-тетрабромпроизводное—циба-гелиотроп В. Аналогичный индиру-бину тиоиндиго алый R, 3-индол-2-тионафтениндиго, получается при конденсации изатина с окситионафтеном. Если вместо изатина взять его 2-анилид, то получается циба серый, 2-индол-2-тионафтен-индиго; практическ. применение имеет только его тетрабромпроизводное циба фиолетовый В.
Из непятичленных циклич. соединений находят применение следующие. А л и зарин-индиго 3R—трибромпроизводное 2-ин-дол-2-нафтолиндиго, получаемое при конденсации дибромизатинанилида с бром-а-на-фтолом; мало применяется (в печатании), прочен к хлору и мылу. Ализарин-индиго G — дибромпроизводное 2-ин-дол-2-антрацениндиго, получаемое при конденсации дибромизатинанилида с а-антро-лом. Ализарининдиго 2G, 2-ин-дол-2-оксантролиндиго, получается при конденсации изатинанилида с оксиантрано-лом. Циба алый 2G, 2-тионафтен-2-аценафтениндиго, получается при конденсации окситионафтена с аценафтенхино-ном. Ряд красителей несимметричных, содержащих в различных сочетаниях нафтин-долы, антриндолы и их сернистые аналоги, находится в стадии исследования.
Индигоидные красители нерастворимы в воде и поступают в продажу в виде порошков или водных паст, содержащих чаще всего ~20% сухого краГсителя. Все они принадлежат к так называемым кубовым красителям (смотрите), окрашивание которыми основано на восстановлении красителя в растворимые в щелочах лейкосоединения, пропитывании волокнистых материалов растворамиэтихлейкосо-единений и обратном окислении их в нерастворимые красители на волокне кислородом воздуха. Лейкосоединения индигоидов
6. ч. желтого или оранжевого цвета, то есть окрашены значительно «выше» самих красителей, что объясняется разрушением в них хромофорной группировки
-ОС-С=С-СО—
I I
Окраски, получаемые при помощи инди-гоидных красителей, почти все отличаются большой прочностью как к свету, так и к мылу и другим реагентам (к-там, щелочам и т. д.). Лишь к трению некоторые окраски (в том числе и самое индиго) не вполне прочны,что объясняют механич. характером связи их с волокном. Наиболее распространенным красителем этой группы является самое индиго. Другие индигоиды применяются в значительно менышм масштабе, гл. обр. вследствие своей высокой цщы и сравнительно высокой стоимости крашения ими, требующего применения гидросульфита.
Группа II. Нафтохинонные красители. Практически годные красители, заключающие бензохинонное кольцо, неизвестны. С технически важными К. в хинон-ного типа мы встречаемся лишь в нафталиновом ряду. Первым (и самым важным) пред-
ставителем этой группы является нафт-а з а р и н, 1, 4-диокси-5, 8-ыафтохинон [3] о он
получаемый нагреванием 1,5- или 1,8-ди-нптронафталина с крепкой берной кислотой и S203 (раствором серы в серной кислоте), причем происходит сначала, восстановление групп— N02 в—NH-OH, затем перегруппировка образовавшегося дигидроксиламин-нафталина в диаминодиоксинафталин, окисление последнего в динафтохинондиимид, омыление этого диимида в нафтодихинон и наконец восстановление нафтодихинона в диоксинафтохинон
Цветность антрахинонных красителей обусловливается, согласно хромофорной теории, присутствием двух хинонных карбонилов и различными ауксохромными группами: —ОН,—NH—,—SR и т. д. Но среди кубовых антрахинонных красителей встречаются и такие, которые совсем не имеют виттовских ауксохромов, например пирантрон, виолантрои и др. Т. о. присутствие ауксохромных групп не является обязательным для красителей, если не принимать за ауксохромы метановые группы, входящие в состав ароматич. ядер. Кубовые красители, к которым принадлежат пирантрон, виолантрон и др., нерастворимы в воде и в строгом смысле слова К. в не являются, так как они либо совсем не усваиваются волокном, либо не дают того цвета и интенсивности, какие получаются при обычном «кубовом» крашении; настоящими
no2
NHOH но nh2
I I I
о NH
I!
I !
N02 NHOH H2N ОН
o2n no2 HOHN- NHOH h2n nh2
! ! I I
HN О HN NH
CQ-00
I I
HO OH
II. о 0
о о
Ιί
II II
о о о он
II I
о он
В виду нерастворимости нафтазарина в воде его обработкой бисульфитом натрия переводят, для применения в крашении, в бисуль-фитное производное
НО 0S02Na /ОН

0Н
NaOaSO ОН
которое при крашении разрушается с регенерацией красителя. Нафтазарин принадлежит к протравным красителям и дает по хромовой протраве глубокосиние, почти черные тона, почему он и называется часто «ализариновым черным S» или «SW». Окраски им отличаютсябольшой прочностью. Глубокий синий цвет окрасок по протраве объясняется образованием внутренней комплексной соли с хромом. Вообще же цветность нафтазарина относят за счет СО-групп (хромофоров) хинонного ядра и гидроксильных ауксохромов (или по хиноидной теории за счет всего хинонного ядра и гидроксилов). Кроме нафтазарина известны: нафтопур-пурин, 1, 2,4-триокси-5, 8-нафтохинон, получаемый окислением нафтазарина, и некоторые производные нафтазарина, замещенные в хинонном ядре остатками фенола или am лина (ализариновый темнозеленый W, ализариновый черный SRA).
Группа III. Антрахинонные К.в. Эти красители представляют собою производные антрахинона (смотрите)
красителями, непосредственно усваиваемыми волокном, служат здесь лейкосоединения, заключающие обычно группу —ОН. В антра-хинонном ряду эти лейкосоединения по цветности часто не только не уступают самим красителям (индантрен), но иногда являются даже глубже окрашенными (желтый флавант-рен, имеющий синее лейкосоединение, и другие). С точки зрения теории хиноидного строения носителем цветности этих К. в является центральное хинонное кольцо антрахинона.
Интересно отметить явления таутомерии среди антрахинонных красителей. Найдено например, что ализарин при попытке этери-фицировать его в щелочном растворе галоидными алкилами дает не ожидаемый эфир (I), а этерифицированное в мезо-положение производное (II)
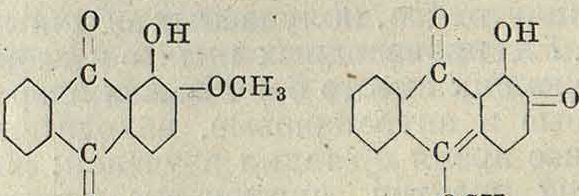
о осн3
I. II.
с правым кольцом, построенным пара-хи-ноидно (В. Перкин мл.), из чего можно заключить, что и щелочные соли ализарина могут существовать в таутомерной и-хино-идной форме. С точки зрения осцилляцион-ной гипотезы цветности такая возмояшость таутомеризации, обусловленная присутствием ауксохромов, давая начало новым осцил-ляционным формам, служит причиной значительного углубления цвета по сравнению с самим антрахиноном. По теории Кенига, соли а дизарина могут быть изображены следующим образом:
^Меч-О 6-
я К
с- +с г
I 11 S
i1 i
О —·?-Me
- +
Синтез ализарина по Гребе и Либерману (из антрацена, через^З-антрахинонсульфокислоту) до настоящего времени является единственным широко применяемым техническим методом получения синтетич. ализарина. В 1871 году Прюдом получил конденсацией амино-ализарина с глицерином весьма ценный краситель— ализариновый синий, положив тем самым начало синтезу ряда сложных циклических производных антрахи-нона. В 1887 году Бонн и одновременно с ним Шмидт заметили способность ализарина и его производных превращаться при действии окислителей в присутствии катализаторов в различные полиоксипроизводные (смотрите Бопна-Шмидта реакция), что позволило обогатить группу антрахинонных К. в весьма, ценными протравными красителями. М. А. Ильинский впервые провел сульфирование антрахинона в присутствии солей ртути, получив при этом а-сульфопроизвод-ные, что позволило получать в большом масштабе целый ряд ценных α-производных антрахинона. В начале 20 века Бонн получил и первый антрахинонный кубовый краситель, иидантрон, и вслед за ним фла-вантрон,исключительная ценность которых направила исследовательскую мысль по новому руслу кубовых антрахинонных красителей. В 1905 году Излером был получен антрафлавон и Шоллем—пирантрон. Год спустя Шолль получил виолантрон, положив этим начало группе ценных бензантроновых красителей. В это же времяУльман ввел в употребление реакцию конденсации аминов с галоидопроизводными в присутствии меди, давшую возможность синтезировать ряд ценных красителей ряда антримидов. В 1909 году Дейнет получил бензоильные производные аминоантрахино-нов, оказавшиеся ценными альголевыми (индантрено-выми) красителями. За сравнительно короткое время антрахинонные К. в заняли одно из важнейших мест среди синтетич. красителей и значение их возрастает из года в год.
По технич. применению антрахинонные К. в делятся на 2 класса: кислотные (гл. обр. протравные) и кубовые. Первые из них м. б. разбиты на два больших отдела: а) оксиантрахинонные красители, которые могут кроме ОН-групп содержать и замещенные ΝΗ2-, SH-группы и тому подобное., и б) красители, содержащие сульфогруппы как в антрахинонном ядре, так и вне его. Оксиантрахинонные красители являются преимущественно протравными и применяются для окраски предварительно протравленных металлич. оки волокон; сульфоантрахинонные же красители благодаря наличию в них S03H-rpynn способны непосредственно окрашивать волокно животного происхождения; при этом они зачастую могут давать при последующей обработке солями хромовой кислоты прочные яркие лаки и применяться как хромировочные красители.
Кубовые антрахинонные красители по их химич. строению м. б. разбиты на два отдела. К первому относятся те красители, в которых наиболее сложным циклом является цикл антрацена и которые получаются конденсацией нескольких антрахинонных производных между собой или с более простыми соединениями, конденсацией, не сопровождающейся образованием новых колец; наиболее простые красители этогокласса—а льголевые красители—представляют собою ацильные, преимущественно бензоильные, производные аминоантрахинонов; более сложные—а н т р-
и м и д ы—содержат по крайней мере 2 антрахинонных остатка, соединенных в различных положениях имидными группами. Второй отдел кубовых антрахинонных красителей содержит различные многоядерные циклы как карбоциклического, так и гетероциклического типов, что может служить основой для их классификации. Общая классификация антрахинонных К. в силу изложенного выше является следующей.
1. Кислотные красители.
А. Оксиантрахинонные красители.
Б. Сульфированные антрахинонные красители: 1) содержащие сульфогруппу в антрахинонном ядре, 2) содержащие сульфогруппу вне антрахинонного ядра.
2. Кубовые красители.
А. Собственно антрахинонные красители: 1) ацильные производные аминоантрахинонов, 2) антримидные красители.
Б. Многоядерные красители: 1) содержащие гетероциклич. ядра; 2) содержащие кар-боциклич. ядра: пиреновые производные и периленовые производные.
1 А. Кислотные оксиантрахинонные красители, содержащие ОН-группы, являются протравными красителями в силу наличия в них способной к лакообразованию группировки (правило Либермана и Костанец-кого), именно двух ауксохромных групп в о-положениях друг к другу и к хромофорному карбонилу. Это правило не является законом, обусловливающим протравные свойства красителей, но в большинстве случаев лишь при выполнении его получаются технически применимые протравные К. в Некоторые полиоксиантрахиноны, не обладающие подобным расположением оксигрупп, не представляют собою красителей, но являются ценными промежуточными продуктами для синтеза более сложных антрахинонных красителей. Ниже приведена таблица наиболее важных полиоксиантрахиш шов с указанием цвета лаков для тех из них, которые применяются в качестве красителей. Положение оксигрупп указано номерами углеродных атомов, при которых они находятся, причем молекула антрахинона перенумерована обычным образом
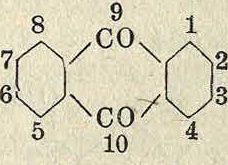
Как видно из таблицы, увеличение числа ОН-групп, за исключением производных галловой кислоты (антрагаллол и руфигаллол), вызывает углубление цвета лаков красителей. Все полиоксиантрахиноны способны давать с к-тами эфиры, из которых борнокислые эфиры обладают характерным для каждого по-лиоксиантрахинона цветом и спектром поглощения, чем и пользуются при контроле производства, чаще всего при проведении Бонна-111 мидта реакции (смотрите), для суждения о ходе реакции. Общие методы получения полиоксиантрахинонов м. б. разбиты следующим образом.
1) Щелочное плавление сульфокислот антрахинона или омыление его галоидопроизводных. Щелочное плавление сульфокислот часто сопровождается и окислительным
14
Т. Э. m. XI.
| Рациональное наименование | Эмпирическое наименование (торг, марка) | Цвет лака с | ||
| СТ | Fe | А1 | ||
| i, 2-диоксиантрахинон | Ализарин | Оливково-корич невый | Фиолетовый | Красный |
| 1, 4- » | Хинизарин | — | — | — |
| 1, 5- » | Антраруфин | — | — | — |
| 1, 8- » | Хризазин | — | — | — |
| 1, 2, з-триоксиантрахинон | Антрагаллол | Желто-корпчи. | — | Желтый |
| 1, 2, 4- » | Пурпурин | Красно-коричн. | — | Алый |
| 1, 2, 5- » | Яркий ализарин-бордо R | Сине-фиолетов. | — | Сине-красный |
| 1, 2, 6- » | Флавопурпурин | — | — | Жплтовато-крас-
ный |
| 1, 2, 7- » | Антрапурпурин | — | — | Желтовато-крас ный |
| 1, 2, 5, 8-тетраоксиантрахинон | Хииализарин | Сине-фиолетов. | — | Синеватый бордо |
| 1, 3, 5, 7- » | Антрахризон | — | — | — |
| 1, 2, 3, 5, 8-пентаоксиантрахинон | Али зарин-цианин 2R | Фиолетовый | — | Красновато-фио летовый |
| 1, 2, 3,5, б, 7-гексаоксиантрахинон | Руфигаллол | Коричневый | — | Коричневато-
желтый |
| 1, 2, 4, 5, б, 8- » | Ализарин-цианин | Синий | — | Фиолетовый |
| 1, 2, 4, 5, 7, 8- » | Ализарин-цианин R | Синий | — | Фиолетовый |
образованием гидроксильн. группы в о-поло-жении к вступающей в реакцию еульфогруп-пе; в тех случаях когда необходимо избежать этого, плавление производят не с едкими щелочами, а с гидратами окисей щелочноземельных металлов, чаще всего с известью. Примером может служить получение ализарина (смотрите) из солей /?-антрахинонсульфо-кислоты при сплавлении ее с щелочами или с известью.
2) Конденсацияпроизводныхфталевого ангидрида с оксипроизводными бензола и замыкание антрахинонного цикла в получившемся при этом оксипроизводном бензоил-бензойной к-ты. Этот способ наиболее часто применяется при получении оксиантрахино-нов с ОН-группами лишь при одном бензольном ядре антрахинонного цикла. Примером подобной конденсации может служить получение хинизарина из фталевого ангидрида и гидрохинона
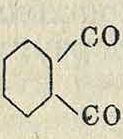
о +
он
/СОч
Сь(Хс0„н(
он он он он
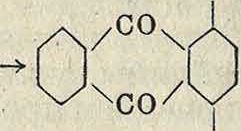
он
3) Конденсация двух молекул производного оксибензойной к-ты, приводящая вначале также к оксибензоилбензойной к-те. В отличие от предыдущего, при этом методе ОН-группы могут находиться и при обоих бензольных ядрах антрахинонного цикла. Примером подобной конденсации может служить получение антрахризона из двух молекул резорцинкарбоновой к-ты
НОч /ч /COOH
он ж
НООС ОН
ноч
,/со
он он
I
но
V
НООС/Ч-МОН
/со
СО
У
ОН
ОН ОН
4) Окисление антрахинона и его производных по реакции Бонна-Шмидта. Окисление м. б. проведено либо действием Мп02 в сернокислой среде либо серным ангидридом или S2Oj веерной к-те в присутствии борной к-ты, азотистой кислоты, серы, селена, брома и т. д. В зависимости от катализаторов, от длительности реакции и температуры ее, при окислении могут получаться различные поли-оксипроизводные, причем ход реакции может контролироваться спектральным исследованием борнокислых эфиров продуктов окисления.
А л и з а р и н—один из наиболее важных синтетич. красителей, вполне идентичный с естественнымализариномизкрапа, корня марены Rubia tinctoria (смотрите выше, К. в естественные); получаетсяон щелочным плавлением jS-антрахинонсульфокислоты, приготовляемой сульфированием антрахинона (о производстве—см. Ализарин). Плавлением технически чистой /?-антрахинонсульфокис-лоты получают чистый ализарин (синеватый), дающий синевато-пунцовые окраски по алюминиевой протраве. При плавлении в тех же условиях 2, 7-дисульфокислоты антрахинона получается антрапурпурин, дающий по алюминиевой протраве более желтоватые оттенки красного цвета. Желтые оттенки дает флавопурпурин, получаемый при щелочном плавлении 2, 6-дисульфокислот антрахинона. Смесь всех трех сульфокислот в различных соотношениях дает ализарин различных марок. А н т р а-руфин и хризазин служат промежуточными продуктами для получения а л и-з а р и н а-с а ф и р о л а; получают их при сплавлении с Са(ОН)2 соответствующих дисульфокислот антрахинона; они не обладают красящими свойствами. Хинизарин, ценный промежуточный продукт для синтеза ряда антрахинонных красителей; он обла-
дает весьма слабыми красящими свойствами и получается либо окислением антрахинона по реакции Бонна-Шмидта либо конденсацией фталевого ангидрида с и-хлорфенолом или гидрохиноном в присутствии серной кислоты, причем одновременно с замыканием антрахинонного кольца происходит и гидролиз с отщеплением хлора. Пурпурин получается при окислении по Бонну-Шмид-ту ализарина или, лучше, хинизарина; мало применим в качестве красителей, служит промежуточным продуктом для получения ализарина сине-черного; сопутствует ализарину в крапе. Антрагаллол получается при конденсации бензойной кислоты с галловой или фталевого ангидрида с пирогаллолом в присутствии серной к-ты. Антрагаллолу может сопутствовать руфигаллол, образующийся при конденсации двух молекул галловой к-ты. Хинализарин, выпускаемый в продажу под названием «ализарин-бордо В», содержит ализариновую группировку при одном бензольном ядре и хин-изариновую при другом; получается окислением по Бонну-Шмидту ализарина или хинизарина. Антрахризон, промежуточный продукт для ряда ализариновых (ант-рахризоновых) красителей; получается конденсацией двух молекул резорцинкарбоно-вой кислоты в присутствии серной кислоты и не обладает, красящими свойствами. Ализарин-цианин различных марок, смесь пента- и гексаоксиантрахинонов, получается по Бонну-Шмидту при действии дымящей серной кислоты на ализарин, хинизарин, ализарин-бордо в присутствии катализаторов (Н3В03, Se, Br, S, HN02); в зависимости от темп-ры, концентрации олеума, катализатора и длительности процесса получаются преимущественно либо пента- либо гекса-оксиантрахиноны. Иногда в реакцию Бонна-Шмидта вводят вместо оксипроизводных антрахинона смесь 1, 5- и 1, 8-динитроантра-хиионов, получая при этом ализарин-цианин WRR; при этом нйтрогруппы служат одновременно и катализаторами и окислителями. К группе оксиантрахинонов принадлежат также и нитро-, амино- и сульфгидрильные производные антрахинона, как наир.: ал и-зарин оранжевый, или 3-нитроализарин, получаемый при нитровании ализарина в ледяной уксусной или в серной кислоте в присутствии борной к-ты, а л и зари н - ц и а ή и н G, или 1, 2, 4-триокси-5,
8-диаминоантрахинон, получаемый при действии 20 %-ного раствора аммиака на 1, 2, 4, 5, 8-пентаоксиантрахинон, и ализарин-маррон, З-амино-1, 2, 4-триоксиантрахи-нон, получаемый при нитровании ализарина в серной к-те и восстановлении полученного при этом З-нитро-1, 2, 4-триоксиантрахино-на.Генетически близко связаны с оксиантра-хинонными красителями и красители типа ализаринового синего, содержащие кроме антрахинонного ядра также и пиридиновое; эти красители получаются из соответствующих аминооксиантрахинонов при действии глицерина в присутствии окислителя и серной кислоты по реакции Скр°у-па. В продажу значительно чаще поступает бисульфитное производное ализаринового синего S, С^НцКОюЭгХаг,
NaOsS—О ОНон
X
с/
I 7 но о i }
I х/
S02Na
к-рое весьма удобно для крашения в силу его растворимости в воде. При нагревании выше 60° бисульфитное производное разлагается и на волокне фиксируется яркий и прочный лак красителя с протравой. Бисуль-фитные производные в силу этого весьмачасто применяются и для иных красителей (например церулеиновых и галловых), когда сам краситель плохо растворим в воде.
1 Б. Сульфированные антрахинон. красители содержат сульфогрупиу, прочно связанную с ядром красителя и остающуюся в молекуле красителя после окраски ткани. Наличие сульфогруппы,повышая кислые свойства красителя, позволяет применять его в качестве собственно кислотного красителя или в качестве хромировочного, если в нем имеются способные к лакообразованию группировки. По способам получения эта группа красителей может быть разбита на два отдела.
1) Антрахинонные красители, содержащие сульфогрупиу в антрахинонном ядре. Простейшим представителем этих красителей является ализариновый красный S, или 3-сульфоализарин, получаемый сульфированием ализарина дымящей серной кислотой при повышенной темп-ре. Аналогичное сульфирование в присутствии ртути, солей ведет к образованию а-сульфопроизводных ализарина с сульфогруппой в положении 5 или 8, открытых М. А. Ильинским и выпущенных в продажу ф-кой Ведекинда под названием э р в е к о-к ислотный ализариновый красный; полиоксиантрахи-ноны, как и диокснантрахиноны, могут давать сульфопроизводные; наибольшее значение имеют аминосульфопроизводные а н-трахризона. Кислотный ализариновый синий GR, 4, 8-диамино-2, 6-дисульфокислота антрахризона, получается сульфированием и нитрованием последнего и восстановлением динитропродукта хлористым оловом в кислой среде. При восстановлении динитропродукта сернистыми щелочами получается кислотный ализариновый зеленый G, отличающийся от предыдущего наличием двух сульфгид-рильных групп вместо двух амидных. Оба эти красящие вещества являются ценными хромировочн. красителями. Если в приведенных выше случаях вместо антрахризона подвергнуть антраруфин сульфированию, нитрованию и дальнейшей обработке, то получаются а л и з а р и н-с а ф и р о л,
1, б-диокси-4, 8-диамино-2, 6-дисульфокисло-та антрахинона, и ализарин-эм е-ральдол, 1,5-диокси-4, 8-дисульфгидро-
2, 6-дисульфокислота антрахинона,—также ценные и широко применяемые кислотные и хромировочные красители.
2) Большое технич. значение имеют антрахинонные красители, содержащие сульфо-группу в боковой ветви. Общий метод их

получения состоит в конденсации аминопроизводных или оксипроизводных антрахи-нона с аминами бензольного ряда, анилином, толуидином и др.; в последние сульфо-группа может быть введена сульфированием, производимым либо до конденсации либо после нее. Эти красители в зависимости от числа сульфированных ариламидных групп бывают производными моносульфомоноарил-аминоантрахинонов или дисульфодиарилди-аминоантрахинонов; общий скелет первых NH-Ar—S03Na
zco 1
и вторых
NH—Ar—S03Na
хСО/
Z00^
χΟΟ/Ιχ
NH—Аг—S03Na
причем могут варьировать как положения сульфированных ариламидных групп, так и различные радикалы и ауксохромы в антра-хинонном ядре и в боковой цепи, что вызывает значительное многообразие этих красителей. Из отдельных представителей следует отметить ализарин-иризоль, моносульфокислоту 1-?г-толиламино-4-окси-антрахинона, получаемый при сульфировании продукта конденсации хинизарина с одной молекулой и-толуидина. В случае избытка и-толуидина и вторая ОН-группа хинизарина замещается остатком и-толуидина и после сульфирования обоих толуидиновых остатков получается ценный ализарин-цианин зелен ы и G. При замене хинизарина хинализарином и обработке последнего двумя молекулами и-толуидина, при последующем сульфировании получается а л и з а р и н-в и р и д и н—протравной и хромировочный краситель. Пурпурин при аналогичной обработке переходит в ализарин с и н е-ч е р н ы й. Несколько особняком стоит а л и з а р и н-р у б и н о л, в котором кроме обычной для этого отдела красителей сульфированной ариламидной группы имеется и пиридоновое кольцо, метилированное при азоте, полученное замыканием из ацетилмонометиламиноантрахинона по следующей схеме /СО
СНз
/ССЧ
4 со ч
N-
-СНз
/СОч
СИ N—СНз
хсо
2 А. Кубовые антрахинонные красители обладают повышенной прочностью к свету, мылу и другим воздействиям; большинство этих красителей получило общее название индантреновых К. в (смотрите Индан-трен). По методам получения и свойствам антрахинонные кубовые" красители делятся на следующие группы.
1) Ациламиноантрахинонные красители, называемые также альголевыми красителями, представляют преимущественно бензоильные производные различных амино-антрахинонов и получаются при конденсации хлористого бензоила с аминоантрахино-
ном в нитробензольный сррде. Хлористый бензоил м. б. заменен бензойной и другими ароматич. к-тами—салициловой, и-метокси-бензойной и др. Простейший представитель этой группы—и ндантреновый желтый WG, 1-бензоиламиноантрахинон. Большое значение имеют полибензоиламиноан-трахиноны: индантреновый крас-н ы и 5GK—1, 4-дибензоилдиаминоантрахи-нон; и ндантреновый желтый GK—· 1, 5-дибензоилдиаминоантрахинон, и ряд их окси- и метоксипроизводных. Из трибензо-илтриаминоантрахинонов следует отметить индантренов ый оранжевый RRK, содержащий эти три группы в положениях 1, 2, 4. Ко второй группе относятся антрахинонные кубовые красители, содержащие антрахинонные ядра, соединенные имидными группами,—т. н. антримидные красители. Получаются они гл. обр. конденсацией аминоантрахинонов с галоидоантра-хинонами в присутствии каталитически действующей мелкораздробленной меди (или полухлористой меди) в нитробензольной или нафталиновой среде. Среднее положение, между первой и второй группами занимают красители, в которых антрахинонные ядра соединены не имидной группой, а карбамидным или имидоянтарным остатками; их получают аналогично альголевым красителям конденсацией двух молекул аминоантрахинона с одной молекулой а или янтарной кислоты; сюда относятся индантрено-вый желтый 3G, 2, 2-диантрахино-нилмочевина, получаемый при конденсации двух молекул /ϊ-аминоантрахинона с мочевиной или ом в нитробензольной среде, и альголевый желтый 3G, 1, 1 сукдинилдиаминоантрахинон, получаемый при конденсации двух молекул а-аминоан-трахинона с одной молекулой янтарной кислоты в нитробензольной среде
/соч,
чСо
—NH—СО—NH-
/С0Ч,
ЧСо индантреновый желтый 3G
/соч
ХСо !
NH—СО—СН2
I
NH—СО—СНз
,zco
хео альголевый желтый 3G
2) У антримидных красителей простейшим представителем является индантре-новыйоранжевый 6RTK, 1,2 -диан-трахинониламин, получаемый при конденсации /J-хлорантрахинона с а-аминоантра-хиноном. Увеличение числа антримидных групп вызывает углубление цвета этих красителей. Так, 2, 6-ди-а-антрахинонилдиами-ноантрахинон, полученный при конденсации 2, 6-дихлорантрахинона с а-аминоантрахи-ноном, представляет собою индантреновый красны и G; его 2, 7-изомер— индантреновый красный R. При введении в эти красители галоидных или метоксильных групп получаются красители еще более глубокого цвета бордо. Триантр-имидные производные, содержащие антра-хиноыиламиновые остатки в двух а-положе-ниях одного и того же антрахинонного кольца, точно так же являются красителями. Таков индантрен бордо, или 1,5-ди-^-антрахинонилдиаминоантрахинон, получаемый при конденсации 1,5-диаминоантра-хинона с двумя молекулами хлорантрахи-нона. Весьма интересен факт, что только те антримидные красители являются кубовыми, в которых имидная группа соединена с ан-трахинонными ядрами в α-положении с одним и в β-положении с другим. Так, 1, 1 -ди-антрахинониламин и 1,5-ди-а-антрахинонил-диаминоантрахинон являются окрашенными веществами, но не имеют характера кубовых К. в Весьма важно и то обстоятельство, что конденсация идет значительно лучше при α-положении амидных групп и при ^-положении галоидн. групп, а не наоборот.
Арильные остатки в аминоантрахинон-ных производных могут быть также фенилй-ными, толильными и нафтильными. Непосредственно подобн. тела не являются ценными К. в.; но если в арильных остатках в о-положении к имидной группе имеются группы, способные к замыканию новых циклов, то такие вещества являются уже ценными кубовыми красителями. Так, наличие группы NH2 может привести кдигидроази-новым производным (I), ОН—к оксазино-вым (II), SH—ктиазиновым (Ш)иСООН— к акридоновым (IV)
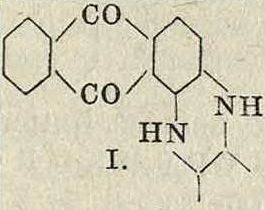
/СОх
хсо/
I NH О !
II.
| О
о —ч |
ч | ГУС% | Ч |
| о о ч | ч
] ΝΗ |
U co | ч
1 NH |
| S 1 | СО 1 | ||
| III. | IV. | Х/Х |
При этом в зависимости от нахождения основной имидной группы в а- либо в /3-положении м. б. получены различные изомеры. Если имидную группу заменить кислородом или серой, то аналогично м. б.получены ксан-тоны (V), тиоксантоны (VI), диоксаны (VII) и дитианы (VIII)
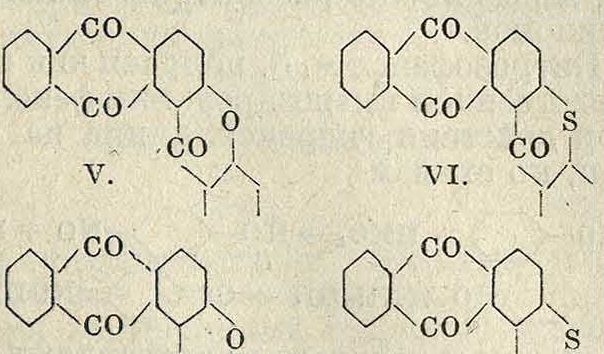
О j S I
УН. Х/Х VIII. Ч
точно так же с возможными изомерами. Остаток, соединенный с гетероциклом, м. б. фе-ниленовым, нафтиленовым и антрахинони-леновым. Общий метод получения этих красителей может заключаться в конденсации по Ульману галоидоантрахинона с производным амина, фенола или тиофенола и в последующем окислительном, водоотнимающем или кислотоотнимающем замыкании гетероцикла. Для нек-рых отдельных представителей существуют и индивидуальные методы синтеза.
2 Б. Многоядерные красители. 1) К содержащим гетероциклические ядра в первую очередь относится ценнейший индант ренов ый синий, который кроме получения из двух молекул амино-бромантрахинона, что представляет только тереотич. интерес, получается также и непосредственным плавлением Д-аминоантра-хинона со щелочью. Известен ряд его метальных, окси- и галоидных производных, обладающих несколько измененными оттенками и повышенной прочностью к хлору. Индантрен синий является дигидро (диаытрахино-нилен)-азином строения
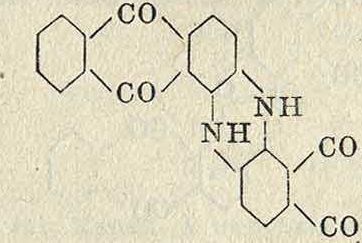
и относится к производным I типа. При более повышенной ί° (310°) щелочного плавления /З-аминоантрахинона получается желтый кубовый краситель индантрен о-в ы и ж е л т ы и G, или флавантрон, следующего строения
в молекуле которого вместо азинового кольца присутствуют два соединенных акридиновых цикла. Красители II и III типа обладающие оксазиновой или тиазиновой группировкой, не получили широкого применения и представляют в настоящее время лишь теоретич. интерес. Производные IV типа, а к р и д о-н ы, получили широкое технич. распространение. Простейший из них получается при конденсации «-хлорантрахинона с антрани-ловой кислотой по Ульману с последующим замыканием акридонового цикла при действии конц. серной к-ты. Аналогичная конденсация ^-аминоантрахинона с о-хлорбен-зойной к-той ведет к образованию изомерного акридона. Большую ценность представляют диакридоны, получаемые конденсацией дихлорантрахинонов с антраниловой кислотой, например индантрен фиолетовый RN, имеющий строение
и получаемый из 1, 5-дихлорантрахинона.
Производные V типа, ксаптоны, пока не имеют широкого применения. Более применимы нек-рые тиоксантоны (VI), например индантрен золотистооранжевый
получаемый конденсацией 1-хлор-2-карбоно-вой кислоты антрахинона с дихлортиофено-лом по Ульману и последующим замыканием тиоксантонового кольца действием конц. серной кислоты. Из производных последних двух типов (VII и VIII) некоторое применение имеет эрвеко желтый, диоксан, следующего строения
получаемый конденсацией двух молекул
1-хлор-2-оксиантрахинона.
2) Весьма большие успехи достигнуты в области антрахинонных сложных карбо-циклических красителей. По строению они отличаются наличием двух сложных циклов—пиренового и периленового следующего строения
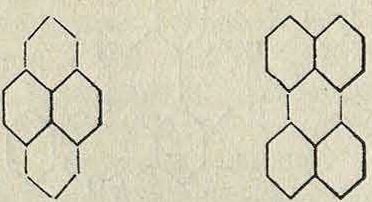
пирен перилен из которых большее значение имеет последний. Пирантрон, выпускаемый в продажу под названием индантрена золотистооранжевого G, имеет следующее строение и содержит п и-реновое кольцо (в схеме заштрихованное). Получается он конденсацией внитробензольной среде, в присутствии порошка меди, двух молекул 1-хлор-2-ме-тилантрахинона в 2, 2-диметил-1, 1 -диацтрахинонил и последующим выделением двух молекул воды с замыканием двух новых ядер, что достигается либо нагреванием до 300—350° либо сплавлением со щелочью. Тот же пирантрон м. б. синтезирован обычным для сложных карбоциклич. соединений методами: получением бензоильных производных и обработ-койпоследнихбезводным А1С13· Так, дибензо-илпирен дает при действии А1С13 пирантрон.
Красители, содержащие перилен о-в о е ядро, приобретают в последнее время все большее значение. Они могут быть получены либо замыканием бензоильных (лучше—галоидо-бензоильных) производных пе-рилена при действии безводного А1С13 либо щелочным плавлением бензантрона и его
производных. Бензантрон, С17Н10О,
000
ч получается при конденсации антрахинона или продуктов его восстановления с глицерином в присутствии серной кислоты или ZnCI2. При щелочном плавлении бензантрон дает виолантрон(1), выпускаемый в продажу прод названием индантрен темно с и н и и ВО, а хлорбензантрон переходит в изовиолантрон (II), выпускаемый под названием индантрен фиолетовый R. Как виолантрон, так и изовиолантрон содержат пери-леновые ядра (заштрихованные на схеме) и получаются конденсацией двух молекул бензантрона. Различие строения виолант-рона и изовиолантрона доказано их синтезом из двух различных дибромдибензбйлпериленов. Аналогично виолантрону получается цианантрон О, или индантрен темносиний ΐ· п. ВТ, если вместо бензантрона взять его хинолиновое производное, получаемое, как и бензантрон, но из /?-аминоантрахинона О /Ч
осо. -оо
|| Чтчгтт, II
о
ГШ2
Ч/Ч^Ч II I N
0 и
Следует отметить, что весьма близкий по конфигурации фенантренхинон о о
/~ч
0-0
не нашел еще применения в синтезе красителей, несмотря на то что запасы фенантрена в каменноугольной смоле весьма велики. Нахождение путей его технич. использования в области К. в.—одна из наиболее важных современных проблем.
Класс II. Хиноноксимные красители.
К ним относятся нитрозо- и нитрокрасители, которые можно рассматривать как оксимы хинонов.
1. Нитрозофенол м. б. получен как при непосредственном нитрозировании фенола, так и при действии гидроксиламина на бензо-хинон, по схемам
I. но-<^> + ηνο2но—<(^>-N0 + н2о
II. 0=0=0 + ΝΗ2°Η -* 0=<Ο=Ν0Η + Н20
Т. о. нитрозокрасители представляют собою таутомерные соединения и по хиноидной классификации зачисляются в класс хинон-оксимов. По хромофорной теории Витта цветность их объясняется: в нитрозо-форме— хромофором -N=0 и ауксохромными группами-ОН или — NR—, а в хиноноксимной форме—хромофорами >С—О и >C=N — R
и ауксохромами, примыкающими к азоту или находящимися кроме того в ядре. По Кенигу, натриевую соль нитрозофенола можно представить следующим образом н н
- + /С=Сч _ + _
0^с( _ + )c^N^:0
%С==С/? S
н н (
! J_____Na_, J
.+
Из нитрозосоединений только те являются красителями, в которых в о-положении к оксимной (=NOH) группе находится ОН-группа, обусловливающая, по Либерману и Костанецкому, протравные свойства красителя. Впрочем и нитрозамины представляют собою основные красители, но весьма малопрочные и практически непригодные.
Из отдельных представителей нитрозокра-сителей следует отметить следующие: эльзасский зеленый, 2, 4-динитрозо-1, 3-резорцин, получается при действии двух молекул азотистой кислоты на Na-резорцинат и дает с железными протравами зеленые, прочные к свету лаки; хромовый лак коричневого цвета мало прочен. Применяются в печати также лаки по медной никелевой и кобальтовой протраве. В и р и д о н, или прочный зеленый, а-нитрозо-/?-наф-тол, получается при действии азотистой кислоты на /S-нафтолят и применяется для печати по железной протраве (дает прочные к свету лаки зеленого цвета) и как реактив в аналитич. химии. В продажу выпускается обычно в виде бисульфитного производного. Кроме того а-нитрозо-/9-нафтол служит промежуточным продуктом для синтеза 1-амино-2-нафтол-4-сульфокислоты нафталина и ряда оксазиновых красителей. Нафтоловый зеленый В, 6-сульфокислота предыдущего, получается при нитрозировании кислоты Шеффера; находит незначительное применение при крашении шерсти в зеленый цвет в виде готового железного лака.
К хиноноксимным красителям с некоторой натяжкой м. б. отнесены и нитрофенолы, к-рые, по Гантчу, могут существовать в аци-форме хиноидного строения. В этой форме нитрогруппу можно представить себе как «окисленную» хиноноксимную группу с пятивалентным азотом, две добавочных валентности которого связаны со вторым атомом кислорода. Так, пикриновая кислота (смотрите ниже) м. б. представлена в виде следующего хинон-оксимного производного
no2 no2
I 1
02N-<^>-OH gHO-S-( )>=0
I
no2
no2
ка.Манчестерский, или Марциуса, желтый, динитро-а-нафтол, применяется для окраски в желтый цвет шелка, мыла, жиров и пищевых продуктов. Нафтоловый желтый S, 7-сульфо-2, 4-д и н и-т р о-а-н a ф т о л,—сульфокислота предыдущего; получается сульфированием а-наф-тола и действием азотной кислоты на смесь его 2, 4-и 2, 7-дисульфо-и 2, 4, 7-трисульфокис-лот и применяется в виде калиевой соли для окраски в желтый цвет шерсти, шелка и пищевых продуктов. Ауранция, гексанитродифениламин, применяется для Окраски шерсти и шелка в незначительных размерах вследствие ядовитости и непрочности; находит применение в фотографии и как чатое вещество. Кислотные свойства ауранции объясняются наличием шести нитрогрупп, лишающих NH-группу основных свойств и придающих ей даже кислый характер, или же принятием для этого соединения таутомерной хиноидной аци-формы o2n no2
02n-O-n=O o2n no2
<
О Me
Класс III. Хинон- и п олухимо нгидразонныэ красители.
К этому классу причисляются: 1) гидр-азонпиразолоновые красители, 2) азокрасители и 3) стильбеновые красители.
1. Первым представителем гидразон-пиразолоновых красителей был тартразин, получаемый действием фе-нилгидразин-и-сульфокислоты на диокси-винную к-ту с образованием дигидразона последней и последующим замыканием пиразолонового кольца по схеме соон
I
со
2H2N—NH-
-SOsNa
СО—СООН
СООН
C=N— NH—<^3>—SO;
С—СООН
Ii /-Λ
N—NH- /_^-S03Na
СООН
Na
Все нитрокрасители представляют собой кислотные красители и являются в то же время чатыми веществами значительной силы. Технически как нитро-, так и ни-трозокрасители получаются непосредственным введением N02- и NO-групп по обычным методам.
2. Из отдельных нитрокрасителей следует отметить следующие. Пикриновая кислота (смотрите), 2, 4, 6-тринитрофенол, применяется для крашения шерсти и особенно шел-
C=N чС-СО7
/N—
SOsNa
N—NH-<^>—S03Na
По этому способу получения тартразин является сульфокислотой фенилгидразона суль-фофенилкетопиразолонкарбоновой кислоты СООН
С—N.
I
С—С
II II О о
^N—<
S03Na
которая (в пиразолоновом кольце) заключает α-дикетонную группировку, свойственную также о-хинонам. Т.о. тартразин следует считать полухинонгидразонным красителем. Но тот же тартразин м. б. получен сочетанием диазобензол-и-сульфокислоты с сульфофе-нилпиразолонкарбоновой кислотой, тауто-
мерным соединением, существующим в ке-тонной и энольной формах соон
С—N.
N—i
~S03Na;
Н2С-С
II
0
соон
1
C=N
ii >N-< —S03Na
ИС=С 7 4—/
I
он соон
!
С—N.
I >
I
он
S03Na + ΝΞΝ—S03H -Cl
соон
I
С—Ν4
• [_ >Ν-<(у—S03Na
С—:С.
ОН
Ν-Ν—ζ У~ SQ3H
На основании этого способа получения тар-тразин приходится считать азокрасителем. Возможно, что именно в таутомерии тартра-зина лежит причина его цветности. Тартра-зин—желтый краситель, отличающийся своим чистым тоном и дающий красивые прочные окраски, особенно по шелку. Кроме тартразина в настоящее время известно довольно большое число пиразолоновых азокрасителей, получаемых б. ч. сочетанием диазосоединений с пиразолоновыми производными, например с фенилметилпиразоло-ном, получающимся в свою очередь действием фенилгидразина на ацетоуксусный эфир с отщеплением а сн3
СО + H2N NiHi—<^>-s-
СН2 - СО ; ОС2Н5
СНз
-N
N-
+ Н20 + С2Н5ОН
СН2—СО
Также и арилиды самого ацетоуксусного эфира служат азокомпонентами (смотрите ниже) при сочетании с диазосоединениями сн2 сн3 сн3
СО С=0 С“0
-fCl-N=NR I _ __ ___ ii I
сн2
CONHAr
СН—N—NR
I
CONHAr
C=N—NHR CONHAr
2. Второй группой красителей, причисляемых к хинонгидразонному классу, являются азокрасители. Общий способ получения их—сочетание ароматич. диазосоединений с какими-либо азокомпонентами, то есть аминами или фенолами бензольного или нафталинового ряда. В нек-рых случаях идентичные с азокрасителями соединения получаются действием фенилгидразина или его производных на хиноны. Так, бен-зол-азо-^-нафтол м. б. получен либо (а) конденсацией фенилгидразина с /?-нафтохино-
ном либо (Ь) сочетанием диазониевой соли бензола с р-нафтолом, по схемам о
(а)
( У—NH- NH2 + 0=<
NH—N=<
О
ОН
I
(Ь) ^>-νξν+
Cl
Возможно, что в молекулах азокрасителей, как и в пиразолоновых, имеется равновесие между азоформой (Ь) и гидразонной формой (а). Второй способ получения (Ь) является наиболее доступным технически, в силу чего лишь им и пользуются при синтезе азокрасителей в фабричном масштабе.
Первые азокрасители были получены П. Гриссом, открывшим реакцию диазотирования. Каро, Витт и Ненцкий подметили в образовании их ряд закономерностей, что позволило произвести синтез значительного числа этих К. в Техническая несложность получения и возможность из сравнительно небольшого числа аминов, фенолов, их сульфонроизводных и карбоновых кислот синтезировать весьма многочисленные разнообразные по свойствам и оттенкам азокрасители поставили эти последние на одно из первых мест среди К. в Наблюдавшаяся вначале непрочность азокра-еителей к мылу, свету и тому подобное. препятствовала конкуренции их с более прочными кубовыми и сернистыми красителями; тем не менее позднейшие исследования указали пути синтеза светопрочных азокрасителей и тем самым окончательно укрепили их значение.
Промежуточными продуктами для синтеза азокрасителей служат различные амины, являющиеся диазокомпонентами азокрасителя, и различные производные аминов и фенолов, являющиеся его азокомпонентом. Первые- подвергаются реакции диазотирования (смотрите Диазосоединения); получившаяся диазониевая соль вводится в реакцию сочетания с азосоставляющей, причем эта реакция в зависимости от свойств взятых веществ может вестись либо в слабокислой минеральной, либо в уксуснокислой, либо в нейтральной, либо в слабощелочной среде. При этом диазониевая соль переходит сначала в синдиазосоединение, а последнее сочетается с азосоставляющей по след, схеме:
R—ΝΞΝ -► R—N=N—ОН + R, (аукс.) ->
С1
R—N =N—Ri (аукс.) + Н20
Достигается это либо прибавлением уксуснокислого натрия к раствору диазониевой соли либо вливанием диазониевой соли в ще-лочный раствор азосоставляющей, причем концентрация кислоты и щелочи варьирует в зависимости от взятых исходных продуктов. В азосоставляющих сочетание происходит преимущественно в и-положении к ауксо-хрому и—лишь в том случае, когда последнее замещено каким-либо радикалом,—в о-положении к ауксохрому. В нафталиновых производных сочетание происходит в положении 4—при нахождении ауксохрома в положении 1 (или а), и в положении 1—при наличии ауксохрома в положении 2 (или β). Но если в α-производных нафталина поло-
жение 3 занято сульфогруппой, то азосочетание идет в положении 2, а не 4, т. к. последнему припятствует сульфогруппа (положения 2 и 3 в нафталиновом ядре не являются о-положениями в отличие от положения 3 и 4). Так, к-та Фрейнда, 1, 3, 6-нафтиламин-дисульфокислота
nh2
H03S-1
SO»H
вступает в реакцию азосочетания своим положением 2 (отмеченным звездочкой), а не 4. Кроме того и среда, в которой ведется сочетание, играет существенную роль. Так, если азосоставляющей является какое-либо производное аминонафтола, то ориентирующим началом в кислой среде является аминогруппа, а в щелочной—оксигруппа. Так, Н-кис-лота
НО NH;
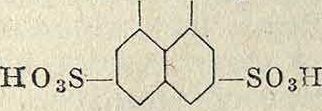
1,8-аминонафтол-3,6-дисульфокислота, вступает в азосочет.лше в кислой среде в о-поло-жении к NH2-rpynne, а в щелочной среде—в о-положении к ОН-группе. Очевидной причиной этого является то обстоятельство, что все азосоставляющие реагируют в хиноль-ной форме и в приведенном выше примере к хинольной перегруппировке способно в кислой среде правое нафталиновое ядро но NH НС1
I II
jio g_1 Н ГФ
so3h
а в щелочной среде—левое о NH.
нч
Н
H03S-
-S03H
реагируя как кетоэнольный таутомер.
По своему технич. применению азокрасители относятся в зависимости от наличия в них тех или. иных групп к кислотным, основным и солевым красителям. Так, все азокрасители, содержащие сульфогруппы, являются кислотными и способны окрашивать животное волокно, вступая в химич. взаимодействие с последним. Если в азокрасителе имеется способная к лакообразованию группировка (правило Либермана и Костанец-кого), то эти красители могут служить протравными. К- последним относятся и мета-хромовые красители, которые содержат часто в виде диазокомпонента пикраминовую кислоту; неолановые красители, которые содержат уже в самом красителе металл, служащий для образования лаков, и эриохромовые красители, производные преимущественно 1-амино-2-нафтол-4-сульфокислоты. Наличие в числе азокомпонентов легко окисляющихся аминов и оксинафталинов придает этим красителям свойства хромировочных. Примерами всех трех типов могут служить следующие красители: пунцовый 2R (кислотный краситель)
СН3 НО S03Na
! I 1
H3C_<(Z)~N=N~
S03Na
ализариновый желтый G (протрав-ный краситель)
<^>-n=n—<^>—он
no2 соон хромотроп 10В (хромировочный краситель)
но он
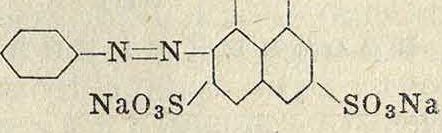
Азокрасители, содержащие амидные группы и лишенные кислых групп, обладают в большинстве основными свойствами и поступают в продажу в виде солей с минеральными (преимущественно соляной) к-тами, как наир, хризоидин (основной краситель)
^ ^>-n=n-<( )—nh2 · HCl
I
NH,
Ряд красителей, преимущественно производных солянокислого ж-аминофенилтри-метиламмония
H2N-0-N(CHs)3C1
обладают одновременно субстантивными и основными свойствами, служат для окраски смешанных товаров и называются я н у с о-в ы м и красителями, как например, янусовый красный В он I
-N=N—<^>-N=N-<^>
I !
СН3 N(CH3)3C1
Те же янусовые красители получаются при сочетании диазосафранина с диметиланмм-ном. Соляные, или субстантивные, свойства азокрасителей зависят от общего строения их молекулы. Для придания азокрасителям, субстантивных свойств необходимо соблюсти одно из следующих трех условий. Центральная диазосоставляющая азокрасителя: должна представлять собою симметричный диамин,наир, бензидин, и-фенилендиамин,то-лидин, дианизидин, диаминостильбен или их производные. Кроме подобных оснований могут применяться и сложные симметричные· продукты конденсации а с диаминами и дихлоргетероциклов с диаминами, точно также придающие красителям субстантивные свойства. Подобные азокрасители,независимо от конечных азокомпонентов, обладают субстантивными свойствами. Если центральный азокомпонент представляет собою· сложное полиметиновое производное (исследования Рупе и Порай-Кошица), то краситель точно так же, независимо от конечного компонента, имеет субстантивные свойства. В сложи, полиазокрасителях наличие в виде конечного компонента 1-кислоты или у-ки~ слоты также придает азокрасителям субстантивные свойства. Все три типа субстан-

тивных красителей могут быть иллюстрированы следующими примерами:
конго красный
nh2
QQ-N=w-CK>
nh2
1
-N=N-
S03Na
S03Na
HCl-NH2-<^])— N=N-<(^>-CH=CH-CO-CH
NHj
HOI
• NHi-QHfcN-QH ϊ!η2
CH
яркий прочный синий В
SOaNa
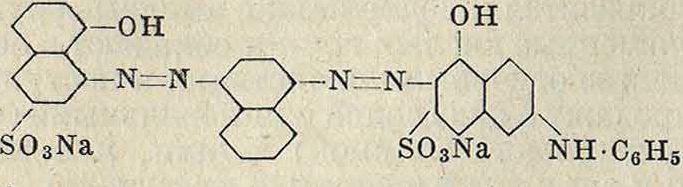
К азокрасителям относится и целый ряд нерастворимых красителей, получаемых из составных частей непосредственно на волокне и называемых л е д я н ы м и, т. к. получение их часто требует охлаждения льдом. Простейшим представителем их является пар a-к расный, получаемый на волокне купелированием диазотированного и-нит-ранилина с /S-нафтолом он
no2
Ткань пропитывают раствором /3-нафтолята натрия и после сушки проводят на холоду через раствор диазотированного п-нитрани-лина. Если вместо последнего взять а-наф-тиламин, то получается окраска цвета бордо, или «кардинал»; с бензидином получается коричневый цвет, с дианизидином—фиолетовосиний и т. д. Хороший коричневый цвет получается, если вместо β-нафтола взять хризо-идин и сочетать его на волокне с и-нитродиа-зобензолом. Число ледяных красителей сильно возросло с введением в качестве азокомпонентов т. н. нафтолов AS, которые являются ариламидами 2, 3-океинафтойной к-ты оо/ОН
VVXCO-NHAr
и ряда оснований к ним, дающих при различных сочетаниях значительное разнообразие очень прочных и красивых оттенков (смотрите Крашение и Нафтолы).
К ледяным красителям близки л и т о л е-вые красители, служащие красящим началом ряда лаков и получаемые преимущественно при сочетании диазокомпонента с jS-нафтолом:
.литолевый прочный алый PRN
он н 3ο-<(3~Ν=Ν-(Ζ)>
νο2
литолевый красный ЗВ сн3 но соон
I I 1
CI-0-N=N-
I
S03Na
литолевый красный R
S03H он
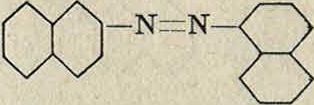
Нерастворимы также и азокрасители для лаков, выпущенные в продажу под названием Hansa, большая часть которых представляет продукты сочетания диазопроизводных о-нитранилина и его гомологов с производными арилидов ацетоуксусной кислоты [4]. Hansa желтый G
СН3—СО-СН—CO-NH-CeHs
СН3
и Hansa желтый 10G
СН3—СО—СН—СО—NH—СвН4—01(о-)

С1
К азокрасителям относятся и красители для ацетатного шелка, ионамины (смотрите), например
<^^-N=N—^^>-NH-CH2-S03Na
По методам получения азокрасители м. б. разделены на моноазокрасители и полиазокрасители (к последним относятся также и дисазокрасители из диаминов). Если обозначить азокомпонент через А, диазокомпонент через D, стрелкой -> направление сочетания D с А и индексом (а)—диазотируемую часть, то общая классификация азокрасителей м. б. выражена следующей схемой.
I. Моноазокрасители -у А.
II. Полиазокрасители:
а) Дисазокрасители типа A А.
б) Дисазокрасители типа D" -> А” -* А.
в) Дисазокрасители типа -у A <-°D.
г) Трисазокрасители, получаемые из трех предыдущих типов либо диазотированием конечного компонента и сочетанием с азокомпонентом либо сочетанием с заранее приготовленным диазокомпонентом, что дает следующие тины:
A <-<*Dd-s· А^ -* Ай А «-<>Г>а->· A -f-^D А^ Ad-> A A -e-^D -> A «- -> A
D<>-*A -s-<>D <-0D.
д) Тетракисазокрасители, получаемые из трисазо-красителей аналогично предыдущему. е) Пентакисазокрасители, весьма редко применяемые.
Технич. осуществление синтеза азокрасителей не представляет трудностей. Аппаратура весьма несложна и состоит преимущественно из деревянных чанов, часто значительной емкости, снабженных мощными мешалками, и из фильтрующих установок. Наибольшую трудность представляет приготовление промежуточных продуктов—диазо-и азокомпонентов. Для удобства работы всю аппаратуру для азокрасителей располагают по ярусной системе, чтобы использовать по возможности принцип самотека. Азо-корпуса красочных фабрик должен быть снабжены холодильными установками или льдоделатель-ными машинами. Правильность ведения процесса получения азокрасителей в значительной степени зависит от соблюдения i°-Hbix условий, концентрации кислоты или щелочи, скорости приливания ингредиентов и тому подобное. Обыкновенно заранее в деревянном чане, помещенном на верхнем ярусе, диазотируют амин, служащий диазосоставляющей, и приливают диазораствор (или диазосуспензию) к азосоставляющей, помещенной в деревянном чане ярусом ниже. Раствор азосоставляющей в зависимости от ее свойства может иметь либо слабокислую, либо нейтральную, либо слабощелочную реакцию. Контроль азосочетания производится качественным определением азо- и диазосоставляющей, для чего капля раствора на фильтровальной бумаге приводится в соприкосновение либо с каплей раствора диазо-к-нитранилина или же другого амина либо с каплей раствора Н-кислоты или R-кислоты. Появление окрашенной полосы на месте соприкосновения с первым раствором указывает на избыток азосоставляющей, со вторым же—на избыток диазосоставляющей. Отсутствие окрашенных полос служит признаком конца сочетания, после чего азокраситель м. б. высолен из раствора, отфильтрован, высушен и поставлен на тип.
I.Моноазокрасители. К моноазокрасителям основного характера относится аминоазобензол, получаемый либо сочетанием диазониевой соли бензола с анилином (анилин -> анилин) и последующей перегруппировкой образующегося ди-азоаминобензола либо непосредственно действием NaN02 на избыток раствора солянокислого анилина. Вследствие нерастворимости в воде аминоазобензол имеет лишь незначительное применение как овой краситель; он применяется гл. обр. для получения и-фенилендиамина (восстановление красителя). Продукт сульфирования аминоаза-бензола, прочный желтый, является кислотным красителем. Хризоидин (анилин -» ж-фенилендиамиы), простейший основной краситель, получается сочетанием диазониевой соли бензола с ж-фениленди-амином и находит вследствие своей непрочности лишь некоторое применение в печати и крашении гл. обр. как азокомпонент при ледяном крашении. Жировой желтый (анилин -> диметиланилин) получается сочетанием диазониевой соли бензола с диметил-анилином и служит гл. обр. для подкраски жиров и масел.
Кислотные моноазокрасители содержат сульфогруппы либо при диазосоставляющей, либо при азосоставляющей, либо при обеих составляющих. К ним относятся оранжево-желтые красители, получаемые сочетанием диазосульфаниловой или диазомета-ниловой к-т с различными аминами и фено лами, например: тропеолин, или оранж I (сульфаниловая к-та -> α-нафтол), оранж II (сульфаниловая к-та^ Д-нафтол), оранж III, или метилоранж (сульфаниловая к-та -> диметиланилин), оранж IV (сульфаниловая к-та -> дифениламин), метаниловый желтый (метаниловая к-та -> дифениламин), прочный красный (нафтионо-вая к-та-> β-нафтол) и многие другие, получаемые сочетанием различных диазотиро-ванных аминосульфокислот с различными аминами и фенолами. К ним же принадлежат и оранжево-красные красители, получаемые сочетанием диазотированных аминов с различными сульфокислотами нафтолов и наф-тиламинов: оранж G (анилин -*· G-к-та), пунцовый G (анилин -> R-к-та), хромо т р о π 6В (анилин -»хро отроповая к-та), азофуксин (анилин ^Н-к-та), пунцовый 2R (ж-ксилидин -> R-к-та), бордо (В, BL, G, R, R extra) (α-нафтиламин -> R-к-та),кристаллический пунцовый (α-нафтиламин -> G-к-та) и другие. Сюда же относятся сине-красные красители, получаемые сочетанием различных диазотированных аминосульфокислот с различными сульфокислотами аминов и фенолов: к а р м у а-з и н (нафтионовая к-та-о-к-та Невиль-Вин-тера), хромотроп 8В (нафтионовая к-та -> хромотроповая к-та) и др.
Кислотные моноазокрасители, содержащие карбоксильные группы (в большинстве производные салициловой кислоты), обладают протравным характером. К числу их относятся: ализарин ж е л т ы и G (ж-нитр-анилин -* салициловая к-та); хром прочный желтый GG (а-нафтиламин-6-суль-фокислота -> салициловая к-та) и многие др.
И. Ди сазокрасители. а)ТипА^Л^А. К производным этого типа относятся по преимуществу субстантивные т е т р азокрасители, получаемые сочетанием те-тразотированного (двукратно диазотирован-ного) диамина, как бензидин, толуидин, дианизидин, диаминостильбен и тому подобное., с различными аминами, фенолами или их сульфоновыми и карбоновыми к-тами. При этом тетразокрасители могут либо иметь вполне симметричное строение либо содержать различные азокомпоненты. Технически последнее осуществляется благодаря свойству первой диазогруппы тетразотированного основания вступать в реакцию сочетания значительно быстрее, чем вторая диазогруппа. Число подобных тетразокрасителей весьма велико. Из них наиболее важны следующие:
хризофенин диаминостильбендисульфокислота ^ фшетол получаемый этилированием яркого желтого из фенола;
конго красный беннитшн ·* нафтионовая к-та оензидин ^ нафтионовая к-та джазочерный
; Н-к-та (щелочное сочетание)
) д м. у-к-та (щелочное сочетание) б ензокоричневый МС
беттчипин л салициловая к-та
д у-к-та (щелочное сочетание) бензопурпурин 4В
толипин ^ нафтионовая к-та толидин ч нафтионовая к-та бензоазурин G
к-та Невиль-Винтера дианизидин ^ к_та Невиль-Винтера
К этому же типу красителей относится б и с м а р к коричневый, или в е з у в и н,
у’ .«-фенилендиамин л-фенилендиамин ^ .и-фенилендиамин основной дисазокраситель, не имеющий субстантивных свойств.
Перечисленные выше представители дисазокрасителей дают окраски от желтого до черного цвета. Различные сочетания применяемых тетразокомпонентов и азокомпонентов дают субстантивные красители почти всех цветов и оттенков. Существенным недостатком их является непрочность к мытью и главным образом к свету. б) Тип Dd->Ad-^A. К. в этого типа в большинстве представляют кислотные красители и м. б. получены обычным путем из моноазокрасителей, содержащих способную к диазотированию аминогруппу. Важнейшими их представителями являются: б и б р и х-с к и и алы й—первый дисазокраситель, открытый Ненцким в 1878 г. и получаемый сочетанием диазотированной дисульфокислоты аминоазобензола с /S-нафтолом; кро-ц е и новый алый (сульфаниловая к-та-* -*· анилин -* кроцеиновая кислота); с у к о н-ный красный (о-толуидин -> о-толуи-дин -* R-к-та); прочный фиолетовый R (сульфаниловая к-та -* а-нафтил-амин -> кислота Шефера); нафтоловый черный В (амино-G-K-Ta -* α-нафтиламин -> -> R-к-та); сульфонцианинЗИ(метани-ловая к-та а-нафтиламин -* толилперики-слота). Увеличение числа нафталиновых молекул вызывает углубление цвета красителя. Число различных кислотных дисазокра-сителей этого типа весьма велико. в) Тип Dd -*· А+- dD. Получение этихкраси-телей м. б. представлено как результат азосочетания диазониевой соли с готовым моноазокрасителем, что роднит этот тип красителей с предыдущим. К числу этих красителей относятся: кислотный коричневый R (анилин -> ж-фенилендиамин «-
нафтионовая кислота). нафтоловый сине-черный
„ (щелочное сочет.) анилин и-к-тд <- (кислое сочет.) паранитранплин и ряд других. г) Трисазокрасителим. б. получены из различных дисазокрасителей: либо диазотированием аминогруппы последних и сочетанием с азокомпонентом либо сочетанием этих дисазокрасителей с диазокомпонентом. Точно так же м. б. получены путем постепенного накопления азогрупп тетракис- и пентакисазокрасители. Часто введение лишней азогруппы производится уже на волокне, для чего окрашенная ткань либо подвергается действию азотистой кислоты и сочетанию с амином или фенолом либо обрабатывается диазотированным и-нитрани-лином. Подобная вторичная обработка тканей, окрашенных азокрасителями (преимущественно субстантивными), вызывает увеличение прочности окрасок и углубление цвета. Из полиазокрасителей, число которых весьма велико, отметим: анил-черный RW, или непосредственный глубокий черный RW, или Колумбия черный RW
,» льтолуилендиамин оензидин ^ (кислое сочетание) Н-кислота <- анилин
(щелочное сочетание)
чикаго-красители, содержащие в своем составе чикаго-кислоту (смотрите Промежуточные продукты синтеза красителей.
III.В группе стильбеновых красителей, получающихся путем внутримолекулярной перегруппировки производных п-нитро-о-сульфокислоты при нагревании их с едким натром, также предполагают наличие замкнутых азогруппировок. Так например, солнечный желтый из и-нитро-о-сульфокислоты представляет собою, по иследованиям Грина и Валя, следующее соединение
S03Na S03Na
CH-O-N N—<( СН
и ><×у сн——N—N— у—сн
ч4
S03Na 0 S03Na
Возможно однако, что красители этой группы представляют собой смесь азо-, азокси-соединений и азометиновых производных. Красители эти отличаются субстантивными свойствами, то есть способностью окрашивать без протравы растительное волокно. Они известны под названиями солнечных желтых (разных марок), хлорантиновых желтых, микадо-желтых, дианиловых желтых; при окислении из них получаются также желтые красители («хлораминовые», «полифени-ловые» и др.), отличающиеся большой прочностью к хлору. Принимая для этих К. в хиноидное строение, можно изобразить например солнечный желтый следующей формулой
S03Na S03Na
CH=<^>=N-N=r<^>=CH
СН:
-О- χ-Ν о
I
—сн
S03Na
Ч
S03Na
В такой форме он может считаться производным дигидразона диметиндихинона, О : С6Н4: СН · СН : С„Н4 : О.
Класс IV. Хинонимидные и хинондиимидные красители.
Хинонимидные красители отличаются наличием в них хинонного цикла, в котором по крайней мере один атом кислорода замещен имидным остатком NH; хинонимидные красители представляют собою производные хинонимида 0=<( )>=NH и хинондиимида
NH=<^>—NH. По своему строению хинонимидные красители могут быть отнесены к двум основным группам. Первую из них составляют индамины, инданилины и индофенолы (смотрите), представляющие арильные замещенные п- (или о-) хинониминов, построенные по следующим основным типам индофенолы H0-O-N-O0 инданилины H2N—^>—N=<^ /=0 индамины H2N-O—*
Если в индаминах или индафенолах в о-по-ложении к имидному азоту содержится группа NH2, ОН или SH, то они способны при окислении замыкать гетероциклич. ядра и переходить в хиыонимидные красители второй группы—азины с азониями, оксазины и тиазины.
1. Индамины и индофенолы представляют собою гл. обр.синие вещества, .которые дают зеленого цвета соли, разлагающиеся при действии минеральных к-т.
Из отдельных представителей их необходимо отметить следующие. Фенилено-в ы 1 сини й—простейший индамин
N—<( ^)=NH или
Н С1 Н Н
nh2
получаемый совместным окислением молекулярной смеси и-фенилендиамина и солянокислого анилина или умеренным окислением диаминодифениламина; является промежуточным продуктом при синтезе фено-сафранина. Биндшедлеровский зеленый, тетраметильное производное предыдущего, получается конденсациейп-ни-трозодиметиланилина с солянокислым диме-тиланилином или окислением молекулярной смеси n-аминодиметиланилина с солянокислым диметиланилином; он является промежуточным продуктом при синтезе ряда азиновых и тиазиновых красителей. Т о л у-иленовый синий, продукт конденсации и-нитрозодиметиланилина с ж-толу-илендиамином
<CH3)SN
N—он
+
С1
h2n/
СНз
NHa
(СН3)аГр
X
и
Cl
h2n
СНз
NHS
или совместного окисления n-аминодиметил-анилина с солянокислым м-толуилендиами-ном, может быть применяем в качестве основного красителя, но вследствие своей непрочности практич. значения не имеет; при окислении переходит в азин (толуиленовый красный—смотрите ниже). Индофенол в паст е—·
Ас
(CH3)2N=<^>=N—
- (CH3)aN-

он;
—о продукт конденсации м-нитрозодиметил-анилина с α-нафтолом; нерастворим в воде; применяется как суррогат индиго, так как дает при действии гидросульфита куб, легко переходящий при окислении воздухом в синий индофенол; выкраски из индофенольного куба непрочны. Целый ряд индофенолов и их лейкопроизводных синтезируется для получения сернистых красителей (смотрите ниже).
2. Хинонимидные красители с гетероци-клич. ядрами относятся к следующим трем типам: а) азиновые красящие вещества и азо-
ниевые красящие вещества (смотрите), содержащие азиновое ядро (I), б) оксазиновые красители, содержащие оксазиновое ядро (II), и в) тиа-зиновые, содержащие тиазиновое ядро (III)
w
Cl
II.
^х
w
Cl
III.
При наличии в этих циклах ауксохромных групп получаются красители, которым можно приписать и те-хиноидное строение. Если пронумеровать атомы в молекуле азина так, как показано в формуле (I), то становится возможным рационально именовать все подобные красители, отбросив устаревшие эмпи-рическ. термины, как эйродины, эйродолы, апосафранины, сафранины, индулины, роз-индулины и тому подобное. Так, наиболее употребительный краситель этого ряда, сафранин Т,
НзС Х ^м Х /СНз
! xci
м. б. назван солянокислым мезофенил-2, 2-диметил-3, 3 -диаминодифеназонием.
Общие методы получения азиновых и азо-ниевых красителей следующие: 1) конденсация о-диаминов с о-хинонами; 2) окисление индаминов или индофенолов, содержащих в о-положении к имидному азоту аминогруппу или фениламиногруппу; 3) совместное окисление индаминов или индофенолов с аминами; 4) конденсация азосоединения с аминами или фенолами. Первый метод синтеза азинов и азониев не имеет широкого применения. Наиболее характерным примером его является получение ф л а вин-дул и н а (солянокислого мезофенилфен-антрфеназония)из фенантренхинона и о-ами-нодифениламина по схеме
. Η2Ν-Ο ΡγΝχΛ
+ ΗΝ^Η -► Y/Vn/X I XC1 kj I XC1
Иллюстрацией второго метода мойсет служить получение толуиленового красного (2-метил-З-амино-З -диметиламиноди-феназина) из толуиленового синего, по схеме
ЧС1
(CH3)2N
| |Х%( | /ч/CEs |
| H2N/ | x^4nh2 |
| /V | /CH3 |
| 4N/v | 4NHa-HCl |
Третий метод имеет весьма широкое применение, причем часто самое получение инд-амина или индофенола производят одновременно с получением красителя, подвергая окислению смесь трех молекул аминов. Так, сафранин Т получается окислением смеси и-толуилендиамина с о-толуидином
ϊϊϋ
и анилином; промежуточным продуктом при этом является индамин, который при дальнейшем окислении с анилином, переходит в сафранин
HjC^/s/NHj /СНз
Г J + Г} -»
H2N/4^ 4^XNHa
HN
nh2
nh2-hci
H3C
H2N
j XC1
Четвертый метод стоит в тесной связи с получением индаминов из нитрозосоединений. Если представить азосоединение в хинон-гидразонной форме, а нитрозопроизводные— в хиноноксимной, то обе реакции изобразятся аналогично
(a) R=<(^)=N-OH + <^~)-Ri ->
-* R=z<^>=N-<^)-R1 + Н20
(b) Rr-<^>=N-NH-<^> + <^>-Ri ->
-> R^<^)=N-<3>-Ri + H2N-<(^)>
В дальнейшем полученный индамин или индофенол может вступать в реакцию с амином по третьему методу и переходить в азо-ниевый краситель или же при наличии NH2группы в о-положении переходить по второму методу в азиновый краситель.
При проведении реакции по этой схеме необходимо конденсировать или о-аминоазо-соединение с амином или и-аминоазосоединение с м-диамином, чтобы полученный индамин содержал амидную группу в о-положении к имидному азоту. Аналогичным путем получаются и азониевые красители, если кроме азосоединения и амина в реакции примет участие и третья молекула амина, но в этом случае наличие аминогруппы в о-положении является излишним. Так, ф е-нилрозиндулин, солянокислый ме-зофенил-5-фениламинонафтофеназоний, получается при взаимодействии бензолазо-а-нафтиламина с анилином и солянокислым анилином по схеме
NH
I I · /V"
ян
ϊ-ΝΗ-<^> + <^>“ΝΗ2
I i
NH
nh2
I I jj
nh2
I
-* NH
X:N/
0 0
(Уо
и при этом сопровождается выделением NH3Наблюдаемое при этом фенилирование имид-ных групп является обычным для подобных реакций и приводит часто к полифенилами-ноазиновым и -азониевым красителям. Тео-ретич. интерес представляет также метод получения азониевых красителей при взаимодействии хинондихлордииминов с аминами по В. Г. Шапошникову.
Азиновые и азониевые красители в большинстве случаев обладают основными свойствами; лишь нек-рые из них (имеющие суль-фогруппы) обладают кислыми свойствами и применяются для крашения шерсти и шелка. Из отдельных представителей следует отметить следующие. Флавиндулин, солянокислый мезофенилфенофенантразоний, получаемый из фенантренхинона и о-ами-нодифениламина; мало применимый желтооранжевый краситель. РозиндулинИ, натриевая соль мезофенил-2-сульфо-4-окси-нафтофеназония, к-рый получается конденсацией нитрозо-1-нафтол-6-сульфокислоты с анилином и последующим окислением полученного индофенола с солянокислым анилином; в незначительных размерах он применяется в крашении шерсти и шелка в алокрасный цвет. Нейтральный голубой, солянокислый мезофенил-3-диме-тиламинофеннафтазоний, получаемый конденсацией нитрозодиметиланилина с β-im-фтиламином; основной краситель. Сафра-’ н и н Т, солянокислый мезофенил-2, 2-диметил-3, 3-диаминодифеназоний,один из наиболее употребительных азониевых красителей (получение его приведено выше). М е-т иловый гелиотропов ый О, солянокислый мезофенил-2-метил-З-амино-З -фениламинодифеназоний, получаемый при совместном окислении п-аминодифенилами-на с о-толуидином и дальнейшем окислении полученного индамина с анилином. М о в е-и н, сернокислый мезо-и-толил-2, 2-диме-тил-З-амино-З-фениламинодифеназоний, первый краситель, открытый В. Г. Перкином в 1856 году, получаемый с незначительными выходами при фуксиновом плаве анилина, содержащего о- и те-толуидины. Применяется главы, обр. для печатания почтовых марок в Англии. Магдала красный, солянокислый мезо-а-нафтил-4-аминодина-фтазоний, получаемый в смеси с симметричным диаминопродуктом при нагревании α-аминоазонафталина с α-нафтиламином и находящий незначительное применение при крашении шелка и приготовлении чернил. Индулиновый синий, солянокислый мезофенил-2, З-дифенилдиамино-З-ами-ноцифеназоний, родоначальник группы ин-дулинов, получаемый сплавлением амино-азобензола с анилином. При увеличении числа фенилированных аминогрупп получаются настоящие индулииы (смотрите). Индулины в виде солянокислых солей представляют основные растворимые в е продукты. Жирнокислые соли их оснований растворимы в жирах и называются жировыми и ндулинами. Раствор солянокислых овых красителей в анетине (ацетильное производное глицерина) служит для печатания на растительных волокнах—под названием ацетинового голубо-
г о; натриевые же соли сульфокислот инду-линов представляют собою растворимые в воде продукты. Близки к индулинам по своему строению и нигрозины, продукты окисления анилина нитробензолом в присутствии железных опилок.
К хинонимидным азониевым красителям относятся, по Грину, и черный анилин (смотрите), образующийся на растительных волокнах и на шелке окислением солянокислого анилина. Значение азиновых и азониевых красителей вследствие их непрочности постепенно уменьшается, и лишь индулины, нигрозины и черный анилин пользуются широким распространением.
Оксазиновые красители представляют производные солянокислого окс-азония (азоксония)
С1
и м. б. получены, аналогично азоновым красителям, из индаминов и индофенолов, содержащих в о-положении к азоту гетероцикла ОН-группу. Обычно получение инд-амина и индофенола и замыкание кольца в красителе сводятся к одной операции, которую проводят либо совместным окислением диамина или аминофенола с полифенолом или аминофенолом либо конденсацией нитрозопродукта с фенольными производными, причем самый нитрозопродукт, взятый в избытке, играет роль окислителя. Так, мельдола голубой, солянокислый 3-диметиламинофеннафтазоксоний, получается конденсацией и-нитрозодиметил-анилина с /3-нафтолом по схеме
N—ОН
N(CH3)a
Cl
(CH3)2N:
/.N.
/V + I I
он
Cl
он
/44W
N(CH3)2 1
С1
η
Наибольшее значение имеет группа галловых красителей, ярких и прочных протравных красителей, родоначальником которых является галлоцианин. Из отдельных представителей необходимо отметить следующие. Резоруфин, солянокислый 3, З-диоксидифеназоксоний, получаемый из мононитрозорезорцина и резорцина; применение имеет его тетрабромпро-изводное. Капри голубой, солянокислый 2-метил-З, З-тетраметилдиаминоди-•феназоксоний, к-рый получается из нитрозо-диметиланилина и диметил-м-аминокрезо-ла. Мельдола голубо й—смотрите выше. Нильский голубой, сернокислая соль З-диэтиламино-5 -аминофеннафтазоксо-ния, получается из нитрозодиэтил-лг-амино-фенола и α-нафтиламина. Галлоцианин, 3-диметил-амино-1-карбокси-3, 4-
диоксидифеназоксоний, а также и ближайшие его производные—см. Галлоцианины.
К азиновым и оксазиновым красителям следует отнести повидимому и ряд красителей для кожи и меха, получаемых на последних окислением различных промежуточных продуктов—аминов и аминофенолов, которые поступают в продажу под названиями урсолов, фурреинов, фуксаминов или накокрасителей. Они дают различные оттенки—от желто-коричневого до черного, причем окислению могут подвергаться как отдельные промежуточные продукты (анилин, w-аминофенол, о-аминофенол, аминоанизол, ж-аминофенол, w-диаминодифениламин, w-фе-нилендиамин), так и их смеси. Красители, которые образуются при окислении этих веществ на животном волокне, имеют, согласно исследованиям Эрдмана [“], хинонимид-ное строение.
Тиазиновые красители — аналоги оксазинов, содержащие тиониевую серу на месте оксониевогц кислорода. Получаются они окислением индаминов и индофенолов, содержащих в о-положении к имидному азоту сульфгидрильную группу, или же введением серы в индамины или индофенолы. Важнейшими представителями этой группы красителей являются следующие. Т и о н и н, или фиолетовый: Лаута, солянокислый 3, 3 -диаминоди-феназтионий
NH
Λ
NH2
Cl
простейший представитель этой группы; получается либо окислением двух молекул и-фенилендиамина в присутствии сероводорода либо окислением простейшего индами-на с тиосульфатами; мало применим в практике и имеет преимущественно теоретич. интерес. Метиленовый голубо й— тетраметильное производное предыдущего; получается он при окислении Биндшедле-ровского зеленого (индамина из нитрозоди-метиланилина и диметиланилина), в присутствии сероводорода или тиосульфата и выпускается в продажу в виде солянокислой соли или двойной соли с ZnCl2; применяется для печатания по танниновой протраве и в медицине. При замене диметиланилина диэтил-о-толуидином получается новый метиленовый голубой, отличающийся повышенной прочностью к кислотам, но меньшей прочностью к щелочам. Метиленовый зелены й—нитропроизводное предыдущего, мало применим.
3. Сернистые красители. В некотором родстве с азиновыми и особенно тиазиновыми красителями находятся сернистые красители. Они получаются сплавлением с полисульфидами при различных ί°, в присутствии или отсутствии растворителей, различных промежуточных продуктов, как например аминов, нитраминов, производных дифениламина и других, а иногда и животных или растительных продуктов. Первыми представителями этого класса были красители, т. н. к а ш у Л а в а л я, полученные при сплавлении различных орга-
нич. отбросов (древесных опилок, крови, -соломы и тому подобное.) с серой и едкой щелочью, открытые впервые Круассаном и Бретонье в 1873 г. Р. Видаль получил первый черный сернистый краситель при сплавлении и-фе-нилендиамина и н-аминофенола с серой и едким натром. Им же открыт также способ сплавления органических соединений с заранее приготовленными полисульфидами, имеющий в настоящее время преимущественное значение.
Строение сернистых красителей еще не вполне выяснено. Основные работы проделаны Р. Гнемом |6], предположившим присутствие в сернистых красителях производных тиодифениламина, соединенных· дисульфид-хной группой.
Вообще в сернистых красителях предполагается наличие содержащих серу гетероциклов, соединенных дисульфидными груп-пами—S—S—. При действии сернистых щелочей, например Na2S, происходит восстановление дисульфидной группы в две сульфги-.дрильные группы—SH, дающие с щелочами растворимые в воде и субстантивно выбираемые растительным волокном соли. При действии кислорода воздуха лейкосоединения сернистых красителей на волокне переходят в фиксируемые последним нерастворимые, прочные к мылу и свету, но недостаточно прочные к хлору красители. В виду нерастворимости сернистых· красителей в органических растворителях выделение их в чистом виде представляет большие трудности; лишь для некоторых из них удалось получить кристаллизующиеся ацетильные, бензоильные и глициновые производные их лейкосоединений и произвести полный их анализ. Так, из иммедиальиндона R, называемого в СССР сернистым -синим R, получаемого при сплавлении с полисульфидами индофенола, приготовленного из нитрозофенола и о-толуидина, было получено (при обработке его лейкосоединения монохлоруксусной к-той) следующее соединение
Н3С
V
vNv
ΗΝ7 -7ч>.Ч7 S--CK2 -COO НООС-СН2 I _I
Это позволяет предположить следующую схему получения красителя, его лейкосоединения и глицинового производного последнего
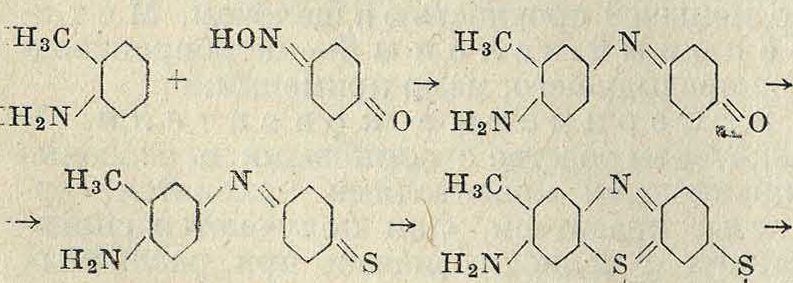
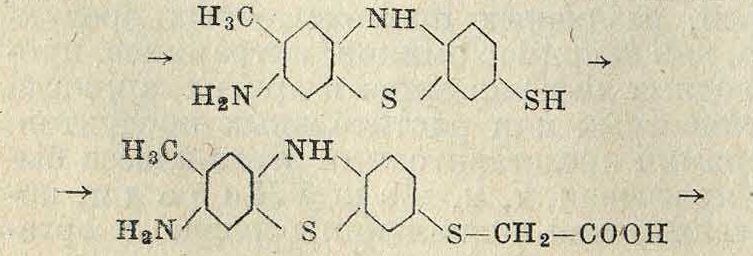
| H.cv | /Ν-γΝ |
| ΗΝ74 | 77 s 74^4s сн2 coo |
| НООС-СН2 | 1 1 |
С другой стороны, был синтетически получен продукт, обладающий всеми свойствами сернистого красителя, введением дисуль-фшдной группировки действием дисульфида натрия на диазониевую соль тионина по следующей схеме
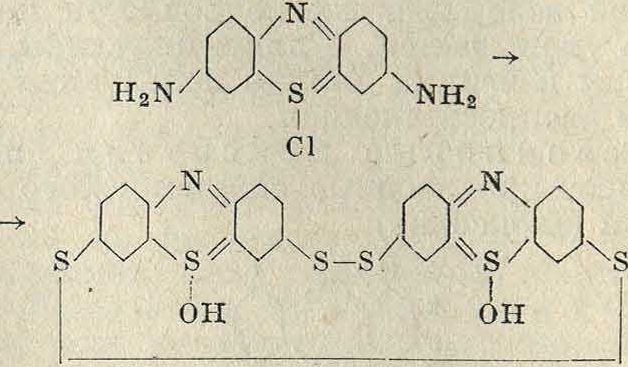
Отсюда можно считать доказанным присутствие в некоторых сернистых красителях тиазинового цикла и дисульфидных групп. Сернистые красители бывают различных оттенков— желтого, коричневого, зеленого, синего и черного цвета. Известен лишь один красный сернистый краситель, полученный .сплавлением готового азинового красителя красного же цвета, но он не является типичным представителем сернистых красителей и не имеет прочности последних.
Сернистые красители находят значительное применение в крашении растительного волокна в силу своей дешевизны, удобства применения и прочности к мытью и свету. Точной классификации сернистых красителей пока не существует вследствие невыясненности их строения; попытку же классифицировать их по окраскам следует считать нерациональной. В зависимости от исходных продуктов, служащих для щелочного плавления, сернистые красители можно разбить на три группы: а) получаемые из аминов, нитросоединений и тому подобное., б) из индаминов и индофенолов и в) из готовых циклич. красителей. Сернистые красители могут применяться и как кубовые, к которым они очень близки, т. к. и те и другие выбираются тканью лишь в виде растворимой Na-соли лейкопроизводного и вызревают на воздухе под действием кислорода. Так, тио индиго может применяться как собственно кубовый краситель, окрашивая ткань из гидросульфитного куба, и как сернистый, окрашивая ткань из сернистой ванны. Точно так же ценный сернистый краситель гидроновый синий, получаемый при сплавлении с сернистыми щелочами и серой индофенола из нитрозофенола и карбазола, дает лучшие выкраски из гидросульфитного куба.
Технически сернистые красители получаются сплавлением органических соединений с полисульфидами различного содержания серы. Вначале приготовляется раствор полисульфида (растворением серы в сернистом натрии), после чего к нему прибавляются органич. соединения, и реакция ведется при различных Г-ных условиях для различных красителей. Нек-рые особенно ценные кра-
сители, как пирогеновый синий или пиро-геновый индиго, получаются в овой среде, когда при более длительной обработке и более низкой t° получаются и более чистые красители. Продукт плавления м. б. непосредственно пущен в продажу в виде пасты или выделен в виде осадка высаливанием и продуванием воздуха; в последнем случае он поступает в продажу в порошкообразном виде. Иногда приходится производить очистку красителя, для чего последний растворяют в Na2S, отфильтровывают от нерастворившихся примесей и выделяют из раствора в виде осадка высаливанием или продуванием воздуха. Сернистые красители выпускаются фирмами под различными названиями. Так, ф-ка Байера выпускает их под названием катигеновых, фабрика Фарбверке—под названием пирогеновых, Касселла—иммедиалевых, Баденская—крио-геновых, Гейги—эклипсовых, Калле—тио-новых, АГФА—сернистых. Под названием сернистых выпускает эти красители также и Анилтрест.
Из ряда отдельных представителей сернистых красителей следует отметить следующие. Кашу Лаваля (о получении его смотрите выше); окрашивает растительное волокно в зеленовато-желтые, до коричневых, цвета. Криогеновый коричневый — продукт сплавления с полисульфидами 1, 8-динитронафталина, предварительно обработанного бисульфитом натрия. И м м е-диалевый желты й—из ж-толуилен-диамина и полисульфида. Иммедиале-вый чисто сини й—продукт сплавления с полисульфидами 4 - диметиламино-
4-оксидифениламина, получаемого восстановлением индофенола из и-аминодиметил-анилина с фенолом. Пироге н-и н д и-г о—продукт сплавления с полисульфидами, или обработки полисульфидами в овой среде 4 - фениламино - 4 - оксидифениламина или лейкоиндофенола, приготовленного из нитрозофенола и дифениламина. Пирогеновый синий—продукт обработки полисульфидами в овой среде 2, 4-дини-тро-4-оксидифениламина, получаемого из 2, 4-динитрохлорбензола и и-аминофенола. Гидроновый синий—продукт сплавления с полисульфидами и серой индофенола, полученного из нитрозофенола и кар-базола, или JV-этилкарбазола. Черный Видал я—продукт сплавления с полисульфидом натрия и-аминофенола. Сернистый черный Т, или иммедиале-вый черный (иммедиалькарбон), или катигеловый черный 2В, самый распространенный краситель этого класса— продукт сплавления с полисульфидом натрия 2, 4-динитрофенола, получаемого омылением 2, 4-динитрохлорбензола. Зеленые сернистые красители получаются при сплавлении с полисульфидами различных соединений в присутствии солей меди. К сернистым красителям близки и тиазоло-вые красители, получаемые сплавлением производных и-толуидина с серой; наир, примулин, содержащий ряд тиа-золовых циклов, получается из дегидротио-паратолуидина (смотрите); применяется гл. обр. для получения на волокне азокрасителей.
Класс V. Метиленхинонные и метиленхинонимидные красители.
Метиленхинонные красители — производные метиленхинона.
0=О=сн“
или метиленхинонимида
hn=<(^>=ch2
в которых один или оба водорода метиленовой группы замещены арильными остатками. Если последними замещены оба водорода метиленовой группы, то получаются так называемым трифенилметановые красите-л и. Например фуксин есть солянокислая соль ди-и-аминопроизводного дифенил-метиленхинонимина
HN-
О
хо-
-NH·
НС1
-nh2
называемого фуксонимином. При восстановлении все подобные красители переходят в производные трифенилметана; так, в фуксине л.ейкооснбвание красителя является триаминотрифенилметаном
h2n-<3-ch
<^>-NH2
переходящим при окислении в карбиноль-ное основание красителя, так называется розанилин
h2n
-К
он
<(3~NH2
—nh2
солянокислая соль которого с отщеплением воды образует краситель
h nh2-<^)>-c
С1
он
—nh2
Ο-ΝΗ*
,1 CI Ч0-”н·
При обратном процессе нейтрализации соли красителя образуются последовательно следующие продукты
HN=( >=0/^—/
/ч н он
J
0-NH*
аммонийное основание
► HN:
0°
/0-NH* ^
4<3>~NH2
имин (диаминофуксонимин)
„/О™·
άκΟ-ΚΗ·
• η2ν-<3-
карбинольное основание
Вначале получается окрашенное аммонийное основание, переходящее с отщеплением воды в окрашенный же хиноидный имин; последний, присоединяя воду, переходит в бесцветное основание, представляющее наиболее прочную модификацию. В зависимости от тех ауксохромных групп, которые со-
15
Т. Э. m. XI.
держатся при арильных остатках, получаются диамино- и триамино-трифенилметановые красители и окситрифенилметановые красители. Если в названных выше красителях при арильных радикалах содержатся в о-положении к трифенилметановому углероду амидные группы, способные к замыканию новых гетероциклов, то при этом замыкании получаются акридиновые красители (эти красители стоят в таком же отношении к трифенилметановым, как азины— к индаминам). Если в тех же красителях при арильных радикалах содержатся в о-по-ложении оксигруппы, точно так же замыкающие новые гетероциклы, то получаются ксантеновые красители. Акридиновые и ксантеновые красители могут быть производными как дифенил-, так равно и трифенилметана, представляя в последнем случае мезофенилакридиновые и мезо-фенилксантеновые красители. Последние в зависимости от наличия в них тех или иных групп могут быть разбиты на три отдела: розамины, содержащие незамещенную мезофенильную группу; родамины, содержащие при мезофенильной группе карбоксил в о-положении к трифенилметановому углероду и NH2-rpynnbi в остальных арильных ядрах, и фталеины, по строению аналогичные родаминам, но содержащие вместо аминогрупп ОН-группы.
Классификация метилен-хинонных красителей. 1. Трифенил-метановые красители (диаминотрифенилме-тановые красители, триаминотрифенилмета-новые красители, окситрифеммметановые красители). 2. Акридиновые красители (собственно акридиновые красители, мезофенилакридиновые красители). 3. Ксантеновые красители [собственно ксантеновые красители (пиронины), мезофенилксантеновые красители: а) розамины, б) родамины, в) фталеины].· 4. Оксикетонные и кетонимидные (дифенилметановые) красители. 5. Хинолиновые красители.
Метиленхинонные красители являются одним из наиболее ранних синтетическ. красящих веществ. Так, фуксин был получен еще в 1856 году Натансоном и в 1858 г. А. В. Гофманом. Вслед за тем были полущены фиолетовый Гофмана, фиолетовый Дебнера и ряд других. Исследованием их строения мы обязаны работам А. В.Гофмана, Э. и О.Фишеров, Розенштиля, Дебпера, Каро, Гантша, Гомолка и других. Однако несмотря на многочисленные работы строение этих красителей не может считаться установленным (смотрите выше теорию цветности). Рациональная номенклатура трифенил-• метановых красителей основана на связи их строения с дифенилметиленхинопом—фуксоном
0=0
и дифенилметиленхинонимином—фуксонимином
<°
О
HN— =С<
Так, фуксин м. б. назван солью п, п-диаминофуксон-имина, а розоловая к-та
>=о=<
-он
чО-°“
п, n-диоксифуксоном. Метиленхинонные красители относятся по технич. применению к основным красителям или к кислотным (если в них содержатся кислые солеобразующие группы S03H и СООН).
1. Диаминотрифенилметановые красители, называемые иначе группой малахитового зеленого, получают конденсацией бензальдегида и его производных с двумя молекулами амина в присутствии H2S04, НС1 или ZnCl2. Конденсацию ведут при избытке амина, который по окончании конденсации полностью отгоняется с водяным паром, а получившееся в твердом виде лейкосоединение красителя окисляется в краситель перекисью свинца в кислом растворе и выкристаллизовывается в виде соли с соляной, серной, щавелевой, уксусной и другими к-тами, что можно выразить схематически так
Некоторые красители, содержащие сульфо-группы, служат кислотными красителями (кислотные зеленые). При синтезе этих красителей бензальдегид можно заменить бензойной кислотой и тогда отпадает необходимость дальнейшего окисления лейкосое-динений. Из отдельных представителей можно отметить следующие. Фиолетовый Дебнера, родоначальник их—хлористый
4-аминофуксонимоний, не имеющий практич. применения. Малахитовый зеле-н ы й—тетраметильное производное предыдущего; получается конденсацией бензальдегида с двумя молекулами диметиланили-на; наиболее распространенный краситель этого отдела; поступает в продажу б. ч. в виде хорошо кристаллизующейся двойной соли с ZnCl2; его хлоропроизводные и сульфо-соли, получаемые соответственно из хлор- и сульфопроизводных бензальдегида, обладают большей прочностью к свету; все они являются основными красителями. Яркий зелены й—тетраэтильный аналог малахитового зеленого, точно так же широко распространенный основной краситель. К и-слотный зеленый йй
so3-c6h4
/0-N<CaHS
-~^N 0=c W СНг|бН4
C2H5 S03Na
Na-соль внутренней соли 4-этилсульфобен-зиламино - этилсульфобензилфуксонимония получается при конденсации бензальдегида с двумя молекулами этилбензиланилина и сульфированием продукта конденсации; после сульфирования и окисления лейкосоединения красителя высаливается Na-соль красителя, имеющего кислые свойства и применяемого для крашения шерсти и шелка.
Ксиленовый зеленый — изомер предыдущего, содержащий обе сульфогруп-пы при бензальдегидном ядре с/х~у ЧСН2~С6Н34<^>-S03Na
S03Na
является 2,4-дисульфонатриевой солью основания 4-этилбензилампно-этилбензилфук-сонимония; получается конденсациейдисуль-фобензальдегида с двумя молекулами этил-бензиланилина и применяется как кислотный краситель.
Триаминотрифенилметано-• вые красители содержат три свободные или же замещенные аминогруппы в и-положении к центральному углероду в каждой из арильных групп и получаются следующими способами: 1) окислением смеси аминов каким-либо умеренным окислителем,
2) окислительной конденсацией диамино-дифенилметана с аминами, 3) конденсацией диаминобензигидрола или диаминобензофе-нона с аминами, 4) конденсацией п-аыино-бензальдогида с двумя молекулами амина. Из отдельных представителей можно отметить следующие. Новый фуксин, или пара фуксин, солянокислая соль 4, 4-диаминофуксонимина; получается окислительной конденсацией диаминодифенилме-тана (из формальдегида и анилина) с анилином; служит также для получения ового синего и щелочного голубого. Фук-с и н, солянокислая соль 4,4-диаминометил-фуксонимина; получается окислением смеси анилина с о- и n-толуидинами. Для окисления раньше применялись хлорн. олово (Берген, 1858 год) и овая кислота (Ни-кольсон, 1859 год), в настоящее же время— исключительно нитробензол в присутствии небольшого количества железных опилок. Процесс ведется след, обр.: к смеси оснований прибавляют 30%-ной соляной кислоты и выпаривают воду; затем вводят железо и нитробензол и нагревают в течение нескольких часов при 190°; полученный плав выпускают из Котла, дают ему застыть, измельчают и кипятят с водой под давлением; полученный раствор отфильтровывают, прибавляют соляной кислоты и высаливают краситель поваренной солью; осадок растворяют в воде, подкисленной соляной к-той, прибавляют к горячему раствору поваренной соли, точно нейтрализуют избыток соляной кислоты со- дой и оставляют медленно кристаллизоваться. Фуксиновый плав заключает кроме самого фуксина еще и побочные продукты— главн. обр. фосфин (смотрите ниже, акридиновые красители), который может быть извлечен из осадка- после первого экстрагирования плава. Фуксин окрашивает животное волокно без протравы, а растительное по кислой протраве в фиолетово-красный цвет. Благодаря малой прочности окрасок он применяется теперь довольно редко. Раствор фуксина при пропускании S02 обесцвечивается, давая так называемую фуксиносернистую кислоту (вероятно — сернистокислый эфир триаминодифенилтолилкарбинола)
nh2
-<^>-nh2
S02H
применяемую как реактив на альдегиды и при действии минеральных кислот легко разлагающуюся с обратным образованием фуксина. Гофмана фиолетовы й— триметилфуксин, первый алкилированный краситель этого ряда; получается путем алкилирования фуксина йодистым метилом или йодистым этилом в автоклаве, в гольном растворе. Метиловый фиолетовый 4В — пентаметилпарафуксин; получается при окислении диметиланилина в присутствии солей меди, причем одна из метиловых групп диметиланилина служит основанием для образования трифенилметано-вого углерода; основной краситель, применяемый в крашении и печатании и при производстве чернил и химическ. карандашей. Кристаллический ф полет о-в ы й,—гексаметилпарафуксин; получается конденсацией кетона Михлера (из а и диметиланилина) с диметиланилином или окислением соответствующего вторичного а (гидрола Михлера) с диметиланилином. Метиловый зелены й—иод-метиловое соединение предыдущего, разлагающееся при 100° на кристаллический фиолетовый и CH3J. Анилиновый синий, или овый сини й,—три-фенилфуксин; получается при нагревании основания фуксина с анилином; он растворим в е, но нерастворим в воде. Щелочной голубо й—моносульфо-производное анилинового синего, получаемое при обработке его при 35° серной к-той. Na-соль, слабо окрашенная вследствие ее перехода в соль карбинольного основания, служит кислотным красителем и после обработки кислотами принимает синий цвет. Водный голубой—трисульфосоль ового синего, кислотный синий краситель, получаемый при полном сульфировании ового синего. Кислотный фу к си н— продукт сульфирования фуксина, представляющий смесь его ди- и трисульфокислот. Формиловый фиолетовы й—двунатриевая соль 4, 4-дисульфобензилдиэтил-диаминодиэтилфуксонимония, получается окислением * дисульфокислоты дибензилди-этилдифенилметана (из формальдегида и двух молекул бензилэтиланилинсульфокис-лоты) с диэтиланилином. Виктория голубо й>—пентаметил-производное нафтилового аналога нового фуксина; получается из кетона Михлера и метил-а-нафтиламина.
Окситрифенилметановые красители получаются аналогично предъ-идущим, если взяты оксипроизводные бен-зальдегида или фенолы вместо аминов. Из отдельных представителей можно отметить следующие. А у р и н, или розоловая кислота,—4, 4-диоксифуксон; получается конденсацией щавелевой кислоты или формальдегида с фенолом в присутствии крепкой сер-
C6H5-CH2-N^<f~V
W С2Н5 он
h2n-
-о-
ной к-ты; применяется для окраски бумаги и для получения лаков. Хромруби н— Na-соль трикарбоновой кислоты предыдущего; получается при действии формальдегида на салициловую к-ту (3 молекулы) в присутствии серной кислоты и дает красно-фиолетовые выкраски по протравленной хромовыми солями шерсти. Эриохромцианин, Na-соль 2-сульфокислоты 3-метил-4-окси-5-карбокси-о-метил-о-карбоксифуксона
S03Na
N
>о со он
/СХ
СН3
0=<ГЛ=с/^сн3
чО-°“
чсоон получается конденсацией бензальдегид-о-сульфокислоты сдвумя молекулами о-крезо-тиновой к-ты; синий протравный краситель. Фенолфталеин, Na-соль 2-карбокси-4,4-диоксифуксона,неправильно причисляемая к фталеинам; получается конденсацией фталевого ангидрида с двумя молекулами фенола в присутствии ZnCl2 или H2S04. В качестве красителя не применяется; употребляется как индикатор в алкалиметрии, так как лишь щелочные соли его окрашены в фиолетовый цвет, свободный же фенолфталеин бесцветен. Объясняют это обычно тем, что лишь соли фенолфталеина имеют хино-идное строение
Н0-О-?=О=°
~ I— COONa
свободный же фенолфталеин является лак-тоном те-диокситрифенилкарбинол-о-карбо-новой к-ты но
КО
-со он
2. Акридиновые красители получаются аналогично ди- и трифенилме-тановым красителям путем конденсации формальдегида или бензальдегида и его производных с м-диаминами с последующим замыканием дигидроакридинового кольца и окислением в краситель по схеме н2нч
nh2
h2n.
сно ч н2
N
NH2
Н2
N
,nh2 h2n.
-сн-
I
nh2 h2n.
/NH
^сн
H2Nn
Λ /ΝΗ2 HC1
ссо
солянокислый 2, 2-диамино-мезофенилакридин
Характерным для этих красителей является наличие акридинового ядра
/*4
I
рациональная их номенклатура основаан на приведенной здесь нумерации акридинового скелета. Изображенная выше форма (I) акридиновых красителей не может считаться окончательной; с таким же правом можно считать их производными хлористого акридония (II) или комплексн. солями (III) н С1
ΝΗ2—i
II.
III.
h2n
о
-nh2
,ΝΗ,
Cl
Часто замыкание акридинового кольца происходит одновременно с конденсацией; в противном случае приходится нагревать промежуточный продукт с кислотой в автоклаве; окисление же производится действием FeCLj. Акридиновые красители м. б. получены и из кетона Михлера конденсацией его с ж-диаминами в автоклавах в присутствии НС1 по схеме:
(ch3)2n4
h2n4
N
со
,nh2
N(CH3)2
(ch3)2n4^. ν4Λ/νη,
ll(CH3)2(ΟΗ3)!ΝχΛ/Ν%Λ/ΝΗ!
N(CH3)2
При этом промежуточным продуктом является ж-аминофенилаурамин. Из отдельных представителей можно отметить следующие. Акридиновый желтый, 3, 3-диметил-2, 2-диаминоакридин, получаемый конденсацией формальдегида с ж-то-луилендиамином основной краситель. А к-ридиновый оранжевый — тетра-метильное производное 2, 2-диаминоакри-
дина; получается при конденсации формальдегида с несимметричным диметил-ж-фени-лендиамином. Бензофлавин—·3, 3-диметил -2, 2 - диаминомезофенилакридин; получается из бензальдегида и ж-толуилен-диамина; основной краситель желтого цвета. Акридиновый оранжевый — тетраметильное производное 2, 2-диамино-мезофенилакридина; получается конденсацией бензальдегида с несимметричным диме-тилфенилендиамином; основной краситель. Ф о с ф и и—побочный продукт при фукси-новой плавке (смотрите выше); получается частичной конденсацией анилина с и-толуидином, основной краситель сн
XT о
,ΝΗ»
СН3
NH2
(^N
/ЧУче/1
NHa-HCl
СН3
I
NHa
Р е о н и н—несимметричный, акридиновый краситель, 2-диметиламино-2 -аминопроизводное мезофенилакридина; получается конденсацией кетона Михлера с ж-фениленди-амином; коричнево-желтый основной краситель. Флавэози н—тетраэтильное производное 2, 2-диаминомезокарбоксифенил-акридина; получается конденсацией фтале-вого ангидрида с двумя молекулами несимметричного диэтил-ж-аминофенола.
3. Ксантеновые крас и, тел и. Пирониновые красители получаются аналогично акридиновым, если вместо ж-ди-амина брать ж-аминофенол, по схеме:
R2n.
Ч,
/ОН НОч
+ сн2о +
NR.
R2N.
/° ч-сн^
,N(Ra Ас) или
RaN4
Ас
I
//°,
Чн
,nr2
(где Ас—кислотный радикал) и представляют собою яркие основные красители. Так, тетраметил-и тетраэтилпиронин, получаемые из формальдегида и ж-диметил- или диэтил-аминофенола, являются красивыми красными основными красителями. Близки к пиро-нинам также и сукцинеины, например родамин S
(CH2)N.
ТССг
i N(CH3)2
Gy I
Ο,τ-Б СООИ
получаемые при конденсации двух молекул диметйл- или диэтил-ж-аминофенола с янтарной к-той. Рациональные названия этих красителей, содержащих пироновый цикл с оксониевым кислородом, производятся от соли ксантилия
Ас
I
2^ 3 "
уч2
i и I L
Мезофенилксантеновые красители. а) Розамин ы—мезофенилпиро-нины с общим скелетом вида Ас
r2n
//°Ч,
Чс
I
nr2
Они получаются из бензальдегида и ж-ами-нофенолов и представляют собою красные яркие основные красители. При введении в них сульфогрупп получаются и кислотные красители. Среди отдельных представителей розаминов отметим следующие. Розами н—солянокислая соль тетраметильного производного 2, 2-диаминомезофенилксан-тилия; получается из бензальдегида и двух молекул диметиламинофенола. К с и л е н о-вый красный В—внутренняя соль дисульфокислоты тетраэтилы-юго производного 2, 2-диаминомезофенилксантилия; получается из дисульфобензальдегида и диэтил-ж-аминофенола; близкий родственник кси-ленового голубого, синевато-красный кислотный краситель. б) Родамин ы получаются конденсацией фталевого ангидрида с различными ж-аминофенолами в присутствии ZnCl2 по следующей схеме:
r2n.
он но. со—о
2nr2
-со
r2n.
С1
I
А
Ч/‘
I
,nr2
-СООН
Отдельными представителями родаминов являются следующие. Родамин В—тетра-этилродамин; получается из фталевого ангидрида и диэтил-ж-аминофенола; красный краситель с желтой флуоресценцией, применяемый для печатания на растительном волокне по танниновой протраве. Родамин 6G — этиловый эфир предыдущего более желтого оттенка; получается этилированием родамина В. Виола мин В—дисульфокислота дифенилродамина, красно-фиолетовый кислотный краситель. Среднее положение между родаминами и фталеинами занимают р о д о л ы, получаемые конден-
сацией фталевого ангидрида с одной молекулой ж-аминофенола и одной молекулой ж-дифенола, как родамин 12G—2-диметиламино - 2- метокси-мезоэтилкарбокси-фенилксантенил; желто-красный основной краситель. в)Фталеин ы—не содержат аминогрупп и получаются конденсацией фталевого ангидрида с двумя молекулами ж-дифено-ла (резорцина и тому подобное.). Причисляемый обыкновенно к этой группе фенолфталеин является в сущности трифенилметановым красителем. Простейшим фталеином следует считать флуоресцеин, получаемый из фталевого ангидрида и двух молекул резорцина и имеющий строение
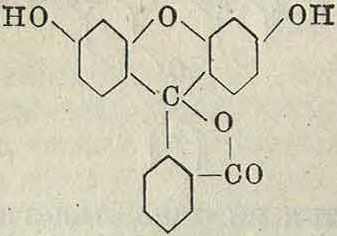
Флуоресцеин, или уранин, является весьма интенсивно флуоресцирующим кислотным красителем. Техническое применение находят только его галоидопроизводные: э о з и н—тетрабромфлуоресцеин; метил-эозин— метиловый эфир эозина; этил-э о з и и—этиловый эфир эозина; эозин алы й—динитродибромфлуоресцеин; эри-т р о з и н—тетраиодфлуоресцеин; ф л о к-с и н тетрабромдихлорфлуоресцеин; бенгальская роз а—тетраиоддихлорфлу-оресцеин и тетраиодтетрахлорфлуоресцеин. Г а л л е и н получают, как и флуоресцеин, при сплавлении при 200° фталевого ангидрида с двумя молекулами пирогаллола; применяется изредка при печатании; служит гл. образом для получения це рулей на S—антр^хичонного красителя, получаемого при замыкании кольца по схеме
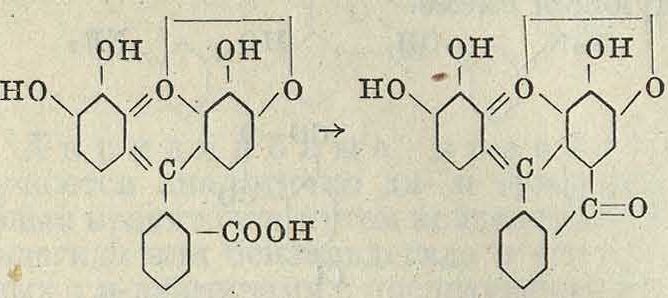
Церулеин В м. б. получен и из флуо-ресцеина при аналогичном замыкании ан-трахинонного кольца. Церулеины подобно многим другим антрахинонным красителям поступают в продажу в виде бисульфитных производных или борнокислых эфиров, хорошо растворимых в воде.
4.Оксикетонны eкрасители получаются по реакции Ненцкого—нагреванием полифенолов с карбоновыми кислотами в присутствии ZnCl2, например но он но он
II II
сн3 · соон + <3>-он -» сн3со—<^>-он галлац?тоф°нон но он
I I
но он
I
<3>-соон + ^>-он -* <3_со-0-он аливаринОЕЫЙ желтый А
Это протравные красители желтого цвета,
в настоящее время практического значения не имеющие; они интересны лишь тем, что по свойствам своим стоят близко к оксиантра-хинонам. Между прочим при этерификации ализаринового желтого А в щелочном растворе получается хиыоидный эфир строения но он
Ο
ι I
<:>=°
ОСН3
Это дает основание считать оксикетонные красители таутомерами и по их хиноидной форме причислять их к метиленхинонным.
Кетонимидные, или дифенил-метановые, красители (аурамины). Простейший и наиболее употребительный краситель этой группы—а у р а м и н О—получается либо действием газообразного аммиака на кетон Михлера в присутствии ZnCl-либо нагреванием тетраметилдиаминодифе2нилметана с серой и нашатырем (по Занд-мейеру). По строению считается таутомером
(CH3)2N-<3-C-0- N№H3)2 · HC1 ii NH
ii (CH3)2N-<^)-C=/=) nh2
=N(CH3)2 · C1
почему и м. б. отнесен к метиленхинонимид-ным красителям. Аурамин—основной краситель, дающий очень красивые окраски по шерсти и шелку и при печатании по танни-ну. При нагревании его растворов происходит разложение на кетон Михлера и аммиак. Другие аурамины получаются аналогично описанному, с заменой аммиака какими-либо первичными аминами.
5. Хинолиновые красители представляют производные хинолина (I) и его метиловых производных—хинальдина (II) и лепидина (III)
сн3
J
| Λ | ηΛ | ΓΛΧ |
| Nsr | XX4N/XCH3 | χΛ·Ν- : i |
| I. | II. | III. " |
Хинолиновые красители могут быть разбиты на соединения с одним хинолиновым ядром и двумя такими ядрами. К первым относится хинофталон, получаемый конденсацией фталевого ангидрида с хинальдином и имеющий строение
/СО,
о
:сн
СО
-/N I
/k
Изомерный с хинофталоном и з о хинофталон строения
<z>
I
со с=сн о
/“
I
получается при более низких /0 и м. б. переведен действием щелочей в’ хинофталон. Хинофталон растворим лишь в е, но при сульфировании дает растворимый в воде чисто желтый краситель — хинолиновый желтый, применяемый для крашения шерсти и особенно шелка, В то время как хинофталон получается из готового хинолинового производного, в другом красителе этого класса, флаванилине, хинолиновое кольцо получается синтетически. Ф давани л и н, мало применяемый желтый краситель, получается нагреванием ацетанилида с ZnCl2 при 230—250°; получение его может быть объяснено предварительной перегруппировкой в о- и и-аминоацетофеноны, которые, конденсируясь, дают флаванилин по следующей схеме:
Qj-NHCO · сн3
^ ^NHi C0-<^)-NH2
Г J +1 +
V4CO CH3I
CH8
+ HC1 ->
c^
-O
CH
—NH2 · HC1
или
CH3
Η
I
/Х с > хн.сл
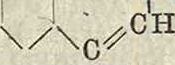
сн3
Ко второму отделу хинолиновых красителей относятся полученные Кенигом красители, содержащие два хинолиновых кольца, соединенных либо метиновой либо три-метиновой группой. Если пронумеровать хинолиновое ядро следующим образом
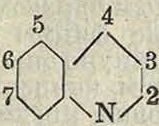
8 1
и принять термин хиноцианин для всех красителей, представляющих продукт соединения двух хинолиновых ядер с метановым радикалом, то все красители этого типа м. б. изображены как 4,4-хиноциаии-ны, или собственно цианины, либо как 2,4-хиноцианины, или изоцианины, либо как 2,2- или 2,4- или 4, 4-виниленхиноциа-нины, или карбоцианины. Все они получаются щелочной окислительной конденсацией хинолина с лепидином или хинальдином в присутствии йодистых алкилов, а также формалина (в случае карбоцианинов). Тащ цианин, или йодистый 1, 1 -диизоамил-4, 4-хиноцианин
/” /_ /C5Hi
c5H„-N >=сн-; n<%
/-
_ _
получается конденсацией лепидина с хинолином в присутствии йодистого изоамила. Этиловый красный, йодистый 1,1-диэтил-2,4-хиноцианин, получается конденсацией хинальдина с хинолином в присутствии C2H5J. Пинавердол, йодистый 1,6,1-триметил-2, 4-хиноцианин. П и н а-ц и а и о л, йодистый 1, 1-диэтил-2, 2-винил енхиноцианин, получается конденсацией двух молекул хинальдина с формалином в присутствии £H3J. Эти красители имеют применение исключительно как сенсибилизаторы в фотографии и фабрикуются в незначительных количествах, так что их цена очень высока (доходит до 1 000 руб-, лей за 1 килограмм).
Анализ К. в см. Анализ красителей.
Общие свойства продажных синтетических
К. в Большинство синтетич. К. в растворимо в воде и родными растворами их пользуются для окраски текстильных материалов и других товаров. Такие красители выпускаются на рынок красочными ф-ками в виде порошков, реже—кристаллов или кристаллообразных крупинок различной концентрации, то есть с различным содержанием чистого К. в Другие красители, как например ализарин, кубовые К. в и т. д., в воде нерастворимы и для приготовления красильных ванн для текстильных материалов приходится пользоваться их суспензиями в воде, которые тем удобнее для применения, чем тоньше измельчено суспендированное вещество. Достаточно тонкого измельчения нельзя достигнуть обычным перемолом высушенного красителя. Поэтому краситель, обычно получающийся в процессе фабрикации в виде осадка в водной среде, часто не высушивают, а пускают в продажу в виде водной пасты с содержанием сухого К. в 20, 40, иногда 50%. Чаще всего встречается 20%-ная паста. Наконец имеются красители, нерастворимые в воде, но растворимые в е, жирах и т. и., редко применяемые для окраски текстильных изделий, но идущие на изготовление овых и масляных лаков, окраску жиров и тому подобное. Эти красящие вещества продаются обыкновенно тоже в виде порошков.
Растворимые в воде красители при фабрикации их обыкновенно выделяются из водных растворов отсаливанием и реже— кристаллизацией. Отфильтрованные от маточного раствора и высушенные, они содержат всегда в большем или меньшем количестве примеси веществ маточного раствора, преимущественно поваренной соли; в разных партиях К. в содержание этих примесей колеблется в зависимости от хода фабрикации, степени отжима от маточного раствора и т. д. Поэтому разные партии одного и того же К. в могут выходить различной крепости. Для того чтобы иметь определенное К. в всегда одной и той же концентрации, его «ставят на тип», примешивая к нему (обычно на шаров, мельницах) какого-либо разбавителя—нейтрального вещества, не мешающего растворению К. в и не вредящего окраске, наир.—поваренной соли, безводной сернонатриевой соли, декстрина. Пробная выкраска на волокне, полученная таким «типовым» красителем, служит образ- · цом и к крепости такого «типа» подгоняют все позднейшие партии того же К. в путем разбавления теми же нейтральными веществами. Нек-рые красители выпускаются в продажу в различных концентрациях, иногда очень сильно разбавленными (например для удобства отвешивания при домашнем или кустарном крашении мелких партий товара). Иногда первоначальный тип выходит довольно сильно разбавленным, впоследствии I же, по мере усовершенствования производ ства или же изменения требований рынка, красочные фабрики начинают выпускать более концентрированные красители. К названиям таких красителей прибавляют обозначение «концентрированный» или «экстра-концентрированный» или же обозначают их концентрацию чи 200:100 (то есть краситель, вдвое более концентрированный, чем первоначальный тип), 500:100 и т. д. Наоборот, разбавленные против типа красители обозначают чи 70:100, 30:100 и тому подобное.
Все красители при восстановлении переходят с присоединением двух атомов водорода в так называемые лейкосоедине-н и я, в большинстве случаев бесцветные или окрашенные значительно «выше» самих красителей, но иногда в тот же цвет, что и красители, и даже глубже. Наоборот, окислением лейкосоединений, являющихся иногда промежуточными соединениями при фабрикации красителей, могут быть получены эти последние.
История и экономика. Производство синтетических К. в стало возможным лишь тогда, когда газовое, а впоследствии коксовое производства стали доставлять достаточно сырья для него, а успехи органической химии поставили работу по синтезу К. в на научную почву. Начало фабрикации синтетич. К. в было положено открытием английского химика Б. Перкина (в 1856 г.), получившего (окислением анилина хромовой кислотой) фиолетовое вещество, интенсивно окрашивавшее шерсть и шелк, названное им мовеином. Для фабрикации мовеина Перкином был основан специальный з-д. Вторым синтетич. К. в был фуксин, производство которого (путем окисления хлорным оловом анилина, содержащего толуидины), разработанное франц. химиком Бергеном, было поставлено в Лионе в 1859 году. Далее наиболее важными достижениями в области К. в были: в 60-х годах —получение анилинового синего Жираром и де-Лером и исследование этой реакции, а также реакций алкилирования А. В. Гофманом, исследование строения красящего начала корня марены—ализарина—и синтез его из антрацена Гребе и Либерманом (в 1868 году), открытие черного анилина Лайтфутом и открытие П. Гриссом диазосоединений; в 70-х годах—синтез азокрасителей и введение их в технику (Руссен, О. Витт), синтез дисазокрасителей (Нецкий), исследования Розенштиля, Э. и О. Фишеров над строением трифенилметановых красителей, синтез малахитового зеленого, установление Ад. Байером строения индиго и затем первый синтез этого красителя, синтез фталеинов (А. Байер, Каро), тиази-нов (Лаут), азинов, в частности сафранина (Гревиль и Виллиаме, Нецкий, О. Витт), оксазинов (Мельдола); в 80-х годах—продолжение исследований А. Байера по индиго и ряд синтезов, осветивших путь к технич. его получению, синтез аурамина (Керн и Каро), тар-тразина (Циглер), развитие химии субстантивных ди-сазокрасителей (Беттигер); в 90-х годах—два гейма-новских синтеза индиго (через 10 лет осуществленные в технике), работы Видаля по синтезу сернистых красителей и введение их в технику, бонн-шмидтовская реакция получения полиоксиантрахинонов, открытие Ильинским сульфирования антрахинона в a-положении, синтез ализарин-сафирола и начало разработки кислотных антрахинонных красителей. Начало 20 в богато крупнейшими достижениями в области К. в.: осуществлено производство индиго по обоим способам Геймана: открыто Фридлендером тиоиндиго и широко разработана область индигоидов; синтезирован Боном индантреновый синий и разработано большое количество способов получения кубовых антрахинонных красителей как индантренового, так и других типов; в области холодного крашения положено начало группе. нафтолов AS и различных диазокомпонентов для сочетания с ними. Во время войны 1914—1918 годов продолжалась разработка области индигоидов, антрахинонных производных, нафтолов AS и т. д.; многие из прежних способов получения известных красителей подвергались пересмотру и значительным изменениям. Послевоенный период принес бадеровекпе инди-гозоли, несколько классов красителей для ацетатного шелка (ионамины Грина), начало синтеза периленовых производных, усиление введения гетероцикли-ческих, гидроароматических и жирных непредельных остатков в молекулы красителей различных классов и широкую разработку прежних тем по кубовым ц холодным красителям. Синтезировано также боль
шое количество лаковых красителей, особенно из группы нитро-аминопроизводных.
Первые красочные з-ды были основаны в Англии и Франции. Вскоре их примеру последовала Германия, где в начале 60-х годов возник ряд предприятий, гл. обр. по Рейну и Майну, поблизости к эльзасской текстильной промышленности и на водных путях, веду“ щих в океан. Несмотря на первоначальное отсутствие своего сырья (газовую смолу приходилось выписывать из Англии) и меньшее чем в Англии развитие текстиль* ной промышленности,германские (и швейцарские) красочные заводы не только перегнали старейшие англ, и франц. з-ды, но и поглотили ббльшую часть их своей конкуренцией или же сделали их своими филиальными отделениями. Уже к концу 19 в герм, и швеиц. красочные промышленности оказались почти монопольными, поставляя синтетич. К. в во все страны мира, а в тех государствах, куда (как например в США и в Россию) ввоз красящих веществ был затруднен высокой таможенной пошлиной, основывая свой филиальные отделения, работавшие на привозимых из Германии полупродуктах. В 1913 году 20 главнейших германских фабрик производили красителей приблизительно на 400 млн. мар., что составляло около 88% мирового производства.
Три главнейшие герм, фабрики: Баденская анилиновая и содовая в Людвигсгафене на Рейне, б. Фридриха Байера в Леверкузене и Эльберфельде и Гехстские фабрики б. Мейстера, Луциуса и Врюнинга. Незадолго до войны герм, фабрики образовали две союзных группы:
1) из Баденской фабрики, Байеровской и Берлинского акц. об-ва анилинового производства, 2) из ГехстеКиХ ф-к, фабрики Л. Кассела и Калле и К°. После войны все упомянутые фабрики, с присоединением к ним фабрики Грисгейм-Электрон, Вейлер-тер-Мер (Weiler-ter Meer) и Ведекинд и К°, образовали Акц. о-во «Interessen Gemeinsehaft fur Farbenindustrie» (I. G.), так что в настоящее время германскую красочную промышленность можно считать единой.
В Англии, Франции, Италии, Японии, а особенно в Америке красочная промышленность сделала большие успехи во время войны и после нее. Во всех этих странах К. в фабрикуются теперь в столь значительных количествах, что производство их почти покрывает внутренний спрос; лишь редкие красители ввозятся в эти страны из Германии пли из Швейцарии. За внешние рынки, главными из которых являются Китай и англ, колонии, идет ожесточенная борьба между Германией и главным образом Америкой; на внутренних ’рынках многие фирмы Франции, Англии, Италии и Америки принуждены были в последние годы войти с германским концерном I. G. в те или иные соглашения, имеющие предметом распределение производства или сфер влияния. В Америке в последнее время основано акционерное общество «I. G. Dyestuffs Corporation».
В России до войны 1914—18 гг. собственной красочной промышленности почти не было. Подавляющее большинство ходовых красителей в России производилось отделениями герм, ф-к: Фр. Байера, Фарбверке, Баденской—в Москве, Кассела—в Риге, Берлинского акц. общества—в Либаве, Калле—в Варшаве. Ставка таможенного тарифа на красители (21 р. с пуда) делала выгодным производство внутри страны массовых дешевых сернистых и азокрасителей из привозных полупродуктов, чем и пользовались упомянутые герм, и швейц. фирмы. Самостоятельные русские фабрики не могли с ними конкурировать, так как производить внутри страны промежуточные продукты они не могли по отсутствию сырья, дороговизне вспомогательных материалов и отсутствию техническ. опыта. В 1913 году в Россию было ввезено 652 тонны индиго на сумму около 2 млн. руб. и 1 540 тонн других красителей на сумму 5,2 млн. руб.; произведено же внутри страны· (почти исключительно филиалами герман. и швейцарских ф-к) ок. 9 000 тонн красителей на 11,5 млн. руб.
В СССР государственная красочная промышленность со сред оточен а в двух трестах—Анилтресте и Юж-химтресте. Первый имеет в своем распоряжении заводы Дербеневский (б. филиал Фарбверке), Дорогомиловский и Бутырский (б. филиал Баденской фабрики) в Москве и Кинешемский (б. Бензоло-анилинового т-ва) в Кинешме: второй—завод близ ст. Рубежной в Донбассе. На Дербеневском заводе выпабатываются главным образом азокрасители, на Бутырском—сернистые, нигрозин и меховые красители, на Дорогомиловском—полупродукты и ализариновые красители. Ру-бежанский завод дает преимущественно полупродукты, сернистый черный, нигрозин и проектирует производство основных и индигоидных красителей. За 1926/27 год в СССР ввезено 1 463 тонны красителей на сумму 5,4 млн. руб., а произведено этими заводами 5 148 тонн на 8,45 млн. руб.
Лит.: г) «Helvetica chimica acta», Basel, 1928. v. 11, p. 87; 2) г. И. 367493, 371258. 36069П: з) «Lieb^s Annalen d. Chemie», Leipzig, 1925, L· 446, p. 123;_
4) Н. F i e г z-D a γ i d, «Helvetica chimica acta» Basel, 1928, p. 776; 5) «Ztschr. ang. Ch.», Leipzig, 1905, p. 1377; «) «B», 1906, Jg. 39, p. 1016.
1) Общая: Пора й-К о ш и ц А. В., Производство органических красящих веществ, Справочник по химической промышленности им. Л. Я. Карпова, вып.4, Л.,1924; Шик О., Химик-текстильщик,пер. с нем., П., 1923; Heermann P., Farberei- и. textilchemische Untersuchungen, 4 Auflage, В., 1923; Pier z-D a v i d Η. E., Kiinstliche organische Farb-stoffe, Technologie d. Textilfasern, herausgegeben von O. Herzog, В. 3, Berlin, 1926; Georgievics G., Handbuch d. Farbenchemie, 5 Aufl., Leipzig, 1922; Bucherer H., Lehrbuch d. Farbenchemie, Lpz., 1921; Mayer Fr., Chemie d. org. Farbstoife, 2 Aufl., Lpz., 1924; Lelivre L., Traitd de matiOres colorantes organiques, artilicielles, de leur preparation industrielle et de leurs applications, t. 1—2, P., 1896; Fierz-David H.E., Grundlegende Operationen d. Farbenchemie, 3 Auflage, Berlin, 1924; I о h 1 a и R. und Bucherer H., Farbenchemisches Prakti-kiirn, 3 Auflage, Berlin, 1926 (имеется в русском переводе); Cain J., The Manufacture of Intermediate Products for Dyes, 2 ed., L., 1919; Caro H., tfber d. Entwlcklung d. Teerfarben-Industrie, Berlin, 1893; Rowe F., Colour, Index, N. Y., 1924; F r i d 1 a e n-d er P., Fortschritte d. Teerfarbenfabrikation u. ver-wandter Industriezweige, В. 1—14, Berlin, 1877—1926; H e u m a η η K., Die Anilinfarben u. ihre Fabrika-tion, В. 1—7. Brschw. 1888—1906; Lehne A., Tabellarische Ubersicht d. kiinstlichen org. Farbstoffe u. ihre Anwendung in Farberei u. Zeugdruck, Brschw., 1898—1906; N 1 e t z k i R„ Chemie der org. Farbstoffe, 5 Auflage, Berlin, 1906 (имеется в русском пер.); Ristenpart. E., Chemische Technologie d. org. Farbstoffe, 2 Auflage, Berlin, 1925; Schulz G. und .f u 1 i u s P., Farbstofftabellen, 6 Aufl., В. 1, Berlin, 1923; Wahl A., L’industrie des matiferes colorantes organiques, Paris, 1912.—2) Строение и цвет красящих веществ: Пора й-Кошиц А. Е., Обзор исследований о связи между спектрами поглощения и строения органических соединепий, «Ж», 1908, т. 40, ч. 2, стр. 62—97; Georgievics &., Beziehungen zwischen Farbeu. Konstitution bei Farben-stoffen, Berlin, 1921; Kaufmann H., Ober d. Zu-sammenhang zwischen Farbe und Konstitution. Stuttgart, 1904; L e у H., Beziehungen zwischen Farbe und Konstitution, Leipzig, 1911; Watson E. R. Colour in Relation to Chemical Constitution,London, 1918; Пора й-К о ш и ц А., «Ж», 1913, t. 40, выпуск 3, сто. 62; K e h r m a n n, «Helvetica chimica acta», Basel, 1921, p. 527; Pfeiffer, Organische Molekulver-bindungen, Stuttgart, 1922.—3) Индигоидные красящие вещества: Georgievics G., Indigo von prakt. und theoret. Standpunkt, W., 1892; Truttwin H., Enzyklopadie d. Kiipenfarbstoffe, Berlin, 1920; Martinet M., Matures colorantes, L ’indigo et ses d6riv6s, Paris, 1926.—4) А н т p a x и-нонные красители: Gnehm R., Die Anthra-cenfarbstoffe, Brschw., 1897; В a r r y-B a r n e 11 e E., Anthracene a. Anthraquinone, London, 1921; Η о u-b e n J. und Fischer W., Das Anthracen und Anthraehinon, Berlin, 1928.—5) Азокрасители: В ΰ 1 о w C., Chemische Technologie d. Azofarbstoffe, Leipzig, 1897.—6) Хинонимидные красители: Шапошников В., Исследования из области азиновых и азониевых красителей, Киев, 1904; W а 11 e r J., Anilinfarbenfabrikation, Hannover,
1903.—7) Трифенилметановые красители: Fischer Е., Untersuchungen in der Tri-phenylmethanfarbstoffe, Hydrazine und Indole, Berlin, 1924; Μ ΰ h 1 h a u s e r О., Technik d. Rosanilinfarb-stoffe, Stuttgart, 1889.—8) Сернистые красители: L a n g e О., Schwefelfarbst.offe, 2 Auflage, Lpz., 1925.—9) Анализ красителей: «Изв. О-ва для содействия и улучшения мануф. промышленности», Москва, 1912; Green A., The Analysis of Dyestuffs a. their Indentification in Dyed a. Coloured Materials. Lake Pigments etc., 3 ed., London, 1920; Handbuch d. Farberei der Spinnfasern, hrsg. v. R. Loe-wenthal, 3 Auflage, В. 1—2, Berlin, 1921—23; Rug-s 1 i P., Praktikum der Farberei und Farbstoffanalyse, Miinchen. 1925; Zenker W. und Rettenberg H., Erkennung und Priifung v. Farbungen. Wittenberg, 1925 (краткий конспект—«ИТПТ», 1926, 20, стр. 3398); P e 1 ё t-J о 1 i v e t. Theorie d. Farbung, Dresden, 1911; «Journal Soc. Dyers and Coloristes», London, 192,3, p. 203. А. Порай-Кошиц и И. Иоффе.