 > Техника, страница 67 > Оксалаты
> Техника, страница 67 > Оксалаты
Оксалаты
Оксалаты, соли и эфиры щавелевой кислоты (смотрите).
0КСAMИД, амид щавелевой кислоты (смотрите).
ОКСИАНТРАХИНОНЫ, пол иок с и антра-х и и о н ы, производные антрахипона (смотрите), содержащие гидроксильные группы. О. являются либо красящими веществами (ем.)ли-
бо промеэ1суточпыми продуктами синтеза красителей (смотрите) и м. б. получены по одному из нижеследующих методов.
1. Синтетич. замыкание антрахинонного цикла (из карбоновых кислот, содержащих окси-групиы). а) При конденсации производных фталевого ангидрида с фенолами, аналогично синтетическому получению антра-хинона, как например он он
0=^>Ю--Ю=-=Ф
он он хинизарвн б) При конденсации двух молекул окси-бензойной кислоты, содержащей по крайней мере одну гидроксильную группу в .м-поло-жении к карбоксильной, и содержащей незамещенный водород в одном из о- или п- положений. При этом для простейшей λι-окси-бензойной кислоты возможны три случая конденсации, когда замыкание цикла идет в оба о-положения к гидроксильным группам, либо в оба п-положения, либо в о- и я,-положения по схемам он он
,-соои соон
-0
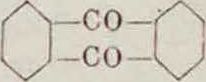
он он антраруфин он
Λ + cooh-^Y
-l^-соонт
-Ct&cr
он з-f V-он он- ’
антрафлавиновая к-та
0—СООН.
ΎθΟΗ-
I
ОН
ι-0-он-Ю-со—0-
-он он
Наиболее часто эта реакция применяется для получения антрахризона по схеме он
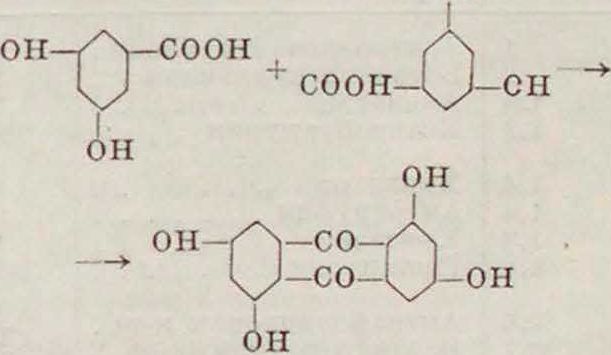
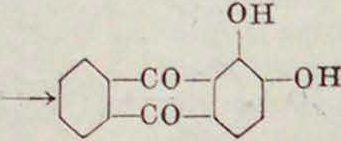
Возможна конденсация различных оксипро-изводных бензойной к-ты, наир.
| он | |
| 0Н- -С00Н | + Лгон - |
| и | соон—LJ-oh |
| он
1 | |
| „°н-С | 1
y-CO-YХ|-ОН |
но при этом идут побочные симметричные реакции.
2. Превращение первичного заместителя антрахннона. а) Из сульфокислот ан-трахинона—при действии Са(ОН)2 или едких щелочей; в последнем случае реакция
30
Т. Э. m. XIV.
сопровождается (в особенности в присутствии окислителя) окислением и внедрением лишней гидроксильной группы по схемам
Эта реакция применима и к сульфокислотам готовых оксипроизводных антрахинона, как например он
I
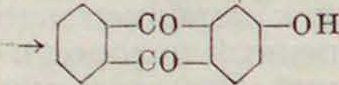
он
Сульфогруппа в α-положении гидроксилиру-ется значительно легче, чем в ^-положении (аналогия с нафталином), б) Из нитро-производных—либо через амины либо непосредственно, как налр.—получение пурпурина из 4-нитроализарина он
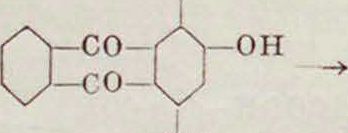
хо2
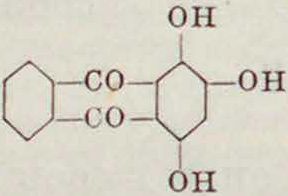
Иногда эта реакция сопровождается и дополнительным окислением и введением ли
шних гидроксильных групп, как например·
N0» ОН ОН
.он-б:^:Сгон
I I
no2 он ОН
но этот метод следует отнести к классу окислительных методов, в) Из г а л о и д о п р о-изводных—как первый синтез ализарина (смотрите), проведенный Гребе и Либерманом.
3. Окисление антрахинонных производных: а) в щелочной среде—как в получении ализарина; окислению м. б. подвергнут и сам антрахинон и готовые 1- и 2-оксиантра-хнноны; б) в кислой среде (смотрите Бонпа-Шмид-та реакция). Во избежание разложения полученных продуктов лучше превратить их в эфиры, преимущественно борной кислоты, в виду чего последняя вводится в реакционную смесь. Подобному окислению могут быть подвергнуты антрахинон, его моно-оксипроизводные: ализарин и другие, которые в зависимости .от условий окисления могут дать целый ряд полиоксиантрахинонов.
4. Удаление части оксигрупп из готовых оксипроизводных при действии восстановителей. Так, пурпурин м. б. переведен в хин-изарин по схеме он он
0=S^-°"-0=S:Q
он он
Число О. весьма велико: всего возможны 75 (2 моноокси-, 10 диокси-, 14 триокси-, 22 тетраокси-, 14 пентаокси-, Ю гексаокси-, 2 гептаокси-, 1 октаоксиантрахинон). В ни-
Таблица важнейших оксиантрахпнонов.
| Положение | Наименование | 1 пл. | Цвет | Цвет выкрасок по протравам | К
Я ~ Л . К E С | Способ получения (нумерация—по теисту) | ||
| онсигрупп | А1 | Сг | 1« | |||||
| 1 | Эритроонсиантрахинон. | 193 | Оранж. | _ | Красн. | _ | 1(a),2(a) | |
| 2 | Бетаонсиантрахинон. | 302 | Желт. | — | Красн. | — | — | 1(a),2(a) |
| 1,2 | Ализарин. | 289 | Оранж. | Красп. | Коричн. | Фиол. | + | 1(a),2(a),3 |
| 1,8 | Ксантонурпурин. | 264 | Желт. | Желт. | Желто-
коричн. |
Желт. | — | 1(a),4 |
| 1,4 | Хинизарип. | 198 | Красн. | Роз. | Сии. | — | — | 1(a),3,4 |
| 1,5 | Антраруфин. | 280 | Желт. | — | — | — | — | 1(0),2(a),2(6) |
| 1,8 | Хризазин. | 193 | Желт. | — | Красн. | — | — | 2(a),2(6) |
| 2,3 | Гистазарин. | >260 | Желто-
коричн. |
Красн. | Красно-
коричп. |
Фиол. | - | 1(a) |
| 2,6 | Антрафлавиновая к-та. | >330 | Желт. | — | — | — | — | Кб),2(a) · |
| 2,7 | Изоантрафлавин. к-та. | >330 | Желт. | — | — | — | 2(a) | |
| 1.2.3
1.2.4 |
Антрагаллол. | 313—314 | Оранж. | Коричн. | Коричп. | — | + | 1(a), Кб) |
| Пурпурин. | 257—259 | Оранж.-
нрасн. |
Алый | Красно-
норичн. |
— | + | 3(6) | |
| 1,2,5 | Ализарин прний бордо R | 278 | Красн. | Красн. | Коричн. | Фиол. | + | 2(a), 3(6) |
| 1,2,6 | Флавопурпурин. | 360 | Зол от. | Ь | » | » | + | 2(a) |
| 1,2,7 | Антрапурцурин. | 369 | Оранж. | » | » | » | + | 2(a) |
| 1,2,8 | Оисихризазин. | 230 | Оранж. | * | » | » | + | 2(a),3(6) |
| 1,2,3,4 | — | — | » | » | » | » | + | 3(6) |
| 1,2,4,5 | Пурпурин бордо. | — | » | Алый | Фиол.-
коричн. |
Син. | + | 3(6) |
| 1,2,4,8 | » | — | » | » | » | * | + | 3(6) |
| 1,2,5,в | Руфиопнн. | 316—318 | Оранж. | Красн. | Коричн. | Фиол. | + | Кб),2(a) |
| 1,2,5,8 | Хинализарин. | >275 | Красн. | Бордо | Сине-крас. | — | + | 3(0) |
| 1,3,5,7 | Антрахризон. | >360 | Желтый | — | — | — | — | Кб) |
| 1,2,4,δ,8 | Ализарин пентацнанан. | — | Коричн. | Фиол. | Синий | — | + | 3(6) |
| 1,2,3,5,6,7 | Руфигаллол. | 259 | Красн. | Сине-
красн. |
— | Фиол.-
черн. |
+ | Кб) |
| 1,2,4,5,6,8 | Антраценовый синий WR | — | Коричн. | — | Синий | — | 4* | 3(6) |
| 1,2,4,5,7,8 | Ализарингексацнанин. | — | — | — | Зелено синий | — | + | 3(0) |
| 1,2,3,4,5,в,7,8 | “ | Красно-
коричн. |
— | Красносини ii | *— | 3(6) | ||
жеследующей таблице приведены наиболее важные из О. (знаком + отмечены О., находящие применение в качестве красителей). См. также Красящие вещества, естественные, ст. 418.
Существует ряд метальных производных О., из которых наиболее важна группа хризо-фановой кислоты или З-метилхрйзазина но он
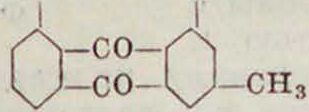
содержащаяся в растениях семейств Rliemn, Rumex, Frangula. Некоторые метилоксиан-трахиноны сопровождают ализарин в естественном крапе.
Лит.: Houben J. u. Fischer V., Das Anthra-cen и. die Anthrachinone, B., 1928; Barnett E. de Barry, Anthracen a. Anthraquinone, L., 1921; Ο n c li m R., Die Anthracenfarbstoffe, Brschw.,
1 897; Fierz-David Η. E., Kiinstliche Organische Farbstoffe, B., 1926. И. Иоффе.