 > Техника, страница 96 > Оксидная изоляция
> Техника, страница 96 > Оксидная изоляция
Оксидная изоляция
Оксидная изоляция представляет собой окись или гидроокись металла, образующуюся на его поверхности в результате химич. реакции соединения металла с кислородом. Окислы нек-рых металлов, как например тантала, алюминия, магния и др., обладают высокими электроизолирующими свойствами. Особый технич. интерес представляет О. и. на алюминии. Ёго соединение с кислородом (А1203) весьхма устойчиво. Вследствие чрезвычайной химич. активности алюминия по отношению к кислороду на поверхности алюминия в атмосфере воздуха всегда образовывается естественным окислением оксидный слой. Свеже-срезанный алюминий покрывается такой пленкой в течение долей ск. Этот слой выдерживает лишь доли Y и не представляет технич. интереса как изолирующий материал. О. и., имеющая технич. значение, получается искусственным способом. Таких способов известно три: 1) термическая обработка (нагревание металла), при которой высокая 1° способствует более активному окислению поверхности металла, чем в естественных условиях; 2) химическая обработка различными к-тами и щелочами. Эти два способа большого технич. интереса для электроизоляционных целей также не представляют, т. к. оксидный слой, таким способом полученный, выдерживает десятки Y; 3) наилучшим способом получения более толстого и электрически более прочного оксидного слоя на алюминии является электролитический. Этот способ называется также анодной поляриза ц и е и мо-
талла. Для этой цели алюминий погружается в электролит в качестве электрода и под действием электрич. тока, пропускаемого через электролит, кислород, соединяясь с алюминием, образует на его поверхности слой окиси А1203, а иногда гидроокиси А1203пН20. Единой общепризнанной теории, объясняющей механизм образования оксидного слоя, пока не существует. Имеются лишь попытки объяснить явление вентильного действия этого слоя, которое связано с процессом образования самого слоя. Сюда относятся теории Гюнтершульце, Добиаш и др. Оксидные слои, получаемые электролитич. способом, можно разделить по их свойствам и применениям на два класса.
Класс I. Весьма тонкие пленки (порядка сотых и десятых долей μ), применяющиеся в электролитич. выпрямителях и в качестве диэлектрика в электрич. конденсаторах. В электролитич. выпрямителях вентильным действием обладает оксидный слой, образующийся на вентильном металле в момент, когда он является анодом. Вентильное действие обнаружено у следующих металлов: Си, Be, Mg, Zn, Cd, Al, Sn, Pb, Nb, Та, Sb, W, U, Fe, Co, Ni. Вентильное действие бывает полным и неполным. Полное, — когда вентильный металл не растворяется в электролитах, неполное — растворимость вентильного металла искажает явление. Вентильное действие наиболее полно изучено на тантале, к-рый дает полное вентильное действие почти во всех электролитах. Для получения оксидных слоев для электрич. конденсаторов обычно употребляют водный раствор аммонийных солей (углекислый или борнокислый аммоний). Основные требования к электролиту следующие: наименьшее растворение оксидного слоя; достижение наибольшего «критического» напряжения, то есть напряжения, при котором появляется искрение; быстрое формование оксидного слоя; получение наибольшей емкости на единицу площади слоя и наименьшего тока утечки на единицу емкости. «Критическое» напряжение для данного электролита тем выше, чем меньше концентрация электролита. Толщина оксидного слоя, равно как и обратная величина емкости слоя, близка к пропорциональной зависимости от величины формирующего напряжения. Электрические конденсаторы для постоянного тока изготовляются на рабочие напряжения до 500 V. По способу, разработанному в ЛЭФИ, конденсаторы на напряжение до 100 V формируются в водном растворе двууглекислого аммония концентрации 0,1 N, на 400 V — 0,004 N. Основным условием для работы подобного диэлектрика в конденсаторе является необходимость постоянного присутствия электролита либо в свободном (жидком) виде — такие конденсаторы называются жидкостными — либо в бумаге, тканях или массах типа желатины, пропитанных ей и проложенных между обкладками конденсатора; такие конденсаторы называются полусухими. В качестве рабочего электролита употребляется раствор соли, в к-ром формировался оксидный слой, в глицерине. Длительность формирования для низковольтных конденсаторов 30—40 мин. Плотность тока при электролизе заметно не влияет на диэлектрич. свойства оксидного слоя. Диэлектрич. коэф. такого диэлектрика ε=8 -г 12. Уд. объёмное сопротивление порядка 1013 Q-см. Емкость слоя для единицы поверхности металла для низковольтных конденсаторов равна 0,2 4-0,5 р¥/см2, ток утечки 105 4- 10~7 A/pF. При рабочем напряжении в 400 V емкость единицы по
верхности 0,01 4- 0,02 [xF/см2 и ток утечки 10"4 A/[iF.
Класс II. Толстые оксидные слои, выдерживающие напряжение в несколько тыс. V и работающие в сухом виде. Толщина такого слоя О. и. достигает нескольких десятых долей миллиметров.
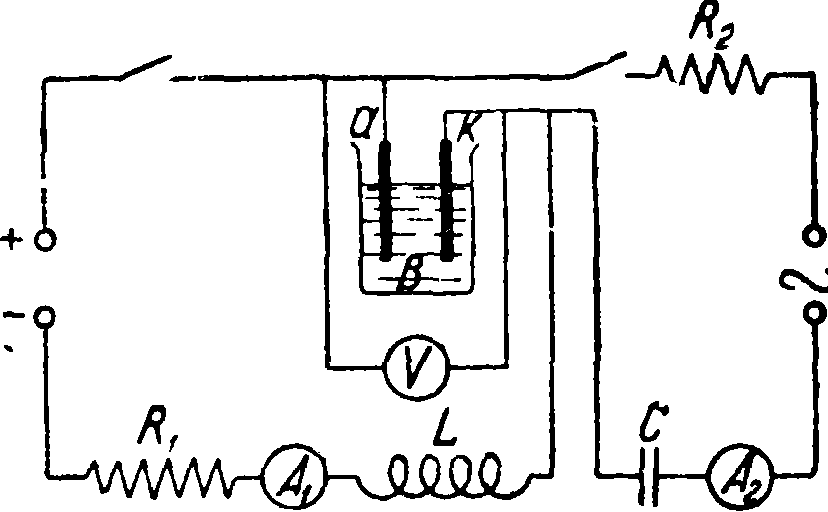
О. и. представляет большой интерес для техники сильных токов. Основные преимущества ее заключаются в следующем: исключительная теплоемкость О. и. 2 050°); хорошие диэлек трич. свойства (при t° 250° уд. объёмное сопротивление 1013 Q-см, tg δ= 0,04); процесс получения изолирующего материала и процесс изолирования проводника в этом случае соединяются в один простой технология, процесс электролиза; уменьшение веса и высокий коэф. заполнения паза. Для получения О. и. употребляют в качестве электролита водный раствор H2S04 (1 N~й концентрации); Н2С204 (2 N-й концентрации); Сг03— 3% и др. Электролиз ведется постоянным или переменным током, а еще лучше при одновременном действии обоих видов тока. Схема наложения токов показана на фигуре (В — ванна, а —алюминиевый электрод,к— катод, В!, R£ — сопротивления, L—дроссельная катушка, С — конденсатор). Наложение токов наиболее благоприятно для электролитического окисления в Н2С204, а для H2S04выгоднее и удобнее употреблять один переменный ток. При этом вторым электродом служит графит. Диэлектрич. свойства О. и. зависят от рода, концентрации и t° электролита, состава алюминия, вида и плотности тока и количества протекшего электричества; t° наиболее выгодно поддерживать 25—30°. Для получения более гибкой изоляции полезно содержание в алюминии 2—5% меди. Более толстую О. и. с пробивным напряжением порядка 9 kV и более можно получить в горячем электролите, но только на пластинах. Такая изоляция очень хрупка и отслаивается. О. и. на проволоке напряжением выше 400 V имеет продольные трещины. Поверхность алюминия предварительно протравливается в 10%-ной КОН и тщательно вымывается дистиллированной водой. После электролиза О. и. отмывается от остатков электролита в горячей воде и высушивается. С целью равномерного покрытия алюминия электролит необходимо во время электролиза перемешивать. Перемешивание осуществляется продуванием сжатого воздуха через отверстия стеклянной трубки, погруженной в электролитич. ванну. Постоянная t° электролита поддерживается либо путем пропускания проточной воды через алюминиевый змеевик, погруженный в ванну, либо применением проточного электролита.
О. и. чрезвычайно гигроскопична. В атмосфере 100%-ной влажности она поглощает до 35% воды. Диэлектрич. свойства несушеной О. и. обусловливаются водой, абсорбированной ею. Зависимости уд. сопротивления о и tg угла потерь несушеной О. и. на алюминии от t° при атмосферном давлении приведены в таблице 1. Уменьшение потерь и проводимости с повышением температуры обусловливается удалением с поверхности и из пор О. и. Рентгеновский анализ показывает, что структура О. и.—мелкокристаллич. модификация А1203. Микроструктура О. и. такова: у самой поверхности алюминия откладывается плотный слой толщиной в несколько а на него уже
Табл, i3 а в и си м о с т ь электрич. сопротивления и диэлектрических потерь в О. и. от 4°.
| 4е | Q | tg б | е | Примечание |
| 18 | 9,5 - 1G8 | 0,2
1 |
1 | Для оксидных пленок, полученных в Н2С2О4 |
| 67 | 1,3. 1012 | 0,0683 | 5,46 | |
| 120 | 2,6. 1013 | 0,024 | 5,9 | |
| 180 | 1,4. 1013 | 0,0315 | 5,31 | |
| 255 | 8,8 - 1012 | 0,046 | 5,46 | |
| 360 | 4,4 - Ю10 | 0,2 | — | |
| 242 | 9,6 - 1012 | 0,044 | 5,78 | |
| 166 | 3 ’
о со со |
0,019 | 5,31 | |
| 84 | 1,8. 1014 | 0.011 | 5,18 | Охлаждалось в полуоткрытой печи |
| 20 | 1,2. Ю10 |
откладывается более толстый и сильно пористый слой. Электрич. прочность О. и. порядка 100 Ч-300 kY/сж2. Она не зависит от t° вплоть до 500°. Явления теплового пробоя не наблюдается. Компаундирование парафином или маслом предварительно высушенной в вакууме О. и. повышает электрич. прочность в несколько раз. Заполнение пор сжатым газом также повышает прочность — при 14 atm в 2—3 раза. Толщина
О. и. может быть измерена тремя способами:
1) в случае тонких слоев — по интерференционной окраске, 2) измерением на поперечном шлифе и 3) непосредственным измерением слоя, отделенного от металла микрометром. Последний способ— наиболее удобный. Для отделения О. и. от алюминия окисленная платина погружается в сернокислый алюминий, через который пропускается постоянный ток. Пластинка со слоем окиси служит катодом. Через 1—2 мин. О. и. отделяется от алюминия отдельными кусочками; f электролита при этом 50—60°.
Главным недостатком О. и. является ее хрупкость, возрастающая с увеличением толщины изоляции. При изгибах она образует трещины до поверхности металла, видимые даже невооруженным глазом. Этот недостаток в сильной степени ограничивает возможность применения О. и. в технике. Для получения в проводах менее хрупкой О. и. применяется способ изгибания проволоки в электролитич. ванне во время окисления. Образующиеся при этом трещины заполняются также окислом алюминия. Оксидированные провода при изгибе на десятикратный собственный диам. теряют электрич. прочность порядка 10 — 20% от начальной. Применение для электролиза токов высокой частоты также уменьшает хрупкость О. и. Твердость О. и. тождественна с корундом 9 по шкале Моса. Примерный росход электрич. энергии (в kWh на 1 м2) при электролитич. окислении приведен в таблице 2.
Таблица 2. —Расход энергии при электролитическом окислении (kWh/At2).
| Пробивное напряжение в Y | Для
1 по сто ян. формир. тока |
Для постоян. и перем. одноврем. | Для · перем. формир. тока |
| 300 | 7,3 | 10,6 | 15,7 |
| 400 | 14,0 | 20,0 | 35,3 |
| 500 | 22,1 | 31,3 | 45,4 |
Несмотря на хрупкость и гигроскопичность О. и. оксидированный алюминий может найти применение для следующих целей: а) обмотки в трансформаторах (ВЭИ построены с О. и. опытный силовой трансформатор 6 600/380 У, 20 kVA; сварочный трансформатор 220/65 У, 15 kVA);
б) обмотки в электродвигателях, подъемных электромагнитах и других машинах и аппаратах;
в) обмотки катушек в электроизмерительных приборах; г) в качестве междувитковой изоляции в роторах турбогенераторов; в этом случае может быть либо оксидирована сама обмотка либо применяться в качестве прокладки оксидированная алюминиевая лента; д) обмотки электронагревательных приборов как широкого потребления (бытовых), так и специальных назначений; в этом случае оксидированный алюминий заменяет импортный нихром; е) конденсаторы (в особенности выгодно для низковольтных) для постоянного тока, а также для компенсации сдвига фаз в установках переменного тока.
Лит.: Гюнтершульце А., Электрические выпрямители и вентили, пер. с нем., 1 изд., М.—Л., 1932; Г у т и н С., Электрические свойства оксидной изоляции на алюминии, «Журнал технич. физики», 1933, т. 3; Т а р e е в Б., Оксидная изоляция и ее значение для электропромышленности, «Электричество», 1933; Александров Н., Дружинина В. и Соколов Н., О свойствах оксидной пленки и способах ее получения, там же, 1933; Степанов Д. и др., К вопросу об электролитическом получении окисных пленок на алюминии, «Журнал физической химии», 1933; Вальтер А. и др., Электролитическая оксидация алюминия переменным током высокой частоты, там же, 1933; Seton а. М i у a t a, «Report of Inst, of Phys. a. Chem. Research», Tokyo, 1926; G-ϋ n t e r-schulze A. u. Betz H., Die Oxydschichte von Sb, Bi, W, Zr, Al, Zn, Mg, «Ztschr. f. Elektrochem.», Lpz., 1931; D obi as А., К r a m p L. u. Lebedinskaya O., Eine elektroosmotische Theorie des elektro-lytischen Gleichrichters, «Ztschr. f. Phys.», B., 1930; Edwards J., Tasterund M. a. Work H., Oxide Coatings on Aluminum, «Trans, of the Am. Inst, of El. Eng.», N. Y., 1934, 4; Burgers W., C las-sen A., Z e r n i k e J., Uber die chemische Natur d. Oxydschichten, welche sich bei anodischer Polarisation auf den Metallen Aluminium, Zirkon, Titan u. Tantal hilden, «Ztschr. f. Phys.», B., 1922; Rohrig H., Elekt-rolytisch erzeugte oxydische Schutzschichten auf Aluminium, «Ztschr. f. Elektrochem.», Lpz., 1931. С. Гутин.