 > Техника, страница 76 > Растворы твердые
> Техника, страница 76 > Растворы твердые
Растворы твердые
Растворы твердые. Аналогично жидкостям способность к взаимному смешению и образованию однородных растворов распространяется также и на твердые кристаллич. вещества. Такие твердые фазы, в которых от-
ношения между составными частями (компонентами) могут изменяться без нарушения однородности, Вант-Гофф (1890 г.) назвал твердыми растворами. Однородные смеси твердых аморфных тел должны рассматриваться как жидкости с больцхим внутренним трением. Но опыт показывает также, что и типич. кристаллич. вещества образуют однородные смеси в различных пропорциях, или т. н. смешанные кристаллы. В подобных системах не только жидкие, но и твердые фазы имеют переменный состав. Темп-ра застывания жидкого раствора лежит ниже 1°зтт. чистого растворителя; это понижение называется депрессией. При кристаллизации из раствора чистого растворителя име-. ем по формуле Рауля-Вант-Гоффа
to ~ ϊχ "м ’
где t0 и tx—соответственно темп-ры замерзания растворителя и жидкого раствора с концентрацией х, М—мол. в растворенного тела и к— коэф., зависящий от природы веществ: Образование Р. т. вызывает аномалии в величине депрессии по указанной формуле для жидких растворов и тогда д, б. применена более общая формула (Ротмунд):
где х и xs—концентрации растворов жидкого и твердого. При этом можно различать несколько случаев. 1) Если а"г> то разность io — tx, или депрессия, представляет положительную .величину, τ, е. наблюдается понижение 1°пл, растворителя. 2) Когда хг<х3, депрессия имеет отрицательное значение, что указывает на повышение 1°пл. растворителя при образовании Р. т. Соответствующие примеры встречаются довольно часто среди металлич. сплавов (Sn-Sb, Cu-Zn, Tl-Pb). 3) При а,=0 Р. т. отсутствует, и получаем в частном случае величину депрессии по формуле Рауля-Вант-Гоффа. 4) Наконец, когда хг=х$, депрессия равна 0 и ta=tx, то есть 1°жт. растворителя сохраняется постоянной для всех концентраций растворов. Такой случай наблюдается в неметаллич. системах при взаимном растворении. правой и левой модификаций оптич. изомеров (Розебум). В ненормально малых величинах криоскопии, депрессии растворителя мы имеем количественный признак, которым многие исследователи пользовались для отыскания Р. т.
Приложение методики физико-химич. анализа раскрывает с несомненностью сутцество-в’ание аналогий между жидкими и твердыми растворами, причем оказывается, что последние имеют громадное распространение среди веществ, находимых в природе и.получаемых искусственно. Образование Р. т. находится в зависимости от ряда факторов, из которых главнейшие: t°, строение кристаллич. решеток и полиморфизм.
Повышение температуры увеличивает подвижность частиц, облегчая способность к диффузии и получению однородных смесей. Близость кристаллических решеток также очень важный фактор смешения в твердом состоянии. При одинаковых основных кристаллографии. формах получаются непрерывные изоморфные смеси во всех пропорциях (аналогично жидким системам вода—); близость же основных кристаллич. типов делает возможным взаимное подчинение в известных пределах решеток самых разнообразных веществ и образование Р. т. до нек-рых предельных концентраций (последние тела аналогичны жидким смесям с ограниченной растворимостью, например вода—эфир).
Непрерывные Р. т. или изоморфные смеси веществ с одинаковыми или близкими кристаллографии, формами, представляют, как указано, предельную группу; кривые охлаждения таких растворов (фигура 1),
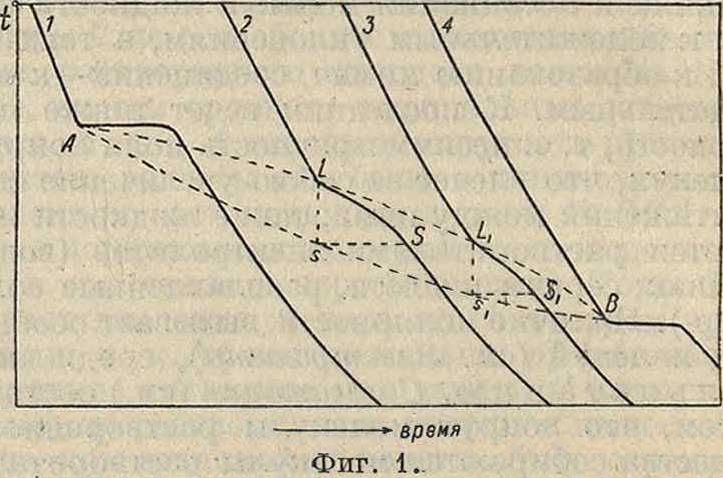
зафиксированные на регистрирующем пирометре, имеют характерный вид—они отличаются отсутствием эвтектич. остановки. Застывание двойных сплавов происходит здесь нацело в однородную массу, и кривые охлаждения (фигура .1, кривые 2 и 3) состоят из двух ветвей, соединенных наклонными отрезками LS и LjSj. Точки L ι I, принадлежат переменным темп-рам начала выделения первых твердых кристаллов сплава, a S и St—температурам конца выделения кристаллов; при этом вертикальные расстояния Ls и LjSj определяют i°-Hbie интервалы затвердевания жидкой смеси. Геометрич. места точек L, Ьг и s, sxдают непрерывные линии ALL-J3 (л и к в и-дус, liquidus) и AssJI (с о лид у с solidus), к-рыми характеризуется разрыв сплошности между жидким и твердым (кристаллическим) состоянием данной двойной системы. Для чис-. тых компонентов А и В интервал кристаллизации равен нулю (фигура 1, кривые 1 и 4); при образовании сплавов он постоянно воз
Фпг. 2.
растает, достигая нек-рого максимума Ls во внутренней части диаграммы.
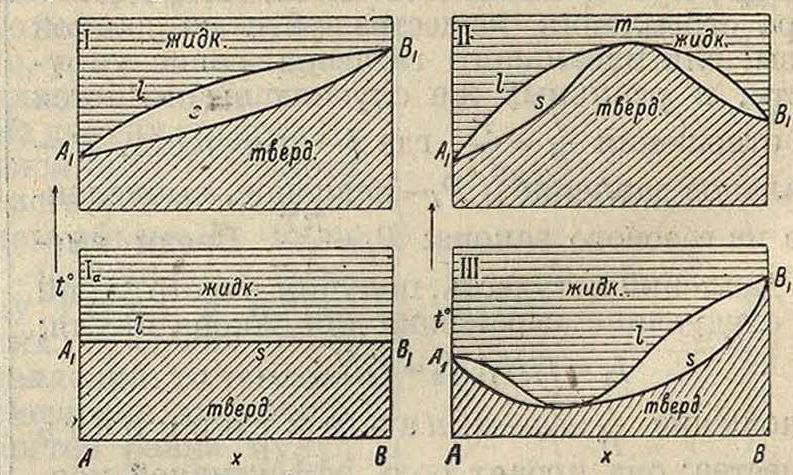
Термин, анализ непрерывных Р. т. устанавливает четыре главных типа диаграмм, различающихся формой линий I (liquidus) и s (solidus) (Розебум, 1899 г.): 1) t „л, смесей лежат между ί°„. компонентов (фигура 2,I); 2) линии I и s имеют 4°-ный максимум (фигура 2, II); 3) линии ins имеют 4°-ный минимум (фигура 2, III); 4) линии I и s совпадают в одну прямую (фигура 2, 1а), параллельную оси кои-
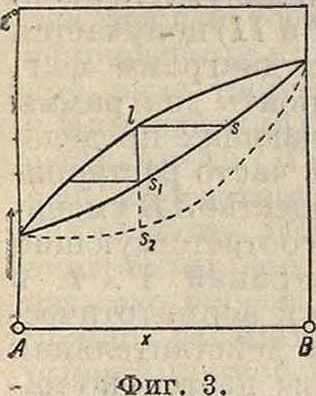
центрации, то есть £°ил. смеси постоянна; такую диаграмму можно считать разновидностью типа I для случая, когда t°nl- компонентов i и В равны (в.металлич. системах пока неизвестны). Типы! и III наиболее распространены. К первому относятся изоморфные смеси металлов Ag-Au (Гейкок, Невиль и др.), Bi-Sb (Готье и Шарли), 1п-Т1 (Курнаков и Путин), Au-Pt (Деринкель), Mn-Fe (Левин и Тамман), Си-Ni (Курнаков и Жемчужный) и др. Представителей Р. т. типа III с минимумом имеем в системах Au-Cu (Курна-коз и Жемчужный), Cu-Mn (Жемчужный, Ура-зов и Рыковсков) и др. Непрерывные изоморфные смеси типа II свойственны гл. обр. органическими веществам. Из металлических сплавов можно указать на Т1-РЬ (Курнаков и Пущин), встречающийся в данном случае при Р. т. с разрывом сплошности (смотри далее). При изучении указанных четырех типов обнаруживается глубокая аналогия между твердыми и жидкими растворами. В применении к Р. т. имеют место след, положения: а) Кристаллизация растворов при постоянной t°, то есть когда £°-ный интервал равен нулю, наблюдается только в минимумах или максимумах диаграмм. В этих точках линии Ins имеют одну общую касательную, и.составы твердой и жидкой фаз равны между собой, б) Первые выделения кристаллов Р. т. содержат избыток того компонента, прибавление которого повышает f твердой фазы. Так например, жидкий сплав I выделяет при охлаждении первые кристаллы, определяемые точкой s (фигура 3), при дальнейшем понижении температуры перемещающейся в sx, где происходит окончательное затвердеваниежид-кости в однородную массу. При быстром охлаждении кристаллы Р. т. могут не успеть выравнять свой состав, и тогда сплав затвердевает в неоднородный комплекс (послойная, или зональная, структура). Для подобных неравновесных состояний температурный интервал кристаллизации ls2 является увеличенным сравнительно с нормальным Zs2. При достаточно медленном охлаждении сплава или его отжиге при £° несколько низшей, чем £° окончательного затвердевания, происходит взаимная диффузия отдельных слоев и образование однородных кристаллич. зерен Р. т. Подобный процесс имеет важное значение в технике.
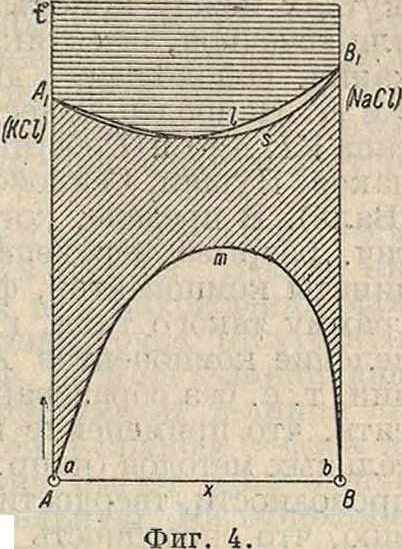
Разрывы сплошности Р. т. Еще чаще, чем для жидкостей, на твердых двойных системах проявляются разрывы сплошности. Устойчивость Р. т. зависит согласно принципу Ле-Шателье-Вант-Гоффа от теплового эффекта их образования. Системы с положительным тепловым эффектом остаются устойчивыми при понижении £° и сохраняют свою однородность. Наоборот, непрерывные Р. т., образующиеся с заметным поглощением тепла, распадаются при охлаждении на два раствора с ограниченной растворимостью (фигура 4). Предельная точка m устойчивого существования Р. т. во всех пропорциях вполне аналогична верхней критич. точке растворения жидких смесей. Если предположить, что кривая распадения amb перемещается вверх до пересечения с s-линиями А1В1 диаграммы I и III
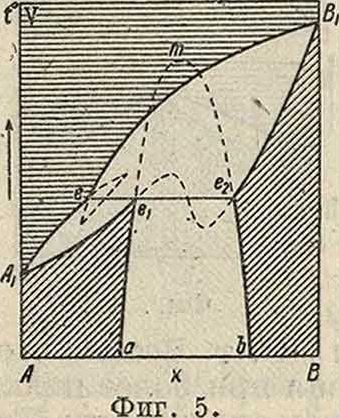
фигура 2, то получаются весьма распространенные типы (фигура 5. и 6) образования Р. т. с ограниченной растворимостью.
Фигура 5 характеризуется существованием переходной точки е, лежащей на горизонтальной линии ee-fiz разрыва сплошности. На участке еге2 наблюдается разрыв линии s твердых растворов Л1е1е2В1, состоящей из двух ветвей Ахег и е2Вг, соединенных друг с другом вол-нообразным отрезком (серпантином) неусгтойчивых равновесий.
Прилагая по Ван-дер-Ваальсу принцип непрерывности также к 1-линии А 1еВ1 жидкой фазы АгеВл, можно предположить, что обе ее ветви Аге и eBlt пересекающиеся в переходной точке е, связаны между собой при посредстве неустойчивого узла (с Двумя точками возврата), показанного нафигурабпунк-тиром. Кривые охлаждения составов, принадлежащих линии разрыва ее2, имеют две остановки: верхняя наблюдается при переменных t° и указывает начало выделения кристаллов твердого раствора А в компоненте В; нижняя соответствует застыванию жидкого сплава при постоянной темп-ре в смесь двух Р. т., принадлежащих предельным концентрациям е1и е2 разрыва твердой фазы. В качестве примера для Р. т. типа V с разрывом в переходной точке можно привести Hg-Cd (Бийль), 1п-Т1 (Курнаков и Путин), Си-Со (Замен, Н. Константинов), Ag-Pt (Деринкель, Курнаков и Немилов).
Фигура 6 (тип VI) представляет сочетание диаграмм фигура 4 с фигура 2 (тип II) и определяется нахождением эвтектической точки Е на горизонтальной прямой разрыва еех сплошности Р. т., предельные концентрации которых указываются устойчивыми отрезками ае и bе7 кривой распадения атЬ. Кривые охлаждения составов, отвечающих двум областям существования Р. т. В в А
ФПГ. 6.
а А в В, имеют, нормальный вид с переменным интервалом кристаллизации (фигура 1, 2 и 3). На кривых охлаждения сплавов в области разрыва eej наблюдаются кроме изломов начальной кристаллизации весьма характерные остановки, при постоянной t°sabm. эвтек-тич. смеси двух Р. т. с предельными концентрациями е и с,. Если отложить по Тамману на перпендикулярах к эвтектич. линии отрезки, пропорциональные продолжительности соответственных эвтектич. остановок, то получается треугольник (фигура 6), вершины
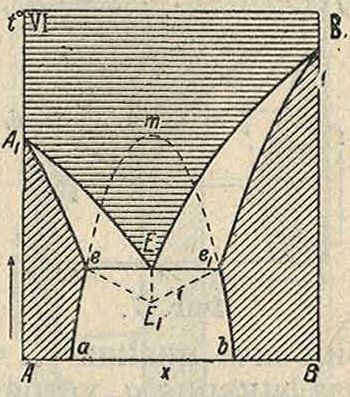
к-рого е я ег не доходят до ординат А А х и ВВХ компонентов системы. В подтверждение данных термин, анализа микрографическое рассмотрение затвердевшего и приведенного к равновесию сплава указывает на полную однородность криста л лич. зерен без всяких прослоек в области Р. т., образуемых компонентами А и В; для концентрации в пределах разрыва ее1 характерно нахождение в промежутках между кристаллами А и В слоистой, или точечной, эвтектики, представляющей ме-ханич. соположение двух предельных Р. т. ей е,. Наиболее известные примеры систем типа VI: Ag-Cu (Робертс-Аустин, Осмонд, Кур-наков, Путин, Сенковский и другие), Aii-Co (Валь). В пределе, когда точки е и ех эвтек-тич. разрыва перемещаются на крайние ординаты компонентов, фигура 6 переходит в диаграмму такого типа, где предполагается выделение компонентов А я В в чистом состоянии, то есть без образования Р. т. Нужно заметить, что применение новых, более чувствительных методов (например определение электропроводности, твердости) приводит к заключению, что способность к взаимному растворению в твердом состоянии является общим свойством вещества.
Полиморфизм Р. т. Способность твердых тел давать несколько кристаллич. полиморфных видоизменений (а, β, γ, .) обусловливает большое разнообразие во взаимных превращениях Р. т.; по аналогии с превращением жидкий раствор твердый раствор можно рассматривать и соответствующие превращения одной твердой модификации в другую, например:
α-твердый раствор Д: /3-твердый раствор.
На фигуре 7 изображен переход непрерывного у-Р. т. (тип I, фигура 2) во второй—непрерывный ряд также типа I, свойственный ^-модификации компонентов А и В, устойчивый
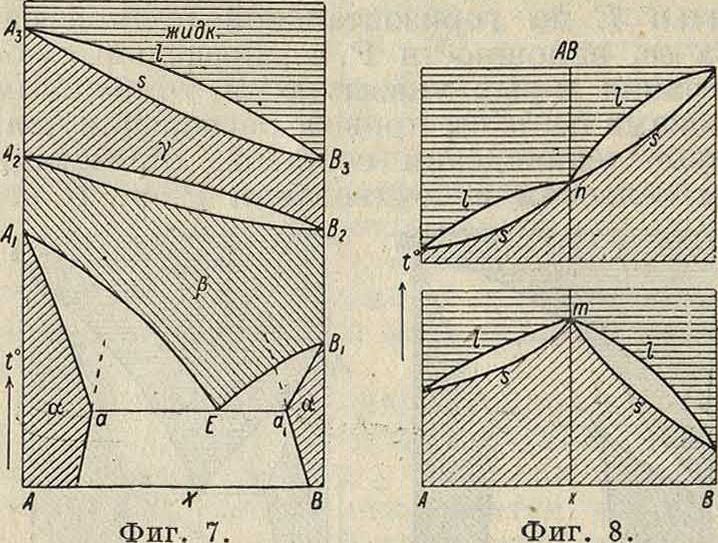
при более низких ί°, чему-Р. т. Весьма часто модификация а, устойчивая при более низких f, образует Р. т. с разрывом сплошности. Так, схема на фигуре 7 (нижняя часть) относится к подобному превращению β ^ а. Здесь точка Е, лежащая на пересечении кривых распадения АХЕ и ВгЕ, отвечает наиболее низкой t° устойчивого существования непрерывных изоморфных смесей /S-модификации. Горизонтальная прямая аЕау определяет границы разрыва сплошности α-модификации. По сходству с эвтектич. точкой, отвечающей минимальной кристаллизации жидких растворов, точка Е получила название эвтектоидной точки [Гоу (Howe)].Соответствующий затвер девший сплав, ниже эвтектоидной температуры, состоит из перемежающихся слоев двух твердых растворов, образованных a-модификациями компонентов А и В.
Р. т. и определенные соединения. Для по-знашАя сущности химич. превращений особенно важны те равновесия, где одновременно с Р. т. наблюдается образование определенных соединений, состав которых подчиняется закону постоянных и кратных отношений Пру-Дальтона. Рассмотрим случай, когда определенное соединение АВ, не диссоциированное как в жидкой, так и в твердой фазе, дает непрерывные Р. т. с компонентами А и В. При таких условиях вещество АВ можно считать самостоятельным компонентом и диаграмма (ж, t) системы A-В распадается на две подчиненные (вторичные) диаграммы А-АВ и АВ-В с общей ординатой, принадлежащей соединению АВ. На фигуре 8 (I и II) изображены равновесия, в которых А В лежит: I—меж-ду {°вд. компонентов А я В я II—выше этих f. Соответствующие сингулярные (особенные) точки соединения п и m расположены на пересечениях двух пар предельных линий жидких растворов I, 1~я твердых растворов s, s. В точках п я т к названным линиям можно провести по четыре касательных. Поэтому сингулярная максимальная точка т, характеризующая определенное соединение АВ на диаграмме (фигура 8, II), отличается по существу от иррационального максимума ш Р. т. (фигура 2, II), где I- и s-линии имеют одну общую горизонтальную касательную. Подобно тому как диаграмма фигура 8 (I и II) получается попарно из соответствующих диаграмм фигура 2, так же точно можно построить диаграммы для компонентов Р. т., обладающих предельными концентрациями. Очень часто растворимость компонентов А и В в веществе АВ уменьшается с понижением t°, и соответствующие кривые предельных концентраций Р. т. в a-модификации приближаются асимптотически к общей ординате. Тогда действительная протяженность состава a-фазы настолько мала, что м. б. изображена точкой на оси состава ж, отвечая в данном случае закону кратных отношений Дальтона, то есть образованию определенного соединения.
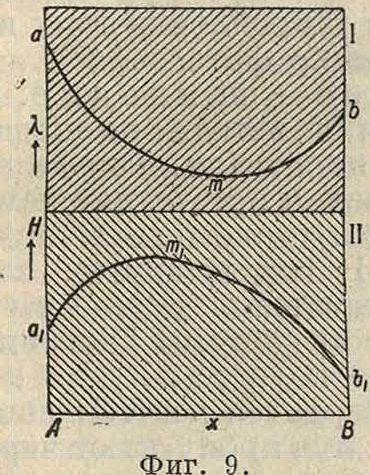
Диаграммы «с о с т а в-с в о и с т в а» Р.т. Образование однородных кристаллич. комплексов при взаимном растворении отражается весьма ясно на многих свойствах двойной системы. Аналогично случаю жидкостей соответствующие диаграммы изоморфных смесей м. б. представлены непрерывными кривыми. Так, изменения уд. объёмов, констант основной кристаллич. решетки, модуля упругости выражаются линиями, близкими к прямой. Гораздо более резко сказывается образование Р. т. на двух обширных группах свойств вещества—на электрич. свойствах и свойствах, обусловленных силами молекулярного сцепления. Для металлич. сплавов особенно характерны диаграммы электропроводности или ее обратной величины"— электросопротивления, а также твердости и «давления истечения». Опыт показывает, что образование металлич. Р. т. сопровождается: а) уменьшением электропроводности /. и б) увеличением твердости Н. Принимая во внимание эти положения, получаем три типич. диаграммы (ж, X) и (ж, Н), изображенные на фигуре 9, 10 и 11 (Курнаков и Жемчужный). 1) Фигура 9
(I,II) принадлежит непрерывной изоморфной смеси двух компонентов А и В и характеризуется непрерывными кривыми аЬ и а1Ь1, из которых первая обладает минимумом электропроводности т, а вторая—максимумом твердости г»!. Легко видеть, что диаграмма твердости представляет как бы обращенную диаграмму электропроводности, но минимум т и максимум пь1 могут отвечать неодинаковым составам. По аналогии с жидкими растворами повышение t° должно делать изотермы более плоскими и смещать минимальную точкут (фигура 9, I) в сторону компонента, обладаю-
Фигура 10.
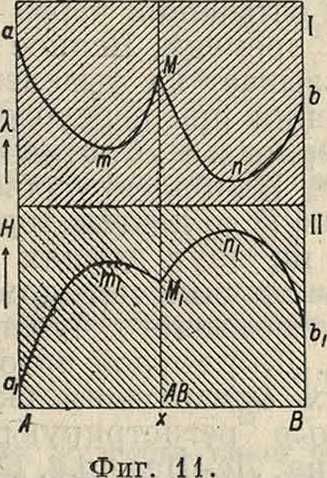
щего меньшей электропроводностью; такое отношение наблюдалось в действительности для нек-рых изоморфных смесей, например для сплава K-Rb (Курнаков и Никитинский). При тех же условиях максимум твердости т1 (фигура 9, II) будет перемещаться по направлению более твердой составляющей сплава. Подобные непрерывные кривые были определены на целом ряде твердых систем: K-Rb (Курнаков и Никитинский), In-Pb (Курнаков и Жемчужный), Ag-Au (Матиссен, Курнаков, Жемчуж-· ный и Зедстрем). 2) При наличии разрыва сплошности изоморфной смеси имеют место диаграммы (фигура 10, I, II), состоящие из трех взаимно пересекающихся линий. Этот случай можно рассматривать как сочетание непрерывной кривой Р. т. (фигура 9) с прямолинейной диаграммой механической смеси двух твердых веществ. Понижающиеся ветви ас и Ьс1 (фигура 10, I) и подымающиеся кривые а^ и Ojdi (фигура 10, II) указывают на непрерывное уменьшение электропроводности и увеличение твердости до предельных концентраций Р. т. 6 точках с и d. Средний прямолинейный участок cd принадлежит сплавам в области разрыва сплошности, представляющим меха-нич. смеси, двух предельных концентраций Р. т., из которых состоит затвердевшая система на протяжении разрыва СВ. Из наиболее известных комбинаций к этому типу относятся сплавы Ag-Cu (Курнаков, Пущин и Сен-ковский), Ag-Pt (Курнаков и Немилов), Си-Со (Рейхардт). 3) Если недиссоииированное в твердой фазе определенное соединение АВ (фигура 11, I) дает непрерывные Р. т. со своими компонентами А и В, то на основании указанного выше положения его электропроводность λ должна понижаться от прибавления А и В. Получающаяся диаграмма состоит из двух ветвей атМ и Мпb, обладающих минимумами ж и и и пересекающихся под углом в сингулярном максимуме М, к-рый отвечает составу соединения АВ. Очевидно, что соответствующие кривые твердости а1т1М1 и М1п1Ь1 (фигура 11, II) должны иметь обратный вид и взаимно пересекаться в сингулярном минимуме Мг,
находящемся между двумя максимумами тги п,_. Характерные диаграммы (фигура 11, I, II) указывают систематич. путь для нахождения интерметаллич. соединений(металлидов), образующихся при разнообразных превращениях жидких и твердых растворов. Т. о. были открыты медные ауриды CuAu и Cu3Au (Курнаков, Жемчужный и Заседателев; Седстрем; Иогансон и Линде), ауриды AuR и Au3R, где R-Zn и Cd (И. Сальдау), палладид меди CuPd (Седстрем) и определены границы существования одномагниевого кадмида MgCd (Г. Уразов) и ферроплатинида FePt (В. Немилов), которые были найдены ранее Грубе и Исааком с Тамманом при посредстве термического анализа.
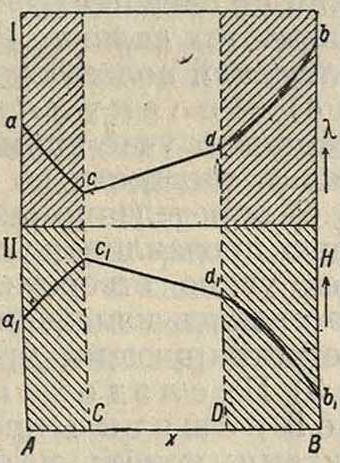
Отсутствие сингулярной точки на линиях свойств. Весьма интересен случай, когда при нахождении максимума t°nA. сингулярная точка отсутствует не только на ϊ-кривой, но и на s-линии диаграммы; тогда в максимуме М s-линия касается соответствующей ί-кривой. (у-фаза на фигуре 12, I), и обе линии имеют одну общую горизонтальную касательную. На основании предыдущих соображений ясно, что состав подобного максимума не отвечает рациональному отношению компонентов и не подчиняется закону постоянных кратных отношений Дальтона. В соответствии с этим имеет место отсутствие сингулярных точек и на диаграммах других свойств затвердевших сплавов такой системы. Так, кривая ее1 (фигура 12, II) электропроводности λ идет непрерывно на всем протяжении состава у-фазы; максимальная точка ег находится на пересечении ветви еег с прямолинейным отрезком е1Ь1 разрыва сплошности и отвечает предельной концентрации Р. т. компонента В в у-фазе. Эта концентрация может меняться в зависимости от температуры и других факторов равновесия. Примеры подобных индивидуальных веществ с иррациональными максимумами 1°пл. найдены в системах Tl-Hg (Курнаков и Пущин), Ί1-Bi (Курнаков, Жемчужный и Тарарин), Cu-Sb (Курнаков и Белоглазов). По всей вероятности такие фазы переменного состава образованы соединениями, диссоциированными
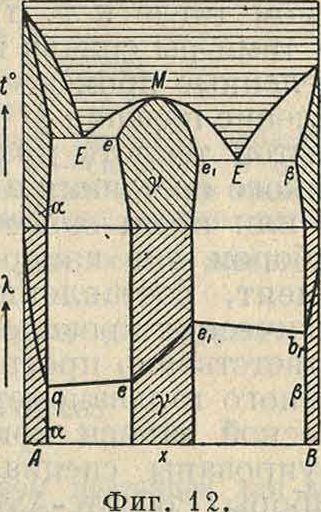
как в жидком, так и в твердом состоянии (системы бертоллидного типа—бертолли-ды); они являются представителями класса веществ, стоящих на рубеже между истинными растворами и химическими соединениями. Среди металлич. и других систем вещества подобного типа весьма распространены, особенно в области высоких f. К этой категории должен быть отнесено большинство самостоятельных твердых фаз переменного состава, которые в
двойных металлич. системах принято обозначать буквами греческого алфавита, когда не имеется возможности причислить их к определенным соединениям. Кроме упомянутых соединений таллия со ртутью и висмутом, сурьмы с медью и тому подобное. сюда относится целый ряд Ееществ((3, γ,δ и т. д.) в сплавах железа с кремнием и алюминием, меди, серебра и золота с оловом, цинком и кадмием. В последнее время подробному изучению подвергалась /S-фаза медноцинковых сплавов, входящая между прочим в состав т. н. ковкой латуни. Изменения состава этого несомненно самостоятельного индивида, лишенного сингулярных точек на линиях свойств, совершаются в очень широких пределах (35,5— 53,7% Ζη, то есть на протяжении 18%). При темп-ре ниже 450—460° названное тело превращается в новую фазу переменного состава (βL), отвечающую повидимому цинковому монокуприду ZnCu.
Приведенный фактический материал свидетельствует· о большом распространении Р. т. среди самых разнообразных классов веществ. Возможность взаимного подчинения основных решеток обусловливает совместную кристаллизацию веществ различной химической природы, благодаря чему Р. т. имеют громадное значение в природе при построении минеральных комплексов и «опорных тканей» животного и растительного организма. Аналогичную роль играют с отдаленных времен металлические растворы в технике и повседневной жизни. Названия культурных периодов в истории человечества—«бронзовая эпоха», «век железа и стали»—соответствуют умению обращаться с твердыми растворами олова и меди, никеля и углерода в железе. Систематическое исследование этой обширной области принадлежит последнему времени и тесно связано с приложением точных методов металлографии и физико-химического анализа.
Методы исследования Р. т. Главнейшие методы исследования Р. т. следующие. 1) Термический анализ (применение метода плавкости); в последнем случае исследуемый сплав расплавляется в соответственно нагреваемом тигле и тому подобное. и отмечается понижение темп-ры сплава при остывании через определенные промежутки времени. Всякоезамедление падения 1° указывает на выделение скрытой теплоты плавления при переходе из жидкого состояния в твердое и м. б. отмечено тем или иным способом. Наиболее удобным прибором для измерения t° является термоэлемент, составленный из двух тонких металлических проволок различных металлов и соответственно проградуированного чувствительного гальванометра. Для точной автоматической записи кривых охлаждения сконструированы специальные регистрирующие приборы (Робертс-Аустина, Ле-Шателье, Кур-накова и др.).
2) Электр и ч. анализ, заключающийся в измерении сопротивления ρ сплава, обычно тянутого в виде проволоки или отлитого в форме палочки. Измеряемый объект выдерживается при определенной t° в термостате, закрепленный в специальном зажиме, позволяющем точно отмечать длину проводника; сопротивление в Ω измеряется двойным листом Томсона, после чего м. б. вычислено Qt, равное сопротивлению 1 см3 сплава, электропровод ность Л= ~ и (°-ный коэф. сопротивления а:
‘ i h г
3) Микроструктура. Для изучения структуры сплава, то есть определения его составляющих в застывшем металлич. слитке, поверхность сплава шлифуется, полируется до исчезновения царапин и затем подвергается соответствующей обработке (например химич, протравливанию,рельефной полировке и тому подобное.). Рассматривая подобную поверхность при достаточном увеличении в отраженном свете, можно по внешнему виду судить о структурных элементах сплава. Для закрепления этих наблюдений пользуются микрофотографией.
4) Молекулярное сцепление. В данном случае применяют методы: а) определения твердости по Бринелю (смотрите ·Твердость) и б) определение «давления истечения» помощью продавливания испытуемого образца через узкие отверстия. В том и другом случае запись изменения давления можно вести регистрирующим прессом системы Гагарина.
5) Исследование кристаллической решетки производится рентгеновыми лучами; монохроматич. луч пропускают через помещенную в центре цилиндрич. камеры пластинку или проволоку исследуемого сплава и получают на фотографии, пленке т. н. круги рассеяния от кристаллич. плоскостей; это дает возможность определять кристаллич. формуй длину элементарного ребра кристаллов и т. о. проследить за изменением кристаллич. формы при образовании и распадении Р. т. (метод Дебая-Шерера); см. также Рентгенография.
Лит.: В иттп рф Η. М., Теория сплавов в применении к металлич. системам, пер. с нем., СПБ, 1909; Степанов Н. И., Об Электр проводности металлич. сплавов, СПБ, 1911.; К у р н а к о в Н. С., Введение в физик -химии, анализ, 2 изд., Л., 1928; его же, Раств ры и сплавы, Л., 1928; К о т ю к о в И. И., Физическая химия, Томск, 1930; К у р н а к о в Н. С. и Ж е м ч у ж н ы ii С. Ф., Твердость металлических сплав в, «Изв. Иотштехнич. пн-та», СПБ, 1908; С а л ь-д а у П. Я., Метод электропроводности при высоких температурах и его значение для выяснения прир< ды твердых растворов, «Известия Ин-та физик -химия, ана-лиза», 1924, т. 2, вып. 2;«>КРМО»; «Изв. Ин-та физико-химич. анализа»; «Изв. Ин-та по изучению платины и других благо; одных металл в», Л.; Tammann G., Lehrb. d. Metallographie, Chemie u. Phvsik d. Metalle u. ihre Legierungen, 3 Aufl., Lpz., 1923; S u Π I e t L., Les mdthodes d’etude des a 111 iges nidtallipues, P., 1923; Finlay C., Phase Rules a. Its Apnlieatl ns, L., 19°3. H. Курнзков v. Б. Ронкин.