 > Техника, страница 79 > Светящиеся составы
> Техника, страница 79 > Светящиеся составы
Светящиеся составы
Светящиеся составы, люминофоры, искусственно приготовленные составы, обладающие более или менее продолжительным свечением (фосфоресценцией), возбуждаемым различными радиациями как световыми, так и корпускулярными (смотрите Люминесценция, а также Спр. ТЭ, т. IX, Фосфоры Ленарца).
Получение «светящихся камней» было известно очень давно китайцам (976 г.). В Европе впервые в начале 17 в на явление фосфоресценции обратил внимание алхимик Винченто Кашиоролло, к-рый при поисках философского камня прокаливал тяжелый шпат из горы Монте-Патерно около Болоньи и получил вещество, названное «болонским камнем»; затем появились другие С. с., а в конце 19 в Бальмен изобрел состав, к-рый превосходил качеством остальные, Сидо получил С. с. из сульфида цинка. После установления Вернейлем причины свечения «бальменов-ской краски» и исследования С. с. Ленардом и его сотрудниками изучение явления фосфоресценции стало на твердую научную базу.
Но теории Ленарда свечение С. с. связано с фотоэлек-трич. активностью вещества: под действием радиации выделяются электроны и С. с. приобретает положительный заряд, локализованный в отдельных областях—ц е н т-р а х, состоящих из нек-рых молекулярных групп. Электроны, выбрасываемые из металлич. атомов центра, задерживаются атомами серы или другого вещества либо находятся между окружающими атомами. При возвращении электронов получается явление фосфоресценции. Ленард считает, что для каждой полосы спектра свечения имеется ограниченный (°-ный участок, на протяжении которого происходит фосфоресценция, а вне этого участка оно перестает быть деятельным. Инфракрасные лучи и подогревание увеличивают частоту столкновений в фосфбре и облегчают возвращение электронов, чем усиливается яркость свечения и уменьшается его продолжительность. В нек-рых случаях красные и инфракрасные лучи тушат свечение, то есть уменьшают его «световую сумму». Необходимым условием возникновения фосфоресцирующего центра является кристаллич. структура, что следует из данных рентгеновского анализа фосфбров. В теории, недавно предложенной Томашеком, предполагается, что металлич. атом центра внедряется в кристаллич. решетку сульфида (или другого соединения), сильно деформируя ее и разрыхляя. Эта деформированная решетка начинает поглощать свет, являясь т. о. первичным аккумулятором световой энергии в фосфбре. При поглощении света в решетке происходит внутренний фотоэлектрич. эффект. Время, протекающее между выбрасыванием электрона и его возвращением, определяет в основном длительность фосфоресценции. При возвращении электрона в решетку энергия последней передается металлич. атому, к-рый, возбуждаясь, излучает затем через очень короткое время квант света, соответствующий фосфоресценции. Так. обр. по Томашеку поглощающая и излучающая части центра разъединены, причем роль первой играет кристаллич. решетка, роль второй — металлич. атом. В некоторых случаях металлич. атом поглощает свет непосредственно, излучая его через очень короткое время, при этом получается кратковременное евечение (флуоресценция). Изложенные представления являются только качественными гипотезами; до сих пор нет точной теории С. с. несмотря на колоссальный экспериментальный материал, касающийся спектров излучения и возбуждения фосфбров, их законов затухания и других особенностей.
Все известные фосфоресцирующие вещества м. б. разделены на два класса: сложные ф о с-ф ό р ы, фосфоресценция которых обязана нали-
чиго в основном веществе следов определенных элементов или соединений, и простые С. с., которые в чистом виде обладают люминесцирую-щими свойствами. С. с. первого класса представляют собою твердые растворы, состоящие из основания —главной массы основного вещества, фосфорогена — ничтожно малого количества активного металла или соединения, присутствие которого дает явление свечения, иногда у с и л и т е л я —небольшого количества редкого металла, усиливающего действия фосфорогена, и плавня — вещества, способствующего введению и равномерному распределению фосфорогена и образованию твердого раствора.
Сила свечения С. с. обладает максимумом, пределы которого зависят от интенсивности, активности падающей радиации и продолжительности ее воздействия. Различные С. с. неодинаково реагируют на различные лучи; одни хорошо возбуждаются от действия дневного света, другие от искусственного; особенно яркое свечение у большинства составов вызывают ультрафиолетовые лучи. Нек-рые составы чувствительны кроме того к катодным, X-лучам или радиоактивным излучениям. Свойства С. с. при данном основании зависят от типа и количества добавок, а также от метода приготовления, что учитывается при подборе рецептуры для определенного назначения. Продолжительность инсоляции различных С. с. при данном источнике света различна; у некоторых возбуждение достигает максимума почти мгновенно, другие требуют нескольких ск. Если состав нанесен на поверхность, то продолжительность инсоляции зависит также от толщины и шероховатости поверхности слоя С. с. Период свечения у различных составов весьма разнообразен. С. с., перенесенный внезапно в темноту, сначала светится очень ярко, затем сила свечения резко падает, а потом постепенно уменьшается до полного загасания; оно наступает у некоторых составов через значительный промежуток времени, измеряемый десятками часов. Нормально у хороших С. с. достаточно яркое свечение при f 15° продолжается 1 -f- 2 ч. После угасания С. с., выставленный на свет, опять заряжается на тот же период времени. Все С. с., свечение которых продолжается ограниченное время, то есть требующие периодич. зарядки, называются С. с. временного действия. Если же состав может возбуждаться от радиоактивных излучений и в него введено радиоактивное вещество в виде механич. примеси, то благодаря постоянному воздействию лучей состав светится беспрерывно, не требуя предварительной зарядки. Время свечения такого состава измеряется годами; оно зависит только от периода жизни радиоактивного вещества и от разрушения основания под действием постоянной радиации. Такие С. с. называются радиоактивными, или постоянного действия. Инфракрасные лучи или подогревание оказывают влияние на свечение С. с., изменяя интенсивность (поглощенная световая энергия начинает излучаться быстрее), и поэтому С. о. светит более короткое время, но ярче; когда свечение С. с. почти незаметно для глаз, при подогревании оно вспыхивает вновь за счет выделения остатка световой энергии; вторичное подогревание уже не дает свечения и требуется новая зарядка. В других случаях длинноволновые лучи тушат фосфоресценцию без ускорения высвечивания.
Область применения С. с. сравнительно ограничена несмотря на то, что казалось бы их мож но широко применить в различных областях жизни, например для освещения помещений холодным светом, для вывесок, надписей и т. д. Однако, так как яркость фосфоресценции сравнительно слаба и кроме того свет виден лишь в ближайшее время после освещения, то после дневной зарядки состав разряжается в период сумерок и к моменту наступления темноты свечение незаметно. С. с. могут быть применены с пользой в тех случаях, когда не требуется длительного и яркого свечения, например для спасательных морских кругов, буйков, для надписей в театрах, для театральных эффектов, для украшений и прочие Радиоактивные составы в виду высокой стоимости имеют применение только для приборов, к-рыми приходится пользоваться в темноте (часы, компасы), и для научных приборов.
По химич. составу С. с. первого класса делятся на ряд групп с различными основаниями:
1) с основанием из сульфидов щелочноземельных металлов или их смесей, которые дают многочисленные, очень яркие С. с., с разнообразным цветом свечения, возбуждающиеся от дневного искусственного освещения и от ультрафиолетовых лучей; 2) с основанием из селенидов, окисей или углекислых солей тех же металлов;
3) с основанием из сульфида цинка, очень яркие С. с., с зеленым, зелено-голубым, желтым и оранжевым цветом свечения, возбуждающиеся как от световых лучей, так и от радиоактивных излучений; 4) с основанием из кремнекислого цинка, с зеленым, желтым и оранжевым цветом свечения, чувствительные к катодным и Х-лучам; 5) борнокислые С. с. с ярким различных цветов свечением, возбуждающиеся световыми лучами. Ко второму классу С. с. относятся: платиново-синеродистый барий и платиново-синеродистый кальций е зеленым свечением, возбуждающиеся от β-, γ- и Х-лучей; платиново-синеродистый натрий, дающий светложелтое свечение от β-лучей; платиново-синеродистый литий, чувствительный к X- и /?-лучам с красным цветом фосфоресценции, вольфрамовокислый кальций, светящийся от X-лучей и излучения радия голубым цветом. Этот класс светящихся составов обыкновенно применяется для экранов в рентгенотехнике, а также для научных приборов.
Приготовление С. с.В виду того что свечение зависит от наличия следов только определенных элементов, то даже ничтожные загрязнения другими веществами влияют на качество составов, и поэтому весь процесс приготовления должен проходить в условиях возможно большей чистоты, гарантирующей от попадания посторонних элементов как в применяемые реактивы, которые должен быть фотохимически чистыми, так и в приготовленную смесь до окончания процесса прокалки. Особенное внимание должен быть обращено на чистоту посуды, тиглей и всей лаборатории в целом. Не рекомендуется пользоваться посудой, бывшей в соприкосновении с различными солями металла, хотя бы даже после мытья. Для всех реактивов и для отдельных процессов должна иметься отдельная маркированная посуда. Вода должна применяться дистиллиро-
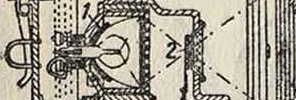
ванная в стеклянной или кварцевой аппаратуре. Тигли применяются фарфоровые, шамотные, платинированные и кварцевые, в зависимости от t° прокалки и химич. состава прокаливаемой смеси. Лучше всего состав помещать в двойных тиглях по типу, изображенному на фигуре 1. Что же касается печей, то таковые необходимо иметь отдельные для каждой группы составов, имеющей определенные металлич. примеси. Конструкция печи должна быть такова, чтобы она гарантировала равномерный нагрев, а также допускала плавный подъем температуры. Обыкновенно применяются газовые, масляные или электрические муфельные печи. Следует избегать железных и медных частей в печах. Все производство С. с. слагается из следующих процессов: получения исходных материалов, приготовления основной смеси, прокалки и измельчения.
С. с. из сульфидов щелочноземельных металлов готовятся сл. обр.: для основания берется один или несколько сульфидов; при этом можно взять заранее приготовленные сульфиды и их прокаливать е добавками или, для упрощения производства, смесь составляют так, чтобы образование сульфидов происходило одновременно с прокй всей массы. Т. к. фосфоресценция связана с кристаллит. структурой, то 1° печи должен быть настолько высока, чтобы молекулы основания стали достаточно подвижными с одновременным образованием центра. Темп-pa для различных оснований и в зависимости от плавней 800 4- 4 100°. Во избежание возгонки отдельных компонентов повышение ί° должно происходить равномерно; продолжительность прокалки 8/4-Μ1/2 час., причем в течение получаса (° поднимается до г° обжига. Количество серы м. б. взято по подсчету для полного образования сульфида с запасом на улетучивание, но в большинстве практически подобранных рецептов серы берется значительно меньше вследствие того, что получаемое основание твердого раствора состоит из смеси сульфида с окисью, к-рап также обладает фосфоресцирующими свойствами. Сера берется дважды перекристаллизованная в сероуглероде, или бензоле и растертая в тончайший порошок. Восстановитель в виде органич. вещества вводится в количестве, необходимом для восстановления основания и предохранения от окисления сульфида в сернокислую соль. Для равномерного распределения фосфорогена и облегчения кристаллизации вводится плавень, обычно в виде углекислых, хлористых или сернокислых солей щелочных металлов. Т. к. металл плавня влияет также на интенсивность отдельпых спектральных полос фосфоресценции, то и это должен быть учтено при выборе плавня. Действие плавня заметно даже в небольших дозах, а оптимальное количество определяется в пределах 24-10%. Во многих практически полученных рецептах вводят несколько плавней, но вообще необходима и достаточна только одна соль. Наиболее часто в виде фосфорогена для щелочноземельных сульфидов применяются металлы: висмут, марганец, медь, свинец и уран. У висмута главная полоса фосфоресценции фиолетовая, у марганца—желтая, а у меди, свинца и урана—зеленые, но это еще не служит основанием для предсказания цвета фосфоресценции, т. к. он зависит также от остальных добавок. Оптимальные количества металлов на единицу веса сульфидов следующие: 0,00014-0,0015 висмута; 0,002-1-0,01 марганца; 0,0001 4-0,0008 меди; 0,00014-0,0002 урана; 0,00014-0,0008 свинца. Фосфороген вводится в виде ового или водного раствора (0,54-1%) азотнокислой или хлористой соли. Во многих случаях добавление второго вспомогательного фосфорогена-усилителя улучшает устойчивость и яркость фосфоресценции, и как таковые применяют редкие металлы: рубидий, торий, тантал, таллий и др. Усилитель вводится в одинаковом или несколько большем количестве с основным фосфорогеном. Наиболее интересные рецепты для приготовления светящихся составов с основанием из сульфидов щелочноземельных металлов приведены ниже в таблицах.
| Свечение фиолетового (t° прокалки 750—800°). | цвета | ||
| СаО, з .. | 100 | 100 | 100 |
| S, з.. | 30 | 31 | 80 |
| Крахмал, з.. | 10 | 10,5 | — |
| Сажа, г..
Na2S, з.. |
_ | _ | 2 |
| 2,5 | — | ||
| Na2S04, з.. | — | 5,3 | _ |
| K2S, з.. | 2,5 | _ | _ |
| K.2SO4, 8.. | — | 5,3 | _ |
| U2CO3, 8.. | — | 10,5 | 4 |
| (NH4)2S, cm*.. | — | — | 10 |
| 0,5%-ный раствор Bi (N03)3, см“ | 5 | 8 | 10 |
| 0,5%-ный раствор НЬКОз, см“. | — | 4 | _ |
| 0,5%-ный раствор АиС1з, см“. | — | — | 10 |
Свечение синего и
(ί° прокалки 800—900°).
СаО, а..
SrC03, г..
Ва(ОН)2, г ..
Sr(OH)2, г..
S, г
Крахмал, г..
Na2S04, г..
K2S04, 0..
Щ2С0з, г..
0,5%-ный раствор ВКХОз)з, с.«з 0,5%-ный раствор RbNOe, см“. 0,5%-ный раствор TjN03, см3.
Свечение зеленого (ί° прокалки 900-
СаО, г ..
SrC03, г..
Ca(N03)2, г.
MgO, г..
SrO, г..
Sr(OH)2, г..
S, г..
Крахмал, г..
1л2СОз, з
Na2SC>4, г..
K2S04, 3..
0,5%-ный раствор Bi(NOs)3, сиз 0,5%-ный раствор Ta(N03)5, см“
0,5%-ный раствор RbNC>3, сл».
Свечение желтого (ί° прокалки 900
SrCOs, з..
ВаСОз, з..
S, з..
Крахмал, з..
Ы3РО4, з..
Na2CC>3, 0..
NaF, з..
NaCl, з ..
Na2S04, з..
MnS04, г..
0,5%-ный раствор CuCl2, с.иЗ.
0,5%-ный раствор Pb(N08)2> c«3
Свечение оранжево (ί° прокалки 1000
ВаСОз, з..
S, з..
Крахмал, з..
K2S04, з..
LI3PO4, з..
Na2S04, з..
Na2B407, з..
0,5%-ный раствор Си(N03)2, см“
0,5%-ный раствор ЕЫМОз, см“.
0,5%-ный раствор Pb(N03)2, с.иЗ
| лубого цвета | ||
| -900°). | ||
| 50 | 70 | 50 |
| — | — | 50 |
| 50 | _ | _ |
| — | 30 | — |
| 15 | 22 | 15 |
| 5 | 8 | 5 |
| 2,5 | 3,5 | 2,5- |
| 2,5 | 3,5 | 2,» |
| 5 | 7 | 5 |
| 5 | 7,5 | 5 |
| 10 | 5 | |
| - 7,5
го цвета |
- | |
| L 000°). | ||
| 25 | _ | 50 |
| ,_ | _ | 50 |
| 25 | — | — |
| — | 30 | — |
| 50 | _ | — |
| — | 70 | — |
| 35 | 20 | 15 |
| 5 | 6 | 5 |
| 5 | 6 | 2,5 |
| 2,5 | 3 | 2,5 |
| 2,5 | 3 | 2,5 |
| 2 | 6 | 5 |
| 2 | — | — |
| - 3 о цвета | 10 | |
| 100°). | ||
| 100 | — | ЮС |
| — | 100 | — |
| 40 | 25 | 40 |
| 5 | 5 | 5 |
| — | 2 | — |
| 2 | — | — |
| — | _ | 1 |
| 0,5 | — | — |
| — | _ | 2,5 |
| 0,2 | 8 | — |
| — | — | |
| i - к р а | с н о е | 10 |
| •1100°). | ||
| 100 | 100 | 100 |
| 25 | 25 | 25 |
| 5 | 5 | 5 |
| — | 2 | 2 |
| 2 | — | 2 |
| — | 2 | — |
| 2,5 | _ | 2 |
| 7,5 | 7 | 5 |
| 7,5 | 7 | _ |
| — | — | 5 |
Техника приготовления С. с. по вышеуказанным рецептам м. б. в основном сведена к следующим двум способам; а) тщательно очищенные от следов каких-либо примесей все основные сухие компоненты измельчают в порошок, перемешивают в фарфоровой чашке, увлажняют ом или сернистым аммонием, затем вливают раствор фосфорогена, тщательно размешивают, высушивают при умеренной ί° в закрытом шкафу с фарфоровой облицовкой, после чего размалывают в шаровой фарфоровой мельнице; б) отдельно смешивают плавни с серой, добавляют раствор фосфорогена, высушивают в шкафу и измельчают в мельнице или в ступке. К основным веществам добавляют полученную смесь и восстановитель, увлажняют дистиллированной водой и при легком подогревании тщательно перемешивают. Вновь сушат и измельчают в порошок в шаровой мельнице. Приготовленную смесь плотно насыпают в тигль, сверху добавляют немного серы, закрывают крышкой и прокаливают з/4—11 /2 ч.; после прокалки тигль быстро охлаждают на воздухе с закрытой крышкой. Охлажденную массу вынимают из тигля, очищают в темной комнате при ультрафиолетовом освещении (через черный никелевый светофильтр) от шлаков, затем раздробляют и измельчают в порошок. Т. к. у нек-рых С. с. сила свечения при сильном измельчении (вследствие разрушения кристаллич. решетки) падает, то крупность помола для каждого состава определяется опытным путем.
Приготовление С. е. из сульфида цин-к а. На яркость свечения С. с. из сульфида цинка сильно влияет чистота исходных материалов, особенно самого сульфида, приготовление которого должно вестись исключительно тщательно. Исходным материалом служит металлич. химически чистый цинк, к-рый растворяют в соляной или серной к-те. Во время происходящей реакции большая часть тяжелых металлов остается в виде черного осадка. Затем осаждают сероводородом остатки тяжелых металлов, фильтруют, кипятят для удаления сероводорода, окисляют бромом или перекисью водорода и добавляют в избытке аммиак для осаждения железа. После фильтрования добавляют кислоты для получения двойной цинково-
аммониевой соли, из которой осаждают сульфид. Полученный сульфид тонко растирают вместе с серой и плавнем <хлористый калий или натрий); фосфорогеном служит медь или марганец; первая вводится на 1 г сульфида в количестве 0,000025-М),0001 г, второй 0,0005-50,002 г; дру-тие металлы дают более слабое свечение. С медью получается зеленое свечение, а с марганцем оранжево-желтое. Все цинковые составы очень чувствительны к а-лучам. Кроме того при марганце С. с. дает очень яркую оранжевую триболюминесненцшо (смотрите Люминесценция). Высушенную массу помещают в неглазурованный фарфоровый двойной тигль (лучше—внутренний кварцевый), т. к. в этом случае не получается неактивной корки. Т. к. сернистый цинк диморфен и его двумя кристаллнч. формами являются цинковая обманка (сфалерит), кристаллизующаяся в кубич. системе, и вурцит, кристаллизующийся в гексагональной системе, то при прокаливании при низкой ί° (до 1 000°) получается цинковая обманка, а при 1° выше 1 020°—вурцит, при переходной (°—смесь обеих форм. Фосфоресценция вурцита лучше. Примесь сернистого кадмия, к-рый кристаллизуется только в гексагональной системе (гренокит), заставляет принять ту же форму и сульфид цинка, но в этом случае цвет свечения—от желтого до оранжевого. Кадмий оказывает влияние при наличии его 2-525%. Прокаливание готовой смеси ведут в муфельной печи, поднимая постепенно (° 11/2-52 ч. до 1 000-5 1 100°. После быстрого охлаждения на воздухе состав очищается при ультрафиолетовом свете от неактивных частей. Массу кладут в горячую воду, почему она распадается в мелкий порошок. Практически интересные рецепты:
| Зеленое | Желто- | ||||
| свечение | оранжевое | ||||
| ZnS, г. | 100 | 100 | 100 100 | ||
| NaCl, г. | 7 | 3 | 5 3 | ||
| KCI, г. | 7 | — | - 3 | ||
| MgF2, г. | — | 3 | — — | ||
| NHtCl, г | 2,8 | — | — — | ||
| S, г. | 14 | 5 | 5 5 | ||
| 0,1%-ный | раствор СиС12, см3 | 15 | 5 | 15 — | |
| 1,0%-ный | раствор Undo, см3 | — | — | - 30 | |
| Желто-
зел. |
Желт. | Оранж | Ораяж.-* красн. | ||
| ZnS, г. | 100 | 100 | 100 | ||
| CdS, г. | 10 | 20 | 25 | ||
| NaC], г. | 5 | 5 | 5 | 5 | |
| 0,1%-ный | раствор | ||||
| СиС12, см“. 15 | 15 | 15 | 15 | ||
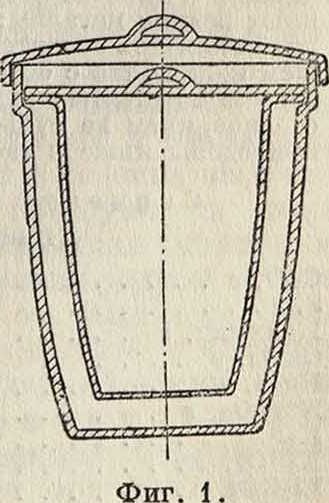
С. с. постоянного действия получаются из сульфида цинка путем добавления радиоактивного вещества, для чего состав промывается горячей водой; в отмытый еще влажный состав добавляют нужное количество раствора радиоактивного препарата и высушивают на водяной бане. Из всех радиоактивных веществ практич. применение для активации составов имеют радий, мезоторий и радиоторий, как дающие достаточное количество α-лучей, вызывающих свечение. При активации радием свечение начинается немедленно после приготовления состава и достигает практич, максимума
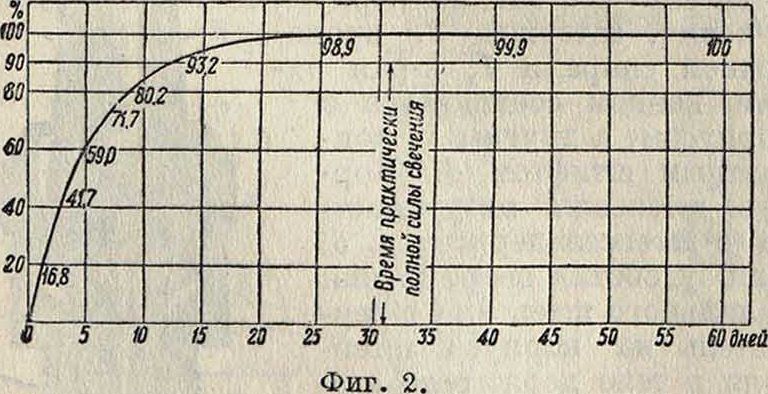
через 30 дн. в соответствии с увеличением а-ак-тивности от образующейся эманации (а-излу-чение самого радия составляет ок. 20% от общего α-излучения); на фигуре 2 изображено нарастание силы свечения от α-активности эманации. Так как жизнь состава определяется не только жизнью радиоактивного вещества, половинное время которой у радия 1 750 лет, а также и сопротивлением С. с. разрушающему действию лучей, к-рое в зависимости от количества введенного радия измеряется несколькими года ми, то энергия радия не используется полностью. Поэтому более целесообразно и выгодно заменять радий более дешевым мезоторием, к-рый сам излучает только β- и у-лучи, но продукт его распада — радиоторий — дает α-лучи. Светящаяся краска, активированная чистым мезоторием, сначала почти не светится, если в нем нет примеси радия, но по мере образования радиотория, к-рое достигает максимума через 4г/2 г., свечение соответственно увеличивается, что изображено на фигуре 3. Радиоторий м. б. отделен от
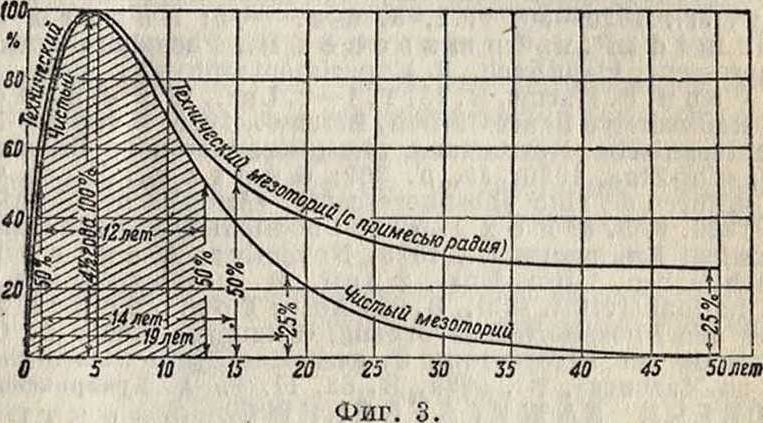
мезотория и использован для активации, но его я-активность все время падает, а соответственно и свечение состава, уменьшаясь через 2 г. до 50%, поэтому он мало пригоден для С. с., предназначенных для ответственных приборов, и применяется для замены постоянного радиоактивного состава в виду своей дешевизны. Падение силы свечения радиоториевого состава показано на фигуре 4. Для активации на 1 я сульфида цинка вводится 0,05-^0,20 мг радия, в зависимости ог требующейся силы свечения. При введении больших количеств состав быстро разрушается.
Мезоторий вводят в том же количестве (на 1 мг эквивалент радия). С. с. постоянного действия наносят на приборы в смеси с прозрачными лаками, не содержащими свободных кислот.
С. с. из ц и н к с и л и к а т а—яркие фосфбры, легко возбуждающиеся от коротких лучей. Приготовляют их двумя методами—с плавлением и оплавлением. По первому способу смесь из фтористого цинка, полученного из сульфата путем воздействия фтористого аммония с введением как фосфорогена марганца (из расчета 0,0001—0,1 на 1 ч. силиката), смешивают с порошкообразным горным хрусталем в неглазуро-ванном тигле и прокаливают в течение часа при 950°. По второму способу прессуют из смеси окиси цинка и горного хрусталя столбики, которые оплавляют на газово-кислородном пламени. Цвет свечения зависит от быстроты охлаждения и м. б. оранжевый, желтый и зеленый, первый—при быстром, последний—при очень медленном охлаждении. БорнокислыеС.с. состоят из б. или м. обезвоженной борной кислоты в виде основания и примеси органич. веществ как фосфорогена. Для приготовления очищают борную к-ту кипячением с азотной к-той от органич. примесей и после перекристаллизации
| И | |||
| и | |||
| Ik | |||
| ЩЫ
ИТ? |
ϊ
Γ |
s | й |
Фигура 4.
смешивают в ступке с нужным количеством фосфорогена, а затем осторожно прокаливают в платиновой чашке, пока периодически охлаждаемый состав не покажет яркого свечения. В качестве фосфорогена применяются: фенан-трен (1 : 100) — дает зеленое свечение, ангидрид фталевой кислоты (1 : 500)—голубовато-фиолетовое свечение, натрийфлуоресцеин (1 : 3 000)— голубовато-зеленое свечение и др.
Лит.: Богоявленский Л., Светящиеся составы постоянного действия, П.,1919;ИвановВ., Светящиеся краски, П., 1917; Жиров Н., Об изготовлении фосфоресцирующих веществ, «Журнал прикладной химии», Л., 1929—30, т. 2, 3, вып. 1—5; Lenard Р., SchmidtP.u. TomaschekE., Phosphoreszenz u. Fluoreszenz, Handbuch d. Experimentalphysik, hrsg. v. W. Wien u. F. Harms, B. 23, T. 1—2, Lpz., 1928; В e r n d t G., Radioaktive Leuchtfarben, Brschw., 1920; Rhode B., Die technische Herstellung phosphoreszierender Substan-zen, «Ch.-Ztg», 1930, 39, p. 369; G u n t z A., Etude sur les sulfures de zinc phosphorescents, «Annales de Cbimie», P., 1926, t. 5, 6; F о x J., «The Chemical Trade Journal a. Chemical Engineer», L., 1928, November; W an in о L„ Leuchtfarben, Ullm. Enz., 2 Aufl., B. 7;Marckwald W.,Radioaktivitat, ibid., B. 9,1 Aufl.; Tomaschek R., Ob>r den Phosphoreszensvorgang, «Sitzungsberichte d. Ge-sellschaft zur Befdrderung d. gesamten Naturwissenschaf-ten zu Marburg», B., 1929, B. 63, H. 4. А. Кучеривевнй.