 > Техника, страница 80 > Силикагель
> Техника, страница 80 > Силикагель
Силикагель
Силикагель, гидрат кремневой к-ты, находящейся в коллоидном состоянии, за последнее время получивший широкое технич. применение в качестве ценного адсорбента.
Брюстер f1] первый из исследователей занимался изучением гелей кремнекислоты. Кюн [2] и Струкман [3] изучали растворимость свеже-осажденных гелей кремнекислоты в различных жидкостях и нашли, что они имеют отрицательный заряд. Трем [*], изучая растворимость кремнекислоты, первый заметил способность наполняющих гель жидкостей замещаться другими жидкостями. Машке [6] нашел, что при взаимодействии щелочных солей кремнекислоты с к-тами свойства образующихся золей зависят от концентрации и t° обоих компонентов; он же установил, что кремнекислота м. б. получена в различных степенях гидратации, в зависимости от условий сушки. Следует указать также на работу Христиансена [*], исследовавшего оптические свойства гл. обр. природной кремнекислоты (смотрите Табашир). Особенно большое значение в деле изучения свойств коллоидной кремнекислоты и процессов, протекающих в системе гель + вода, имели исследования Ван-Бем-мелена [’], к-рый нашел, что гели при поглощении жидкостей или паров не образуют с ними химич. соединения, но что здесь происходит процесс адсорбции. Для объяснения процесса обезвоживания и оводнения гелей Жигмонди, приложив учение о капиллярных силах, доказал амикроскопичность гелей и, пользуясь уравнением Минковского [8], показал возможность вычислять диаметры капиллярных отверстий в гелях по понижению упругости пара. Работы Бахмана [9] (1912 год) подтвердили амикроспо-пичность структуры геля кремневой кислоты. Жигмонди, Бахман и Стевенсон [10] повторили исследование Ван-Беммелена по определению изотерм систем: гель Si02 + пары воды и гель Si02 + пары а и сконструировали особый аппарат, дающий возможность быстро определять изменения упругости паров в отсутствии воздуха. В 1913 г. Бахман [“] показал, что при поглощении жидкостей гелями кремнекислоты имеет место чисто капиллярный процесс без какого-либо взаимодействия с субстанцией геля. В 1914 г. Андерсон по понижению упругости паров воды, а и бензола, адсорбированных гелем Si02, вычислил наибольшие и наименьшие диаметры капилляров: вода—5,49-1-
2,75 тр, —5,17-1-2,42 тр, бензол—5,98-1-2,70 тр. Патрик в 1914 году исследовал поглощение коллоидной кремнекислотой углекислого газа, сернистого газа и аммиака при различных t° и давлениях.
В 1920 г. впервые был описан [12] в общих чертах способ получения С., обладающего удовлетворительными адсорбционными свойствами по отношению к парам. Способ этот (по Патрику) следующий: при взаимодействии растворов соляной кислоты и силиката натрия образуется золь, коагулирующий в течение 1—18 часов. Когда гель достаточно отвердеет, его промывают чистой водой до полного удаления электролитов, сушат в вакууме при 110° и доводят в нем содержание воды до 7—8%. Патрик пришел к следующим выводам: 1) максимумом адсорбционных свойств обладает С., содержащий ок. 7% воды, 2) эмпирия, ур-ие Фрейндлиха (смотрите Адсорбция) не всегда приложимо к полученным экспериментальным данным, 3) наиболее удовлетворяющим действительности ур-ием можно считать следующее:
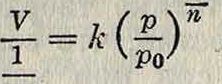
ап
где V — объём конденсированной фазы, а — поверхностное натяжение, р — давление газовой фазы, р0 — упругость паров жидкости, к п ~ —
постоянные, зависящие от физич. свойств адсорбента и адсорбтива. Несмотря на значительное количество работ по С. вопрос о способах его получения ограничивался лишь общими указаниями [13]. В 1925 г. Холмс и Андерсон [“] опубликовали новый способ получения С. с высокой сорбционной емкостью. По этому способу С. готовится взаимодействием растворов жидкого стекла с растворами различных солей (FeCl3, NiCl2, А1С13, СаС12 и др.). Пример: к 500 см3 жидкого стекла уд. в 1, 375,. разведенного водой до 10 л, приливают при сильном помешивании 1 440 см3 2/jiV раствора FeCl3; осадку дают отстояться и затем отфильтровывают через полотно. Отфильтрованную массу раскладывают тонким слоем на лотки с полотняным дном и сушат в теплой вентилируемой комнате. После нескольких дней просушивания куски геля становятся твердыми и ломкими; тогда гель вносят в сосуд и промывают водой до отрицательной реакции на хлор. Полученный красный гель после высушивания при комнатной t° активируют нагреванием в сушильном шкафу при 135—145° в течение 12 час. Перед употреблением такой гель активируют еще раз при 150°, пропуская через него слабый ток воздуха. Сорбционные свойства такого геля (при упругости паров бензола при 30°) равны 43,2%. Для придания гелю большей пористости авторы отмывали заключающийся в нем коллоидный гидрат окиси железа, настаивая гель в 6N растворе соля-
ной к-ты, с последующим промыванием водой. Такой гель показал сорбционную емкость по бензолу при 30°, равную 50%. Кроме феррок-сид-геля авторами были получены гели, содержащие окислы алюминия, хрома, кальция и меди. Они получались взаимодействием 500 см3 0,44N раствора хлористой соли металла с 1 л раствора, полученного разбавлением 50 см3 продажного жидкого стекла. Для приготовления гелей, содержащих закись никеля, на 1 л стекла брали по 110 см3 2/,iV раствора NiCl2. В табл. 1 приведена сорбционная емкость полученных гелей по бензолу при 30° (в %).
Таблица 1. — Сорбционная емкость гелей.
| Тип геля | i Сорбц. емкость промытого геля I (после высушивания) | Сорбц. емкость геля, обработанного к-той |
| <А1203)х (Si02)y | 4,1 | 24,5 |
| (СаО)х (Si02)y | 8,6 | 21,2 |
| (Сг203)х (Si02)y | 23,2 | 37,8 |
| <CuO)x (Si02)y | 26,1 | 37,9 |
| (NiO)x (Si02)y | 60,0 | 96,8 |
Оказалось, что ферроксид-гель (гель «from iron») и гель «from nickel» гораздо лучше обесцвечивают масла, чем обыкновенный С. Холмс, Сел-ливан и Меткаф (Metcalv) [1δ] нашли, что при промывании геля 3/χΝ раствором горячей соляной кислоты получается С. одинаковых сорбционных свойств с гелем, промытым серной к-той при 115°. Далее было установлено, что оптимальным содержанием воды в С. до его промывки нужно считать 50—70% и что очень сильное влияние на повышение сорбционных свойств С. оказывает процесс синерезиса (смотрите). Для изготовления нового типа С. авторы дают следующий рецепт: к 50 л разбавленного раствора силиката натрия (2,5 л продажного жидкого стекла уд. в 1,375, разведенного до 52,5 л) медленно приливают при сильном помешивании 8 a 2hN раствора FeCl3. Жидкости дают стоять ок. 60 час., затем фильтруют через полотно, положенное на железную сетку, располагая осадок толщиной ок. 5 см. Когда содержание воды упадет до 60%, куски геля размером ок. 2 сантиметров помещают на неделю для выпотевания в закрытые банки (процесс подсушивания длится до двух и более недель). Гель после выпотевания ломают на куски размером ок. 1 сантиметров и кипятят несколько раз по 1 ч. с 6/i4-e/1iV раствором серной кислоты до удаления Fe(OH)3, промывая гель водой после каждого кипячения. Затем отмытый гель сушат при 150° в течение 8 ч., после чего активируют при 140—200°, пропуская через толщину геля струю сухого воздуха. В" табл·. 2 приводится сравнительная сорбционная емкость трех типов С. (по данным Холмса).
Таблица 2. — Сравнительная сорбционная емкость различных гелей.
| Адсорбтив | Гель Патрика | Гель, подвергнутый горячей активации | Феррок сид-гель |
| Бензол. | 32,2 | 62 | 126 |
| 32,1 | 63 | 119 | |
| Ксилол.
Четыреххлористый |
33,4 | 62 | 120 |
| углерод. | 57,7 | 120 | 222 |
| Сероуглерод. | 44 | 91,5 | 182 |
| Хлороформ. | 55,7 | 107 | 202 |
| Бромистый этил. | 57,1
30,5 |
107 | 208 |
| Этиловый эфир. | 54,3 | 108 | |
| Газолин. | 27,6 | — | 68 |
| Амилен. | 25,9 | 53,4 | 96,7 |
Описанный метод приготовления дает возможность регулировать величину капиллярных отверстий; например при высушивании С. до содержания в нем около 35% воды происходит сильное уменьшение объёма геля и образование мелких капилляров, а при доведении содержания воды до 55% образуются более широкие капилляры.
Феллс и Фирс [16] предложили способ получения высокопористого С. — «Carbo-gel». Способ приготовления этого типа гелей следующий: раствор силиката натрия (уд. в 1,181) смешивают с раствором тростникового сахара в 1/1N растворе соляной к-ты. Отвердевший гель ломают на небольшие куски и нагревают на паровой бане в открытой фарфоровой чашке; при этом гель буреет, затем чернеет. После этого гель нагревают в воздушном термостате до 300° в течение 2 ч. Полученный продукт тщательно промывают водой, на что требуется ок. 4 ч., и активируют в течение 2 ч. при разрежении 15—20 миллиметров рт. ст. Адсорбционная емкость полученных образцов геля приведена в таблице 3.
Таблица 3.—А дсорбц ионная емкость образцов геля (по Фелпсу и Фирсу).
| Состав геля в | % | Адсорбировано в % | ||
| S102 | н2о | С | Бензол | |
| 93,20 | 6,80 | 65,4 | 62,2 | |
| 91,65 | 6,41 | 1,94 | 68,1 | 65,4 |
| 88,37 | 7,02 | 4,61 | 73,2 | 69,5 |
| 86,96 | 7,11 | 5,93 | 75,6 | 70,8 |
| 86,12 | 6,90 | 7,28 | 77,8 | 72,8 |
| 83,76 | 6,64 | 9,60 | 80,2 | 75,0 |
| 79,66 | 6,92 | 13,52 | 85,0 | 80,1 |
| 75,59 | 6,31 | 18,10 | 88,2 | 82,7 |
| 66,59 | 6,00 | 7,41 | 84,3 | 78,9 |
| 53,96 | 5,84 | 40,20 | 74,8 | 67,7 |
| — | — | 100,00 | 25,1 | 22,3 |
Окатов [”] разработал способ получения С., основанный на медленной коагуляции золя, с последующей обработкой геля активирующими растворами. В качестве активирующих веществ он применял аммиак и сернокислые соли аммония или щелочных металлов. При этом было замечено, что гель с оптимальной динамической активностью получается при изготовлении его след, образом: к 10/j.iV раствору соляной кислоты приливают раствор жидкого стекла, взятого в таком отношении к к-те, чтобы 6-^-8% кислоты в реагирующей жидкости оставалось свободной после смешения. Кроме этого концентрация раствора жидкого стекла должна быть такой, чтобы получающийся золь содержал 10-М1% Si02. Это достигается предварительным определением содержания Si02 в жидком стекле. Полученный так. обр. золь оставляют стоять в ваннах на несколько дней до наступления достаточной зрелости геля, что определяется появлением на поверхности геля жидкости (синерезис), растрескиванием и отставанием от стенок сосуда. Для определения количества аммиака, необходимого для приготовления активирующей жидкости, поступают след, обр.: после изготовления золя берут пипеткой 50 см3 золя, переносят в мерную колбу и оттитровывают аммиаком. Отсюда, зная объём изготовленного золя, вычисляют объём аммиака, необходимый для нейтрализации всей свободной кислоты в золе. После того как гель достиг достаточной зрелости, его ломают на куски размером 2—3 см, кладут в сосуд вместе с сывороткой и обливают активирующим раствором, состоящим из 0,25iV раствора Na2S04 и содержащим аммиак в количестве, необходимом для нейтрализации 0,4—0,5 всей свободной соляной кислоты в геле. После суточной активации геля раствор сливают, а гель промывают водой до отсутствия кислой реакции в толще геля. После этого гель вносят в термостат и сушат при 150° до превращения геля в твердую массу. Такой гель обладает удовлетворительной скоростью поглощения при невысоких концентрациях. Активация геля при обработке раствором сернокислых солей основана на коагуляции и дегидратации ионом S04" коллоидных комплексов кремнекислом в непрокоагулировав-шем золе, находящемся в толще геля, причем действия этих ионов проявляются только в слабокислой среде (Окатов). По мере повышения содержания аммиака в активирующей жидкости при высушивании происходит все меньшее сжатие объёма геля, то есть образование более грубой капиллярной структуры. Такие гели хорошо поглощают пары лишь при высоких концентрациях и совершенно непригодны для низких концентраций.
Кроме вышеуказанных способов С. может быть получен, и притом в наиболее чистом виде, путем взаимодействия четыреххлористого кремния SiCl4 с водой. Этот способ получения м. б. весьма рентабельным, так как при получении хлористого алюминия из глины в качестве побочного продукта образуется четыреххлористый кремний, не имеющий технического применения и являющийся поэтому отбросом производства.
Тиссен и Кернер [18] получили С. путем омыления этилового эфира ортокремневой к-ты. Ими получены Оыли следующие гидраты: Si022H20; 28ί02·3Η20 (пиро-); Si02· • НгО (мета-); 2Si02H20 (метадикремневая к-та). Кроме того были вычислены теплоты образования этих гидратов путем применения уравнения Клапейрона-Клаузиуса из упругости паров гидрата при разных /°. Вычисленные теплоты образования весьма незначительны по сравнению степлотами гидратации других веществ. Ниже приведены граммолекулярпые теплоты образования при 320,5° (абсолютные): Si02*2H20—I 200 cal, 2Si02*3H20—i 500 cal, Si(VH20—1 000 cal, 2Si02· H20 — 1 000 cal. Сапожников, Окатов и Сусаров [19] показали, что С. обладает вполне удовлетворительными адсорбционными свойствами по отношению к ок азота, причем по мере понижения концентрации адсорбтива и повышения ί° адсорбционная способность геля, падает; поглощение ΝΟ2 выгоднее вести при 1°, близкой к нулю; при обратном получении из геля поглощенной ΝΟ2 выходы достигают 954-99%.
Изучение изотерм адсорбции [20] для 02, СО и С02, а также для бинарных систем: СО + + 02 при 0°, СО + 02 при 100°, С02 + 02 при 100° и С02 -г СО при 100° показало незначительную сорбционную емкость С. по отношению к этим газам, например для кислорода при 100° и 142 миллиметров давления она равна 0,54 см3, а для СО при 100° и 127 миллиметров — 1,37 см3. Кроме С. в зернах и порошке, применяемого гл. обр. для очистки нефтепродуктов, в практике появились формованные гели в виде пластинок и цилиндриков. Формованные гели имеют преимущество перед зернеными в том, что при их изготовлении не наблюдается отходов и требуется меньшая затрата тепла на высушивание (т. к. при формовании большая часть воды отжимается). Прессование по данным патентной литературы [21] ведется при давлениях порядка 300—500 aim. В нек-рых случаях однако С. в цилиндриках м. б. получен путем пропускания через обыкновенную рубку.
Применение С. Возможность широкого технич. использования С. впервые была установлена в 1918 году в лаборатории фирмы Davison Chemical Со. в Балтиморе (США), что явилось толчком для образования фирмы Silica-gel Corporation, сконструировавшей адсорбционно-поглотительные установки для улавли вания паров органич. растворителей и паров воды из воздуха. Фирма указывает на следующие применения С.: сушка воздуха при подаче его в доменные печи, улавливание паров бензина из природных газов, паров бензола на коксобензольных з-дах, улавливание паров летучих растворителей, улавливание нитрозных газов, концентрирование и получение сухого сернистого газа. Кроме этого возможно применение С. как носителя контактной массы в сернокислотном производстве и вообще как субстрата (подкладки, пористой основы) для самых разнообразных катализаторов.
Холмс, Рамзай и Эльдер [22] указывают, что платинированный С., при одном и том же содержании платины, обладает более высокими ка-талитич. свойствами, чем платинированный асбест. Получение платинированного С. вели путем смачивания носителя слабощелочным раствором H2PtCle · 6Н20. Гель после смачивания просушивали при 100° и охлаждали до комнатной г’, после этого осторожно пропитывали раствором формалина и медленно нагревали до 100“. После почернения гель тщательно промывали горячей водой и сушили. Авторы работы указывают, что максимальный процент окисления S02 равен 96%. Ададуров и Бродович исследовали контактирующие свойства С. по отношению к S02 и нашли, что гели, полученные путем взаимодействия растворов жидкого стекла с раствором NiCl2 или Fed, обладают высокими контактными свойствами (до 67%). В технич. масштабах платинированный С. обычно готовят путем обрызгивания формованного геля (в цилиндриках) раствором H2PtCle, с последующим восстановлением при нагревании. О применении С. для рекуперации паров растворителей см. Рекуперация паров летучих растворителей.
Сравнительно широкое применение С. получил в технике осветления минеральных масел, керосина и сырого бензола благодаря его способности полимеризовать непредельные соединения и адсорбировать растворенные примеси. По данным фирмы Silicagel Corporation С. почти нацело освобождает керосин также и от сернистых соединений. Регенерация С. после отбелки по данным той же фирмы ведется путем продувки перегретым до 450° водяным паром, который вытесняет большую часть адсорбированных гелем веществ, с последующим продуванием смеси пара с воздухом при 350°. С. регенерируется нацело без изменения своих свойств. Процесс регенерации длится ок. 5 час. Для очистки масел [23] гель должен быть тонко измолот (при прохождении через сито с 200 отверстиями на дм. не должно получаться остатка); при применении более крупного порошка процесс очистки сильно замедляется. Работы по изучению очистки нефтяных погонов от сернистых соединений были произведены Ватерманом и Перкином [а4], Миллером и Дунстаном [25]. Белль [26] дает описание установок для очистки сильно загрязненного бензина с суточной производительностью до 1 000 бочек (для очистки водных растворов гель применяться не может вследствие своей гидрофильности). Внедрение С. в практику отбельных процессов тормозится лишь его относительной дороговизной по сравнению с натуральными отбеливающими материалами — флоридином, фуллеровой землей и тому подобное.
Лит.: i) «Ohimie et Physique», Paris. 1820, t. 29, p. 41 i—429, 1828, t. 52, p. 412—416; 2) «journal f. prakt. Chemie», Lpz., 1853, B. 59, p. 1—6;3) «Liebigs Annalen», Lnz., 1855, B. 94, p. 341; i) «Annalen (1. Physik u. Chemie»,
Lpz., 1864, p. 529; 6) ibid., 1872, B. 221, p. 549—578, B. 222, p. 90—111; 6) ibid., 1885, p. 259, 260, 298—305, 439—446; 7) «Zeitschrilt i. anorg. Chemic», Leipzig, 1908, B. 59, p. 225—249, 1909, B. 62, p. 1—23; 8) Enzytlopadie d. mathem. Wissenschaften.Mch.— B., 1907, B. 5, T. 1, H. 4, p. 71; «Ztschr. f. anorg. Chemie», Leipzig, 1912, B. 73, p. 125; 1«) ibid., 1912, B. 75, p. 189; Щ ibid., 1913, B. 79, p. 202; X2) «Ain. Soc.», 1920, v. 42, p. 946; is) «.lourn. of Physical Chemistry», N. Y„ 1918, v. 22, p. 510—519; Щ «Industrial a. Engineering Chemistry», N. Y., 1925, v. 17, 6; 15) ibid., 1926, April; 1«) «Chemistry a. Industry Reriew», L., 1927, v. 46; l?) «Журнал прикладной химии РФХО», 1929, 1; Щ «Ztschr. f. anorg. u. allgem. Chemie», Lpz., 1931, B. 197; 19) «Ж», t. 6, вып. 8; 20) «Am. Soe.», 1931, p. 497; 2i) к a u s c h, O., Das Kieselsfturegel u. die Bleieherden, B., 1927; 22) «Industrial a. Engineering Chemistry», N. Y., 1929, v. 21, 9; 23) «Brennstoff-Cbemie», Essen, 1923, В. 4, p. 358; 24) ibid., 1925, В. 6, p. 255 — 257; 25) «J. Ch. I.», 1924, y. 43, p. 181; 26) «Ch.-Ztg», 1924, p. 48, 518. А· Окатов.