 > Техника, страница 80 > Синтетический каучук
> Техника, страница 80 > Синтетический каучук
Синтетический каучук
Синтетический каучук. Первые наблюдения по превращению циэтиленсвых углеводо-р<дов в каучукоподобные вещества (в С. к.) были сделаны Г. Бушарда в 1879 г. при нагревании изопрена и И. Кондаковым в 1901 г. при автополимеризации диизопропенила К1]. Вопрос о синтезе каучука как о практич. задаче был впервые поставлен в 1909 году В этом году и в ближайшие годы производилось обследование явлений полимеризации и связанного с этим вопросом получения С. к. независимо и одновременно С. Лебедевым [2] в России, Гар-риесом [3] и Гофманом [4] в Германии, Перкином и Метьюсом в Англии. Впоследствии вопросами синтеза каучука в России занимались И. Остромысленский [6] и Б. Бызов. Наибольшее внимание этому вопросу было уделено в Германии, где во время войны построен завод С. к. из диизопропенила. Он выпустил свыше 2 000 тонн каучука. С окончанием войны этот з-д был закрыт.
В 1926 г. по инициативе ВСНХ была усилена работа по С. к. в СССР. Разработанный С. Лебедевым способ получения дивинилового каучука из а был изучен на опытном заводе в Ленинграде. Первый большой завод, работающий по этому способу, лущен в ход в июле 1932 г. в Ярославле; второй завод пущен в сентябре 1932 г. в Воронеже. Третий завод в Ефремове пущен в течение мая—июля 1933 г.; постройка четвертого завода в Казани близится к окончанию. Вопросы, связанные с получением С. к. из нефти, разрабатывались до 1934 г. на опытном заводе «А» в Ленинграде, а сейчас в Москве.
Химия С. к. сейчас достаточно определенно намечает пути своего дальнейшего развития. Если до недавнего времени она стремилась к тому, чтобы С. к. возможно точнее копировал, свойства природного каучука, то в настоящее время задача ставится значительно шире. Всякая новая форма С. к. приносит новый комплекс свойств, которых нет ни у природного каучука ни у других С. к. Способностью превращаться в высокомолекулярные полимеры, обладающие рядом признаков природного каучука (эластичность, способность вулканизоваться горячим и холодным способом), отличаются многие вещества, имеющие в молекуле сопряженную систему двойных связей:, с=с — с=с.
Эту группировку атомов можно назвать к а у-чукофором. Процесс получения С. к. поэтому распадается на следующие две основные операции: 1) синтез веществ, имеющих в молекуле каучукофор (обычно это углеводороды, но в последнее время внимание исследователей стали привлекать производные этих углеводородов, например вещества, содержащие галоид или этоксильную группу —О · С2Н6, и 2) превращение этих BfiineqTB в высокомолекулярные полимеры, или полимеризация. Строение полимерных форм С. к. в значительной степени разъяснено изучением действия на них озона (метод Гарриеса) и обследованием продуктов, получающихся при распаде озонидов. Различают два типа полимеров (каучуков): нормальные и анормальные. Первые получаются в результате самопроизвольной полимеризации при комнатной г° или при нагревании—обычно в пределах 50 н- 150°. Их строение аналогично строению природного каучука. Для изопрена например строение нормального полимера таково:
[—сн2—с=сн—снг—сн2—с=сн—сн2—
I I
СН? СНз
Анормальные каучуки имеют структуру, отличную от структуры природного каучука. Такие каучуки получаются при полимеризации, протекающей под влиянием энергичных возбудителей процесса. Наибольший интерес имеет вопрос о структуре каучуков, заполимеризован-ных действием металлич. натрия. На основании работ Циглера [6] натрийбутадиеновому каучуку приписывают структуру
| СН2^.СН2 | -СН2
1 | |
| СН | СН | сн- |
| СН | СН | сн |
| II | II | II |
| сн2 | сн2 | сн2 |
Вопрос этот однако не может считаться окончательно решенным.
Синтез исходных материалов. Бутадиен-1,3, иначе дивинил, винилэтилен, э р и т р е н [5, 7] СНа : СН · СН : СН2. При атмосферном давлении это газ, 1°кип. —4,3° (751 миллиметров). D~f=0,65615; D=0,64483; Df= =0,62743. Молекулярная рефракция MRo== 20,85. Для ф-лы С4Н6 требуется MRd=19,72. Отсюда экзальтация +1,13. Упругость пара р в пределах от—79° до +29,8° имеет следующие значения в миллиметров:
t° -79 —58 -29 —14 —7,2 0 +8,2 +15,0 +29,8 р 20 116 338 529 692 902 1 215 1 532 2 419
Кривая упругости пара дивинила в интервале
—14° (-29,8° выражается следующим ур-ием:
1183
]gP=7,2860--ψ-. Бутадиен как ненасыщен ный углеводород способен присоединять по две молекулы водорода, галоидоводородных кислот, хлора, брома. Как вещество, содержащее сопряженную систему двойных связей, он способен присоединять сернистый ангидрид, а также молекулу малеинового ангидрида. Наиболее характерная реакция для бутадиена—присоединение брома. При избытке этого реактива образуется кристаллический плавящийся около 110° тетрабромид С4НвВг4. Главная масса (90%) этого бромида состоит из высокоплавкой модификации с г°пл. И8°. В виде примеси имеется ок. 10% низкоплавкой модификации с 1°пл. 39°. Металлич. цинком в овой среде бутадиен регенерируется количественно из обоих тетрабромидов. Количественное определение бутадиена производится или в виде тетрабромида или в форме соединения с малеиновым ангидридом. Впервые бутадиен-1,3 был получен Кавенту в 1862 г. при разложении паров амилового а в железной трубке при красном калении. Этот способ не имеет практического значения. Известно свыше двух десятков способов получения бутадиена-1,3. Здесь приведены лишь те, которые по доступности сырья и выходам имеют практич. значение или могут его получить при усовершенствовании. 1) Из ацетилена. Недавно химиками амер. Общества Дю-Пон-де-Немур [10] разработан способ получения димерной формы ацетилена. Получается он при каталитическом действии Cud. Его формула: СН I С · СН : СН2. Превращение этого углеводорода в бутадиен возможно при частичном присоединении водорода
СН ! G · СН : СН2 + Н2 — СН2 : СН · СН : СН2. Однако проведение этого процесса с хорошими выходами может натолкнуться на значительные затруднения вследствие его осложнения образованием продуктов дальнейшего присоединения водорода к бутадиену. Оригинальный выход из положения был найден в замене во дорода хлористым водородом. При этом был получен охлоренный аналог бутадиена—хлоропрен, способный полимеризоваться в каучукоподобное вещество. 2) Смесь ацетилена и этилена, взятых в эквимолекулярных количествах, по наблюдениям Вертело (1867 г.) дает нек-рое количество бутадиена при пропускании через накаленную докрасна трубку. Процесс течет по уравнению: СН : СН+СН2 : СН2 — СН2 : СН - СН : СН2.
Этот способ пока не имеет практич. значения вследствие малых выходов бутадиена. 3) Можно считать установленным, что большинство органич. соединений при пирогенном разложении образует некоторое количество бутадие-на-1,3. Количество бутадиена колеблется в широких пределах, в зависимости от исходного материала и от условий процесса. Наиболее обещающим сырьем для пирогенного процесса образования бутадиена-1,3 является нефть; может быть некоторые специальные сорта нефти окажутся особо пригодными. Образовать бутадиен способна как сама нефть, так и все ее фракции. Оптимальные условия процесса: £° 700+ 750° и возможно быстрое удаление образовавшегося бутадиена из сферы высокой £° (закалка). По опытам С. Лебедева [8] и его сотрудников из бакинской нефти и ее фракций были получены такие выходы бутадиена: би-биэйбатская нефть 3,75%; различные фракции бензина 7,5+11%; керосин 6,0%; соляровое масло 5,5%; мазут 2,5%. При существующих способах пиролиза нефти (получение светильного газа и блаугаза, ароматизация нефти, крекинг) количество возникающего в процессе бутадиена повидимому колеблется от предела, близкого к 1%, домалых долей процента. Вопрос о выделении и эксплуатации бутадиена, образующегося при процессах пирогенизации нефти, в особенности при ожидаемом широком развитии крекинга, является вопросом значительной экономической важности. Значительные трудности встретятся при очистке нефтяного бутадиена-1,3 от многочисленных сопровождающих его других непредельных углеводородов. Последние затрудняют полимеризацию бутадиена и повидимому неблагоприятно отзываются на качестве получающегося каучука.
4) Из ацетальдегида можно получить бутадиен-
1,3 в три последовательные фазы: а) полимеризация альдегида в альдоль под влиянием щелочей: 2СН3 · СНО=СН3 · СН(ОН) · СН2 · СНО;
б) восстановлением альдоля в 1,3-бутиленгли-коль электролитически или каталитически: СНз“СН(ОН)-СН2-СНО+Н2=СНз“СН(ОЫ)·СН2-СН2(ОН);
в) дегидратация 1,3-бутиленгликоля в бута-диен-1,3 в присутствии водуотщепляющих катализаторов:
СНз-СН(ОН) · СН2 · СН2(ОН)=2Н20 + СН2 : СН · СН : СН2. Исходный альдегид м. б. получен или из ацетилена (способ М. Кучерова) или из этилового а. Этот способ может стать приемлемым при проведении всех трех фаз с весьма высокими выходами. 5) Из смеси альдегида со ом по способу, разработанному И. Остромы-сяенским [6]. Эквимолекулярная смесь альдегида и а, пропущенная через трубку с окисью алюминия, при 360+460° образует бута-диен-1,3 в значительных количествах. Реакция повидимому течет через 1,3-бутиленгликоль: СНз· СНО + СН3 ·СН2(ОН) =СН3·СН(ОН) ·СН2·СН2(ОН), к-рый далее дегидратируется окисью алюминия в бутадиен-1,3. Этот способ был проведен на специальной установке на заводе «Крас ный Богатырь» в Москве в 1919—22 гг. Было найдено, что выход бутадиена по этому способу равен 6%. 6) Из этилового а С. Лебедевым [9] был разработан очень простой способ получения бутадиена, непосредственно из а. Пары этилового а пропускают через трубу, заключающую катализатор, при 425—450°. Катализатор представляет тесную смесь вещества, способного отщеплять от а воду, например А1203, с веществом, способным отщеплять от а водород, например ZnO. Реакция течет по ур-иям:
2СНз-СН2(0Н)=2Н20 + Н2 + СН2 :СН-СН : СН2, ЗСНз-СН2(ОН)=ЗНгО + Иа+СвНю и т. д.
Первая из этих реакций преобладает, остальные имеют подчиненный характер. Побочными продуктами при этом процессе являются: этилен, псевдобутилен, уксусный альдегид, эфир, нормальный бутиловый и гексиловый ы и другие продукты. При хорошо подобранном катализаторе выходы бутадиена превосходят 20% на затраченный. По этому способу получают бутадиен первые заводы С. к. в СССР.
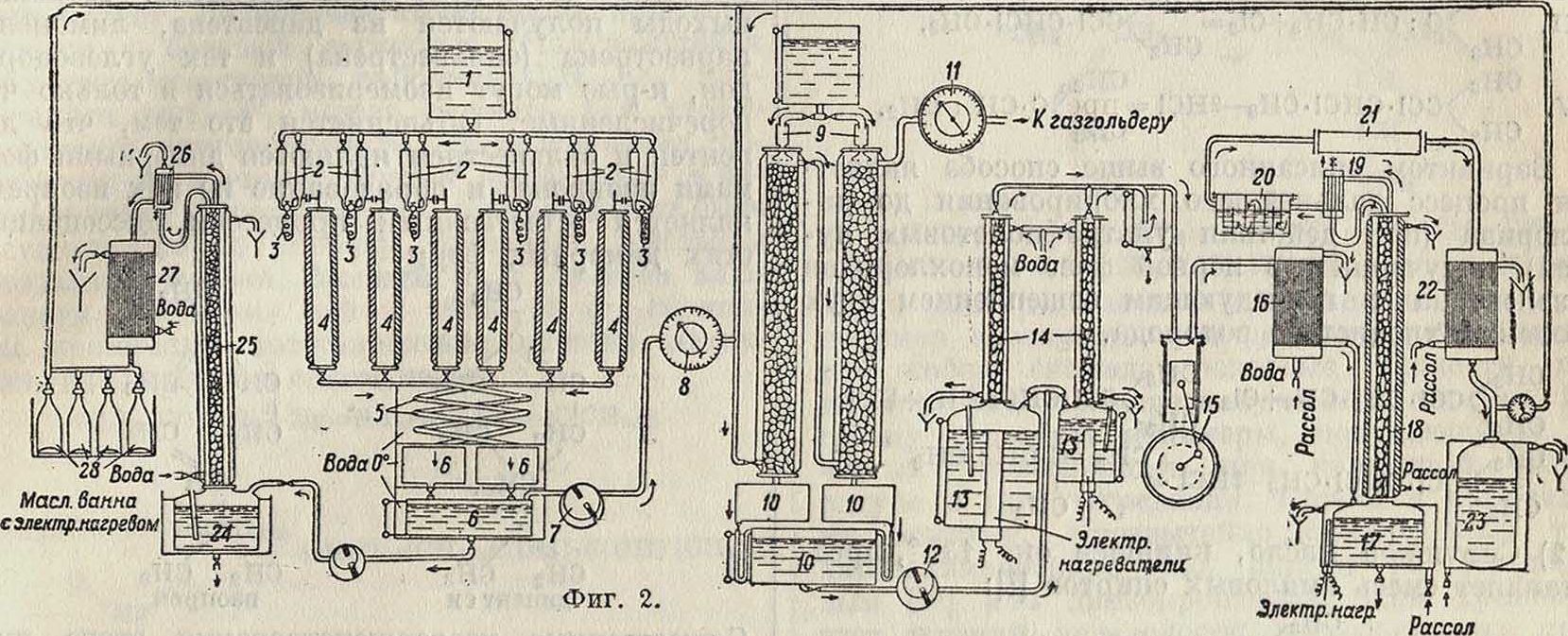
Фигура 1 и 2 представляют установки для переработки 80 килограмм а в сутки. Химически процесс является однофазным. Технологически он разбит на четыре части: 1) контактное разложение а; 2) разделение продуктов разложения на жидкий конденсат и газ; 3) переработка газа; 4) переработка жидкого конденсата. Аппаратом для контактного разложения является печь, состоящая из системы труб, наполненных рыхлой контактной массой. Трубы обогреваются отдельно или в общей оболочке. На фигуре 1 изображена отдельная печь с двусторонним эле-ктрич. нагревом (диам. 10 см, длина 1 м, материал красная медь). На -карман, 2—вакуум, 3—трубка для поступающих паров а, 4—верхний фланец (железо), 5—изоляция (асбест), 6—карман для внутреннего нагрева (красная медь), 7—карман для термопары печи (красная медь), 8—намотка (нихром), 9—трубка для отводящих газов из печи, 10—нижний фланец, 11—стенки печи. На фигуре 2 изображена батарея из 6 таких печей: 1—бак для а, 2—мерники для а,
3—перегреватели для а, 4—печи, 5—ледяной холодильник, 6—приемник конденсата,
7—эксгаустер, отводящий газ разложения в систему поглотителей. Процесс разложения ведется при t° ок. 450°. Пройдя через холодильник, продукты разложения разделяются на газ и жидкий конденсат. Газ состоит из бутадиена-1,3 и ряда побочных продуктов: водорода, этилена, псевдобутилена, ацетальдегида и незначительных количеств окиси углерода, метана и др. Газ содержит значительное количество паров летучих жидкостей, входящих в состав конденсата. Переработка газа протекает так. обр.: газ, вышедший из холодильника 5, поступает через газоме-ритель 8 на скрубберы 9, орошаемые жидкостью, способной растворять тяжелые составные части газа, включая бутадиен и псевдобутилен. Такой жидкостью может служить, керосин и др. Скрубберная жидкость стекает в бачки
10, а газ, состоящий главным образом из Н2, С2Н4, СО и СН4, через газомеритель 11 поступает в газгольдер. Скрубберная жидкость передается насосом 12 в перегонные кубы 13, а оттуда в колонны с насадкой 14. Здесь из скрубберной жидкости отгоняются растворенные в ней газы и летучие продукты разложения а. При помощи компрессора 15 и холодильника 16 газы конденсируются и передаются на ректификационный аппарат. Последний состоит из бака 17, колонны 18, дефлегматора 19, промывателя 20, сушила 21, холодильника 22 и приемника для ректификованного бутадиена 23. Ректификация ведется под давлением около 3 atm. В промы-вателе 20 бутадиен освобождается от примеси альдегида. Ректификованный бутадиен, содержащий в качестве примесей псевдобутилен, ди-этиловый эфир и нек-рые другие вещества, поступает на полимеризацию. Для переработки жидкого конденсата его перекачивают из бака 6 в куб 24 ректификационного аппарата, состоящего из колонны 25, дефлегматора 26, холодильника 27 и приемников 28. Конденсат состоит из неразложенного а, воды, диэти-лового эфира, бутилового и гексилового ов, уксусного альдегида и некоторых других карбонильных соединений, а также углеводородов этиленовых, двуэтиленовых и бензольных. Конденсат подвергают разделению на фракции. Из них путем ряда физических и химических операций выделяются в технически чистом состоянии перечисленные выше отходы.
Изопрен [7], иначе метил-2-бутадиен-1,3, или /J-метилдивинил,
СН2 : С · СН : СН2
I
СНз бесцветная, очень подвижная жидкость своеобразного резкого запаха. Его физические константы приведены в следукщей таблице:
| Характеристики | по Гарриесу [З] | по С. Лебедеву |
| ΙΟ
1 кип.. |
33,754-34° (762 миллиметров) | 34,5° (765 миллиметров) |
| Уд. вес. | 0|Ь5=0,6793 | £>|0,0 = 0,6803 |
| Показ, преломл. | П2Ь°=1,42267 | л|0.0 = 1,42207 |
| Молекулярная рефракция MR-q.. | 25,45 | ί 25,40 найд. 1 24,33 выч. |
| Экзальтация. | — | 1,07 |
Изопрен легко присоединяет две молекулы водорода в присутствии металлич. катализаторов: никеля, платины, палладия. Конечным продуктом реакции является изопентан. В промежуточной фазе образуется смесь амиленов: изопропилэтилена, несимметрического метил-этилэтилена и триметилэтилена. Бром присоединяется в количестве двух молекул. Первая молекула присоединяется преимущественно к крайним углеродным атомам сопряженной системы:
СН2Вг - С : СН · СН2Вг
I
СНз
Вторая присоединяется значительно труднее. И дибромид и тетрабромид жидки. Хлористый и бромистый водород присоединяются легко, образуя при полном насыщении жидкие гидробромиды (или гидрохлориды), например СНз · СВг · сн2 СН2Вг
СНз
Эти соединения имеют существенное значение для выделения изопрена" в химически чистом состоянии из смеси других углеводородов. Подобно большинству сопряженных систем изопрен способен образовать соединение с сернистым ангидридом S02. Этот последний может быть взят для реакции и в газообразном состоянии и в виде водного раствора. Это соединение известно в двух формах: кристаллической и аморфной. Из первой изопрен можно регенерировать нагреванием; вторая при нагревании разлагается. Для количественного определения полимеризацией необходима, в виду способности изопрена увлекать в реакцию полимеризации некоторое количество триметилэтилена, что неблагоприятно отражается на качестве полимера. Большой интерес по своей значительной массе представляют те пентаны и пентены различного строения, которые образуются при пирогенизации нефти. При мощном развитии крекинга количество пентаново-пентеновой фракции будет велико, и ее выделение из продуктов крекинга не представит значительных затруднений. Очевидно м. б. использована и
изопрена пригодны дигидрохлорид и гидробромид; однако для получения точных цифр при посредстве этих соединений надо располагать значительным количеством анализируемого материала. Повидимому наилучшим анали-тич. методом является получение кристаллич. соединения изопрена с малеиновым ангидридом по методу Дильса [п].
Впервые изопрен был выделен Виллиамсом в 1860 г. из продуктов пирогенного разложения каучука; строение его было установлено работами Ипатьева, Мокиевсксго и Эйлера. Описано и запатентовано громадное количество способов получения изопрена. Здесь приведены лишь немногие способы для характеристики тех путей, по которым в этой области движется химическая мысль. Очевидно только тот способ может рассчитывать на успех, который имеет дешевую сырьевую базу. Сырьем настоящего момента служат: нефть и продукты ее крекинга, каменный уголь, а также получающиеся из него продукты (газ, деготь, первичная смола), целлюлоза, крахмал и получающиеся из них продукты (, сивушное масло, ацетон), скипидар, ацетилен. По каждой из этих категорий сырья зарегистрировано немало способов синтеза и вариантов этих способов.
1) При пирогенизации нефти [’] и ее погонов всегда образуется незначительное количество изопрена. Одна часть его находится в легких жидких продуктах пирогенизации, а другая в газообразных продуктах, откуда он может быть извлечен скрубберным промыванием или же комбинацией компримирования с охлаждением. Полученный таким способом изопрен смешан со значительным количеством других углеводородов, преимущественно триметилэтилена, от которых он неотделим перегонкой. Удобным методом очистки изопрена от триметилэтилена может служить образование нестойкого комплекса с полухлористой медью. Во всяком случае предварительная очистка изопрена перед пентановая фракция нефтей, хотя ее количество вообще в нефтях незначительно. Пути превращения в изопрен пентанов и пентенов различного строения хорошо изучены и теоретически и в лабораторном масштабе. Все три возможных пентана:
I. СНз-СНа-СНг-СНа-СНз,
сн3
и. >сн-сн2-сн3,
сн
СН3х /СНз
III. )с
СНз7 ХСЫ3
находятся в нефтях и повидимому с преобладанием второго находятся в продуктах пирогенизации нефтей. Второй из них имеет углеродный скелет тот же, что и изопрен, и переход от него к изопрену наиболее прост. Первый и третий тоже удается, хотя и более сложным путем, превратить в изопрен. Для всех трех пентанов первая фаза процесса одна и та же—хлорирование до получения монохлоропен-танов. Для возбуждения процесса хлорирования применяются или катализаторы или ультрафиолетовый свет ртутной лампы. Во второй фазе смесь изомерных хлоропентанов подвергается нагреву 400-^450° в присутствии извести или катализаторов (например ВаС12) для отщепления молекулы хлористого водорода. При этом хлориды пентанов типа 11 и III образуют почти исключительно триметилэтилен [хлорид пентана (III) с изменением углеродного скелета]; хлориды нормального пентана (I) образуют два изомерных пентена нормального же скелета. Эти последние по указаниям патента BASF могут быть с хорошими выходами изо-меризованы в триметилэтилен пропусканием над окисью алюминия при 450°. Полученный во второй фазе триметилэтилен действием хлора превращают в дихлоризопеитан. Наконец последний, теряя две молекулы хлористого водорода при повышенной t° в присутствии изве-
сти или катализаторов, образует изопрен. Для изопентана реакция имеет следующий вид:
(СНзч СНзч
^СН.СН2-СН3+С12=_ >СС)-СН2СНз + НС1,
I.
i СН3/ ~ СНз7
1СНзч СНз
>СН.СН2-СНз+С12= (СНз СН3
СН-СНСЬСНз + НС1,
II.
III.
СНзч СНзч
_)-ССЬСН2-СНз-НС1 =___)С : СН-СН3,
СНз
СНз·
СНзч СНзч
>СН-СНС1-СНз-НС1= >С : СНз
СНз
СНзч
СН-СНз,
IV.
СНз
СН3.
С : СН-СН3+С12 =
СН3.
N
ССЬСНСЬСНз,
СС1-СНС1-СНЗ-
СН3
СН2,Ч
2НС1=УС-СН СНз7
СН2.
СН3
Вариантом описанного выше способа является процесс дальнейшего хлорирования до ди-хлорица (при действии ультрафиолетовых лучей) полученных в первой фазе монохлоридов изопентана с последующим отщеплением двух молекул хлористого водорода. сн3.
СНз
СС1-СН2-СН3+С12=
сн3.
СНз
ССЬСНСЬСНз+HCI,
СНзч СН2 : С-СН : СН2
>СС1.СНС1-СН3-2НС1=I СН3 СНз
2) Сивушное масло, кипящее ок. 130°, представляет смесь амиловых ов [7]:
СНзч г. >СН-СН2-СН2ОН,
сн3
СН2(ОН)ч
II. >СН-СН2-СНз СН3
со значительным преобладанием первого. Углеродный скелет обоих ов тот же, что и у изопрена. Можно наметить два пути для перехода от этих ов к изопрену. По первому пути отщепляют от этих ов воду пропусканием паров изоамилового а над окисью алюминия при 400°. В результате появляются три амилена, приблизительно в равных количествах: сн
I. ^СН-СН : СН2:
СНз сн3.
II. >С:СН.СНз,
сн3
СНзч
III. >С-СН2-СНз.
Clh"
Действием хлора они превращаются в соответственные дихлориды; последние, отщепляя по две молекулы НС1 при высокой 4° в присутствии катализаторов, образуют изопрен. Нормальным продуктом реакции отщепления НС1 при низких температурах являются не изопрен, а соответственно: а) изопронилацетилен, б) диметилаллен и в) непредельный монохлорид; поэтому необходимо допустить во время реакции изомерное превращение исходных хлоридов в такие изомеры, к-рые, отщепляя 2НС1, образуют изопрен. Частично происходит и изомеризация готовых углеводородов в изопрен, к-рый при повышенных t° является повиди-мому наиболее стойким изомером. Второй путь превращения амиловых ов сивушного масла в изопрен заключается в превращении ов в монохлориды действием хлористого водорода и в дальнейшем хлорировании монохлоридов до дихлоридов с последующим контактным отщеплением 2НС1 при высокой 4°. Все операции, производимые при высоких t°,
ведутся при разрежении для предохранения образовавшегося изопрена от разрушения.
3) Способ получения изопрена из скипидара Г12] сводится к пирогенному его разложению. В 1884 г. Тильден при пропускании скипидара через нагретую докрасна железную трубку получил ок. 6% сырого изопрена. В. А. Мокиев-ский показал, что этот сырой изопрен представляет собою смесь почти равных количеств изопрена и триметилэтилена. Впоследствии было установлено, что различные углеводороды, входящие в состав скипидара, далеко не одинаково, пригодны для получения изопрена. Хорошие выходы получаются из дипентена, лимонена, карвестрена (сильвестрена) и тех углеводородов, которые могут изомеризоваться в только что перечисленные. Объясняется это тем, что ди-пентен и сильвестрен являются димерными формами изопрена, и образование из них изопрена является естественным процессом диссоциации этих димерных форм.
| СНз
1 |
СНз
1 | |
| ;*С
сн сн2 |
/с
СН СН2 | |
| i i | II | |
| сн2 сн2 | сн2 сн2 | |
| сн | СП | |
| 1
п |
1
cv | |
| СН2 СНз | СВГ2 СНз |
дипентен изопрен
Существенные усовершенствования этого процесса были внесены Зильберрадом и Штаудин-гером, которые показали, что применение при реакции пирогенного разложения дипентена пониженного давления или разведения паров дипентена инертными газами значительно повышает выходы изопрена, предохраняя образовавшийся изопрен от разложения. Той же цели достигает и быстрое удаление изопрена из области высоких t° (закалка). При соблюдении этих условий Штаудингеру удалось повысить выход сырого изопрена до 60%. Прибор, в котором получают изопрен пирогенизацией скипидара или его фракций при соблюдении упомянутых выше условий, носит название изо пр е-новой лампы. Существенной частью этого прибора является накаливаемая током спираль и в ме-таллич. проволоки, через витки которой проходит пар разлагаемого материала.
4) Значительный интерес представляет синтез по способу Мерлинга из ацетона и ацетилена. Так как ацетон сейчас синтезируется из ацетилена, то материалом для этого синтеза изопрена можно считать один ацетилен. Реакция проводится через натриевое производное и ведет к образованию а, содержащего в молекуле ацетиленовую связь. Ацетиленовую связь затем восстанавливают до этиленовой; от полученного т. о. непредельного а отщепляют воду и получают изопрен. Схема реакции такова:
сн3 сн3 сн3
С—СН2+НС: СН-*СН3-С-С ·СН - СН3- С-СН : СН2 —
I I I
ONa ОН ОН
СН3
-> СН2 : С · СН : СН2.
По своей сложности и дороговизне синтез по способу Мерлинга пока имеет лишь теоретический интерес. В нем однако возможны значительные усовершенствования.
Диизопропенил [7], иначе β, у-диме-тилдивинил, иначе диметил-2,3-бутадиен-1,3:
сн2=с-с=сн2
с!н3 сн3
Бесцветная жидкость, t°Kun. 69°; ГГ ’=0,7304; Лд’5=1,44321. Молекулярная рефракция ΜϋΏ(найдено)=27,77; для ф-лы СвН10МЛо (вычислено)=28,97; отсюда экзальтация=0,80. Этот углеводород, подобно бутадиену-1,3 и изопрену, способен присоединять два и четыре атома брома, одну и две молекулы галоидоводородных кислот. Первые два атома брома присоединяются с большой легкостью. Получающийся при этом кристаллик. дибромид С6Н10Вг2, плавящийся при 48°, может служить для характеристики диизопропенила. Диизопропенил получается из ацетона. Ацетон превращают в пи-након путем восстановления, которое может быть осуществлено по способу Голлемана действием амальгамы магния. Магний м. б. заменен алюминием. Во время войны 1914—18 гг. германцы применяли восстановление ацетона метал-лич. алюминием в едком натре:
2СН3 · со -CH3+Mg= (СНз)2С—С(СНз)2;
(СНз)зС—
I
Mg
-С(СНз)2
I
о
О
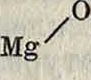
+ Н20(СНз)2С(0Н)-С(0Н) (СНз)2.
Пинакон после отщепления двух молекул воды превращается в диизопропенил. Отщепление воды производится нагреванием в присутствии катализаторов (А1.203, KHS04 и др.) или перегонкой под давлением. Т. к. исходным материалом для получения диизопропенила всегда является ацетон, то вариации способа получения этого углеводорода сводятся к различным способам получения ацетона. В настоящее время серьезное значение имеют два способа получения ацетона: 1) брожение глюкозы и других углеводов (параллельно с получением га-бутилового а) и 2) синтез из ацетилена через альдегид (по реакции М. Кучерова) и уксусную кислоту (или же из ацетилена в ацетон в один производственный прием).
Полимеризация. Вторая ^ основная операция в синтезе каучука заключается в превращении углеводорода ряда бутадиена (или его производного) в высокомолекулярную форму, б. или м. приближающуюся по свойствам к природному каучуку. Этот процесс носит название поли-меризац и и. Для углеводородов ряда бутадиена его можно выразить общим ур-ием:
хСАп-з=‘сАп.Лх.
Для каучукоподобных полимеров величина их повидимому варьирует в пределах от нескольких сот до нескольких тысяч. Скорость процесса полимеризации для различных производных бутадиена-1,3 колеблется в очень широких пределах. В зависимости от условий (г°, освещение, наличие полимеризующего агента, присутствие стимулирующих или тормозяш.их примесей) получаются полимеры различного частичного веса и различных свойств.
Ауто- и термополимеризация. Полимеризация чистых бутадиена, изопрена и диизопропенила при комнатной или слегка повышенной ί° ведет к образованию только каучукоподобных полимеров высокого частичного веса. Хотя качество получаемого при этом каучука высокое, но по своей медленности этот процесс не имеет практич. значения. При повышении г° скорость процесса быстро нарастает, но при этом часть углеводорода полимеризуется в димерную форму. Количество последней с повышением t° быстро увеличивается. Так, для диизопропенила при £°, не превышающих 50°, димер практически не образуется. При 100° образуется около 60% димера и при 150° около 80%. Образование ди- и полимерной формы для бутадиена может быть представлено ур-иями [*]:
I.
сн
X
сн
II
сн2
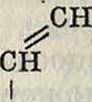
сн2
I
| сн2 | сн2 сн2 |
| -» | |
| сн | сн |
| сн | 1
сн |
| II | II |
| сн2 | сн2 |
И. х (СН2 : СН · СН : СН2) — (- СН2 · СН : СН · СН2 —
-СН2-СН :СН-СН2-СН2-СН : СН-СН2 - и т. д. х раз).
Т. к. непосредственное превращение димера в полимер невозможно, то димеры, представляющие собою скипидароподобные жидкости, являются пока труднореализуемыми отходами. По· своему строению полимеры, получающиеся из чистых, углеводородов при комнатной температуре и при нагревании, близки к природно-. му каучуку. Чрезвычайно своеобразный тип автополимеризации был описан И. Кондаковым [13] для диизопропенила. При хранении этот жидкий углеводород постепенно на протяжении нескольких месяцев превращается в· белоснежную рыхлую каучукоподобную массу, нерастворимую в обычных растворителях, а лишь набухающую. Впоследствии такой же тип полимеризации был наблюдаем и у изо-, прена и у дивинила. Легкость образования этой формы возрастает в ряду дивинил—изопрен— диизопропенил. Этого типа полимер диизопропенила под названием «метил-каучук Н>> был использован в Германии во время войны 1914— 1918 гг. Строение полимеров этого типа недостаточно разъяснено.
Полимеризация под влиянием света. Факт, что освещение вызывает полимеризацию многих непредельных веществ, установлен давно. Известно, что дивинил, изопрен и диизопропенил превращаются в высокомолекулярные формы под влиянием ультрафиолетовых лучей. По данным Гарриеса изопрен при этом образует преимущественно твердое каучу-конодобное тело. Систематические исследования по действию света на углеводороды с сопряженной системой двойных связей не опубликованы.
Полимеризация под влиянием катализаторов. Большое число патентов описывает полимеризацию дивинила и его гомологов в присутствии различных возбудителей процесса: 1) к-т (преимущественно уксусной) и веществ типа хлорангидридов, 2) кислорода, озона, соединений, содержащих непрочносвязанный кислород (например перекиси, окисленный скипидар), 3) метеллоорганических соединений, амида натрия, 4) щелочных и щелочноземельных металлов. Большинство этих способов полимеризации не имеет реальной ценности; серьезное значение имеют лишь возбудители группы (4) и в особенности металлич. натрий. Способность металлич. натрия вызывать полимеризацию дивинила и его гомологов была впервые подмечена Метьюсом и Стрен-джем [*]. В зависимости от материала и условий процесс длится от нескольких дней до не скольких недель. Темп-pa процесса не должна превышать 60—70° во избежание образования димерных форм. Металлич. натрий вводят в форме проволоки, дисперсии или коллоидного раствора. Количество его должен быть тем меньше, чем удельная поверхность его больше; оно варьирует от малых долей процента для коллоидного раствора до 0,5—2% для проволоки. Этот способ полимеризации имеет особенно важное значение для получения дивинилового каучука. Исследования на опытном заводе лит. Б в Ленинграде показали значительную гибкость этого способа. В зависимости от условий процесса он может дать каучукоподобные полимеры, растворимые в обычных растворителях (эфир, хлороформ, бензол) или нерастворимые, мягкие или жесткие. Вариация свойств обусловлена величиной мол. веса и возможно различием в строении.
Полимеризация в каучукоподобные полимеры сопровождается громадным сжатием и выделением значительного количества тепла. Сжатие при образовании из мономера каучу-конодобных полимеров колеблется для различных углеводородов и различных типов полимера от 20 до 30%. Для дивинила оно близко к 30%. Тепловойэффект полимеризации изопрена в природный каучук равен 450 cal/г Г15]. Для различных полимеров дивинила тепловой эффект полимеризации колеблется в довольно широких пределах: 315—415 cal на г вещества; для растворимых форм—ниже; для нерастворимых форм—выше (для расчета взята теплота полимеризации жидкого дивинила). Столь значительный тепловой эффект полимеризации при малой теплопроводности каучука обусловливает необходимость проведения полимеризации в длительные сроки или применения специальных средств для отвода теплоты реакции. При несоблюдении этих условий подъем температуры на больших установках может вызвать обугливание полимера.
Свойства синтетических каучуков. На основании опубликованных до сих пор материалов лишь очень немногие С. к. могут быть характеризованы с удовлетворительной полнотой. Характеризованы м. б. разновидности диизопро-пенилового каучука на основе опыта Германии во время войны 1914—18 гг., а также дивиниловые каучуки на основе данных опытного завода лит. Б в Ленинграде. Для характеристики изопреновых каучуков имеются лишь отрывочные и недостаточные сведения. Есть указания, что изопреновый термополимер наиболее приближается по свойствам к природному каучуку, с которым он имеет одинаковый исходный материал (изопрен) и сходную химич. природу. С. к. присущ ряд признаков, отличающих их от природного.
О к и с л я е м о с т ь, стабилизация. Почти все типы синтетического каучука энергично окисляются кислородом воздуха. Окисление тем энергичнее, чем каучук жестче и чем развитее его поверхность. Особенно энергично поэтому окисляется губкоподобный автополимер, описанный Кондаковым для диизопропе-нила, и аналогичные полимеры дивинила и изопрена. Также чрезвычайно энергично окисляются рыхлые вальцованные шкурки из натрий-дивммл-каучука. Длительное хранение таких сортов каучука невозможно. Окисляясь, каучук теряет свои эластич. свойства и через несколько недель или месяцев превращается в хрупкий «сухарь». При неумелом хранении кип такого каучука может наступить самовозгорание, подобно самовозгоранию кип хлопка. Это невыгодное свойство С. к. совершенно устраняется введением антиоксидантов, или стабилизаторов, каковыми являются многие органические основания, многоатомные фенолы и др., например введение путем вальцевания 0,5—1% альдоль-а-нафтиламина (Age-Rite) совершенно предохраняет от окисления натрийдивиниловый каучук. Относительно малая окисляемость природного каучука обусловлена наличием в нем стабилизирующих веществ (органических оснований и смол), попадающих в него из латекса при коагуляции.
Ограниченная способность переходить в пласт и ч. состояние. Характерная способность природного каучука переходить в пластич. состояние при механич. обработке на вальцах у некоторых типов С. к. отсутствует совсем, у других выражена очень слабо. С. к. упорно сохраняет свой «нерв». Это обстоятельство затрудняет получение гладкой каландровой пластины из мало наполненных смесей синтетического каучука, а также конфекцию изделий.
Пониженная клейкость. Смеси из С. к., в особенности из сухих типов, обладают пониженной клейкостью по сравнению со смесями из натурального каучука. Хотя свежеобнаженные поверхности таких смесей обладают клейкостью, приближающейся к таковой натурального каучука, она обычно сохраняется недолго и быстро падает. Это обстоятельство затрудняет конфекцию изделий из С. к., т. к. те десятки мин., в течение которых сохраняется клейкость,—срок недостаточный в производстве. Недостаточная пластицируемость и клейкость—два характерных свойства С. к., к которым придется приспособиться резиновой пром-сти. Хотя С. к. поддаются обработке на обычной аппаратуре, применяемой на резиновых заводах для обработки природного каучука, но надо думать, что оригинальные свойства С. к. вызовут к жизни новые и оригинальные способы обработки и новую аппаратуру.
Вир ы С. к. Диизопропениловый каучук. В Германии во время войны было приготовлено свыше 2 000 тонн этого каучука [16]. Готовилось три сорта каучука. Один из них под названием мети л-к а у ч у к W получался полимеризацией диизопропенила нагреванием до 70° в течение примерно пяти месяцев и имел вид прозрачной вязкой желтоватой массы. Другой сорт—м е т и л-к а у ч у к Н—белоснежный губчатый автополимер, полученный холодным способом по Кондакову. Наконец третий сорт получался полимеризацией металлическим натрием в присутствии углекислого газа. Это мети л-к а у ч у к В. Все три сорта обладали рядом недостатков, из которых наиболее существенным является недостаточная эластичность (кожистость) при обычных 1°-ных условиях и почти полная потеря эластичности на холоду. Марка W после мастика-ции может быть растворена. Она применялась для изготовления изделий (шин и прочие). Марка Н служила для приготовления эбонита, по элек-трич. свойствам не уступающего эбониту из натурального каучука. Марка В применялась гл. обр. для изготовления кабелей. После войны производство метил-каучуков было прекращено вследствие низкого качества каучука и его высокой стоимости (15 руб. за кг во время войны 1914—18 гг., 7 р. 50 к. после войны).
Бутадиеновый (д и в и н и л о в ы й) каучук. Для дивинила известны следующие полимеры: термополимеры, губчатый автопо лимер и натрий-полимеры. Термополимер иввестен в двух модификациях: растворимой и нерастворимой; обе образуются одновременно со значительным преобладанием нерастворимой формы. Термополимер с трудом обрабатывается на вальцах; смеси имеют кожистый характер; вулканизованные—мало прочны. При полимеризации дивинила, содержащего примеси, характер термополимеризата существенно изменяется. Свойства этого каучука мало изучены. По качеству он во всяком случае ниже натрийбутадиен-каучука. Повидимому термополимеризация как метод получения бутадиен-каучука может сохраниться лишь в тех случаях, где натрий неприменим. Такой случай представляет дивинил, получаемый пирогенизацией нефти и ее фракций и неочищенный от углеводородов, реагирующих с натрием (однозамещенные ацетилены, циклопентадиен). Темп-ры, применяемые для термополимеризации, варьируют от 60 до 100°. Дальнейшему повышению темп-ры с целью ускорения процесса препятствует значительное образование димерной формы. Введение веществ, подверженных таутомерным превращениям или легко окисляющихся, ускоряет процесс образования полимера (Б. Бызов). Автополимер губчатый для дивинила был получен лишь в очень небольших количествах; он близок по свойствам к метил-каучуку Н, описанному выше. Изучение его только начинается. Натрий-б у т а д и е н-к а у ч у к [7, 17] получил наибольшее значение в синтезе каучуков как по удобству и легкости получения, так и по качеству получаемой из него резины. Чистый дивинил в присутствии 0,5—1% натрия в форме тонкой проволоки, равномерно распределенной в массе дивинила, по димеризуется нацело в 2—5 дней. Для заводского дивинила вследствие наличия примесей этот срок увеличивается до 10 и более дней. Характер полимеризата подвержен колебаниям в зависимости от примесей, типа примененного натрия, его распределения и температуры процесса. Для дивинила, получаемого из а по описанному выше способу Лебедева, свойства полимеризата варьируют от очень сухого, трудно поддающегося обработке, до мягкого. Чем чище дивинил, чем меньше натрия, тем вообще суше получается полиме-ризат. Пластичность (по Карреру на приборе Вильямса) полимера, удобного для обработки, колеблется от 0,05 до 0,35. Хорошего качества натриевый полимеризат бутадиена представляет почти бесцветную, очень упругую, прозрачную массу, почти не деформирующуюся при хранении, уд. в ок. 0,89 (20°). В тех случаях, когда этот каучук предназначен для изоляции и некоторых других специальных задач, его на вальцах отмывают от натрия и сушат в виде листов в вакуум-сушильных аппаратах. Если такие задачи не ставятся, каучук м. б. обработан вместе с заключенным в нем натрием, который при этом окисляется и связывается вводимыми примесями. Отмытый от натрия на вальцах, этот каучук представляет б. или м. рыхлую шкурку, почти бесцветную. Высушенный в атмосфере азота, этот каучук содержит около 0,2% золы. Беззольная часть имеет следующий средний состав: 88,75% С, 11,09% Н, 0,16% О. При хранении на воздухе такой каучук жадно поглощает кислород, теряя постепенно упру гие свойства и через несколько месяцев превращается в «сухарь»; он энергично поглощает кислород при обработке на вальцах; так, при мастикации в течение 30, 45 и 60 мин. количество кислорода в каучуке возросло соответственно на 0,25, 1,0 и 0,2%. Введение в натрий-бутадиен-каучук обычных для природного кау-. чука антиоксидантов (Age-Rite, Neoson-D.) в количестве 0,5—1%, как показали двухлетние наблюдения, совершенно его стабилизует. Растворимость для натрийбутадиен-каучука не является характерной константой; она варьирует очень широко от легкой растворимости в эфире, бензоле, бензине, хлороформе и других растворителях до полной нерастворимости в этих жидкостях. Растворимость зависит от условий полимеризации, от термич. обработки, от степени окисленное™. Все условия, ведущие к получению сухого полимера высокого молекулярного веса, ведут к уменьшению растворимости. К этому же ведет длительная термич. обработка. Нерастворимые формы лишь набухают. В метиловом и этиловом ах все типы натрийбутадиен-каучука нерастворимы. Отношение к повышенной г° натрийбутадиен-каучука сухого типа очень характерно и резко отличается от поведения природного каучука. В то время как при нагревании природного каучука до 75° он сначала приобретает липкость и наконец совсем раскисает, натрийбута-диен-каучук в этих условиях внешне совершенно не изменяется. В структуре натрийбутадиен-каучука однако при этом происходят значительные изменения (циклизация, изомеризация); растворимость уменьшается; убывает и склонность к реакциям присоединения.
Механические свойства резины из натри йбутадие н-к а у ч у к а колеблются в широких пределах в зависимости от типа полимеризата. Сухой тип дает резину более прочную, чем мягкий тип. Вулканизация смесей несколько замедлена по сравнению с таковой для натурального каучука, но легко поддается регулированию действием обычных ускорителей вулканизации. Вулканизат из натрийбутадиен-каучука, серы и ускорителя обладает ничтожной прочностью. Так, смесь состава 100 ч. натрийбутадиен-каучука, 3,5 ч. серы и 0,25 ч. тиурама дает следующие показатели при испытании на разрыв-
Продолжительность вулканизации в мин..
Прочность в к г/см2.
Относительное удлинение в %. Остаточное удлинение в %.
| 40 | БО | 60 |
| 5 | 6 | 4 |
| 840 | 444 | 472 |
| 48 | 12 | 4 |
Механич. прочность С. к. приобретает от введения в него активных наполнителей, обладающих большой степенью дисперсности. По величине усиливающего эффекта их можно распределить в следующий ряд: газовая сажа, ламповая сажа, каолин, окись магния и углекислая магнезия. Лучшие результаты дает газовая сажа при введении ее в смесь в количестве 50—75% по весу от каучука. Для хороших сортов натрийбутадиен-каучука прочность на разрыв составляет 200 килограмм/см2. Ламповая сажа из того же каучука дает резину с прочностью не выше 150 килограмм/см2. Лучшие сорта каолина дают смесь с прочностью 100 килограмм/см2. Для каолинов с меньшей степенью дисперсности прочность падает до 70 килограмм/см2 и даже еще ниже. Для примера ниже приведен рецепт смеси для шинного протектора и результаты ме,ханич. испытаний; 100 ч. каучука, 4 ч. серы, 65 ч. сажи арроу-
блек, 10 ч. окиси цинка, 4 ч. стеариновой к-ты, 10 ч. руберакеа, 1 ч. дифенилгуанидина, 1 ч. альдоль-α-нафтиламина. Вулканизация в течение 130 мин. при давлении пара в 3 килограмма. Прочность (в кг/см2) 159; относительное удлинение 712%; остаточное удлинение 38,9%.
Эксплоатационная выносливость изделий из натрийбутадие н-к а у-ч у к а. На опытном заводе лит. Б в Ленинграде были изготовлены из натрийбутадиен- каучука следующие .изделия, бывшие в эксплуатации на протяжении 11/2 г. и после окончания службы подвергнутые испытанию. 1) Автомобильные шины с поверхностью из С. к. на каркасе, промазанном натуральным каучуком: усилителем служила газовая сажа; пробег первых трех шин до выхода из эксплуатации 16 и 18 тыс. км. 2) Автомобильные шины с тою же поверхностью и каркасом, промазанным С. к. с каолином в качестве усилителя: первые шины этого типа показали значительно меньший пробег— 74-12,5 тыс. км. 3) Калоши из натрийбутадиен-каучука: в эксплуатации выносливость, не уступающая изделиям из натурального каучука.
4) Прорезиненные ткани в форме макинтошей по выносливости не уступают тканям, прорезиненным натуральным каучуком.
Хлоропрен [10]. Особняком стоит недавно изготовленный фирмой Du Pont de Nemours в США хлоропрен СН2 : CCI · СН : СН2 и полученный из него каучук, обладающий хорошими механич. свойствами. Он характерен тем, что не требует вулканизации и напоминает вулканизованный природный каучук. Исходным материалом является ацетилен, который под влиянием водного раствора полухлористой меди способен полимеризоваться в винил-ацетилен: СН · С СН : СН2. Последний, присоединяя хлористый водород, образует хлоропрен. Это бесцветная жидкость; t°Kun 59,4° при 760 миллиметров и
6,4° при 100 миллиметров·, —1,4583. Молекулярная рефракция найденная МAd 25,26, вычисленная—24,66. Вязкость при 25°=0,394 центи-пуазам. Из химич. свойств характерна чрезвычайная прочность атома хлора как в мономере, так и в полимерах. Хлоропрен легко присоединяет два атома брома; реагирует с малеиновым ангидридом. Полимеризация хло-р о п р е н а происходит при его хранении: он постепенно густеет, остудневает и дней через 10 превращается в плотную эластичную массу, названную μ-полимером. Он напоминает вулкан зованный каучук. Свойства μ-полимера: i?20=1,23, π2»=1,5512; прочность на разрыв
140 κι/см2, относительное удлинение 800%; непластичен, не дает 1ладко.о листа при вальцевая и. Он набухает, но не растворяется в обычных растворителях каучука. Если полимеризацию прервать, не доведя ее до конца, то получается пластичный вполне растворимый α-полимер. Он способен обрабатываться на вальцах. При 30° он теряет свою пластичность, превращаясь в μ-полимер через 48 час. При 130° процесс превращения заканчивается в 5 минут. Строение е<о предпола: ается аналогичным природному каучуку с заменой метиловой группы хлором: [—СН2 · СС1:СН · СН2 · СН · СС1: :СН-СН2—]х. Списаны и нек-рые другие полимерные ()ормы хлоропрена. Хлоропреновые к у-чуки еще мало изучены. Об эксплуатонной их прочности сведений нет.
Лит.: 1) Конд 1ко в И., Синтетич. каучук, его го-мология и аналоги, Юрьев, 1912; 2) л е б еде в С., Иссле дование в области полимеризации двуэтиленовых углеводородов, «Ж», 1910, 1911 и 1913; его же, Исследование в области полимеризации двуэтиленовых углеводородов, СПБ, 1913; 3) Harries С., Untersuchungen iiber die natiirlichen u. ktinstlichen Kautschukarten, B., 1919; 4) Hofmann F., «Ζ. ang. Ch.“, 1912, B. 25, p. 1465; 6) Остром ысленский, «Ж», 1915, 1916; e г о ж e, Каучук, М., 1914; 6) z 1 e g 1 е г К. u. В a h г, «В», 1928, В. 61, р. 253; ?) S с h о t г S., Synthetic Rubber, L., 1926; 8) Лебедев С., Получение дивинила из нефти и ее фракций, «Синтетич. каучук», М., 1932; 8) е г о ж е, Сов. П. 24393/1928; И) Du Pont de Nemours et Со., «The Journ. of the American Chemical Society», Wsh., 1931; В) n i eis u. A I der, «B», 1929, B. 62, p. 2337: 12) Staudinger u. Klever, ibid., 1910, B. 64, p. 2212;!3) Kondakoff, «Journ. f. prakt. Chemie», 1901; n) Matthews, Strange, Ан. Π. 24790/11910; WlGei-g e r, Ueber die Konstltution der Hochpolymeren, Zurich, 1926; ιβ) Burgdorf C., Artificial Rubber During the War in Germany, «I.Eng. Chem.», 1926, 11; l?) Memmler, Hndb. d. Kautschuk-Wissenschaft, Lpz., 1930. С. Лебедев.
С И Η T 0 h, кислородсодержащая сложная маслянистая смесь, получаемая из окиси углерода при контактных процессах переработки (Ф. Фишер, 1913). Процесс образования С. в основном является процессом гидрирования (смотрите) окиси углерода (смотрите Жидкий уголь).
Появление жидких кислородсодержащих продуктов реакции наблюдается только тогда, когда процесс контактного восстановления окиси углерода ведут при увеличении давления. Такой метод получения жидких соединений запатентован Баденской анилиновой и содовой ф-кой (BASF) еще в 1913 году Несколько времени спустя той же проблемой получения жидких продуктов из окиси углерода под давлением занялись Фишер и его сотрудники. Ими было установлено, что для приготовления катализатора безусловно должно употребляться железо, к-рое в таких условиях предпочтительнее, чем кобальт и никель. Железные опилки обрабатывались едким калием и высушивались. Применяя специальный циркуляционный аппарат, в котором реакционные газы при давлении в 150 aim многократно прогонялись через трубку с катализатором, нагретую до 400—450°, Фишер получал смесь жидких продуктов. Такая жидкая смесь состояла из двух слоев—одного водного, содержащего ы, альдегиды, кетоны, кислоты и воду, и другого—маслянистого, которого получалось по объёму раза в два больше, чем водного. Из к-т были обнаружены (в обоих слоях) следующие: муравьиная, уксусная, про-пионовая, изомасляная и повидимому высшие, прямого определения которых однако не делалось. Альдегиды, присутствующие гл. обр. в маслянистом слое (до 21%), содержали пропио-новый альдегиды альдегид масл ных к-т и ряд других высших адельгидов. Присутствия формальдегида обнаружено не было; из ов в значительных количествах присутствовали: метиловый, этиловый, нормальный пропиловый; из кетонов—ai етон, метила, етон и /ругне. Кроме этих соединений в масле приеутствовали углеводороды (до ;.%) и э,иры. После отделения водного слот главная маслянистая часть о ладала следующими гвойствами удельный вес — 0,8289; содержание углерода ~ г,0% и водорода—12%; высшая теплотворная способность 8 200 Cal,· “. г, низшая теплотворная способность 7 5.0 Cal/«; темп-ра застывани ι ниже — Ь0°; границы кипения: до 100° п регон ется около 40%, до 100° перегоняется около 91%; продукт о ладает очень низкой температурной вспышкой. Все приведенные данные показывают пригодность продукта дл употр, бления его в качестве моторного топлива. Особенно благопри тные р зультаты получались при употреблении смеси синтола с бензолом.
Практич. значение синтолового процесса заключается в том, что он открывает возможности получения из дешевых углеродистых веществ (уголь, торф и дерево), переходя через окись углерода, ценных синтетич. продуктов. Вместе с тем на пути практич. использования синтолового процесса стоят значительные препятствия, заключающиеся гл. обр. в трудности разделения получающихся продуктов.
С и н т и н — продукт, получаемый из С., отличающийся от него значительно меньшим содержанием кислорода, если не полным отсутствием последнего. Синтии состоит гл. обр. из углеводородов. Процесс получения синтина осуществляется Ф. Фишером след, обр.: фракция С., кипящая от 100 до 225°, подвергается нагреванию до 420° в течение часа под избыточным давлением. После этого продукт оказывается разделенным на два слоя—верхний водный и нижний маслянистый, составляющий основную массу. Исследование этой маслянистой фракции показало, что она в основном состоит из углеводородов, кипящих как ниже исходной (ниже 100°), так и выше ее (до 300°) и с переменным отношением С : Н=1,5 : 2,2. Следует указать, что нагревание С. не в автоклаве, а при обыкновенном давлении ведет к обратному процессу: С. распадается на газообразные продукты и уголь. Образование синтина по Ф. Фишеру происходит т. о., что сначала из ов с отщеплением воды возникают непредельные углеводороды, а эти последние под влиянием давления конденсируются в нафтеноподобные углеводороды. Возможность последнего превращения экспериментально доказана Ипатьевым; за эту же схему говорит высокое содержание олефинов в газе, образующемся при нагревании С. в автоклаве. Кроме работ Ф. Фишера имеются и другие работы, осуществляющие аналогичный процесс получения различных углеводородов путем нагревания разных кислородсодержащих органич. соединений в присутствии угля {или без него) до г° в 500—600° и при избыточном давлении. Получающийся при этом маслянистый продукт перегоняется:
ДО 1С0° 150° 200» 250° 300°
17% 35% 57% 74% 84%
Фракции ниже 100° обладают запахом бензина. Фракции выше 100° растворяются в конц. серной кислоте на 50% (С. растворяется целиком). Часть, не растворимая в серной к-те, после очистки и перегонки оказалась состоящей из углеводородов. Продукты, растворимые в серной к-те, содержали: углерода ок. 80%, водорода ок. 12% и кислорода ок. 8%.
Лит.: Фишер Ф., Искусственное получение жидкого топлива, пер. с нем., Л., 1927; E 1 1 i s С., Hydrogenation of Organic Substances, N. Y., 1930; Sabatier P., Die Katalyseind. organisehen Chemie, B., 1927; R i d e a 1 E.K., I’aylor H. S., Catalysis in Theory a. Practice, L., 1926; Jiselier F., Tropsch H., «Brennstoff-Chemie», Essen, 1923, p. 193, 275, 281; «B», 1923, B. 56, p. 2436, 2728; Ibid., 1926, B. 59, p. 830, 923; «Abh. d. Kohle», 1921, B. 6, p. 382; Ipatiew W., <-B», 1911, B. 44, p. 2978; I p a 11 e w W. u. Kljukwin N., Ibid., 1925, B. 58, p. 4; К о b a v a s h i, J a m a m о t o, «Journ. Soc. Chem. Ind. Japan», 1929, v. 32, p. 23; «Brennstoff-Chemie», 1929, В. 10, p. 134; Frolicb К., «Ind. Eng. Chem.», 1931, v. 23, p. 1386; Morgan G. T., «Proceed, of the Royal Soc.», L., 1930, V. 127, p. 246; Guerbet M., «CR», 1901, t. 128, p. 511; Weizmann, fiartard, «.Tourn. of the Chemical Society», L., 1920, p. 334; A d k i n s, К i n-s e y,-F о 1 k e г s, «Ind. Eng. Chem.», 1930, v. 22, p. 1046; Brown, G a 1 1 о w a v, ibid., 1928, v. 20, p. 960; 1929, V. 21, p. 310; 1930, v. 22, p. 175; G r a v e s G. D., ibid., 1931, v. 23, p. 1381; Smith, Davis, Reynolds, ibid., 1928, v. 20, p. 462; Schuftan P., «Z. ang. Ch.», 1926, B. 39, p. 276; Ф. П. 605839/1925; BASF, Г. П. 293787 (295202, 295203)/1913; Ан. П. 254760/1925; Ф. П. 593942/1925; 623068/1926; 598447/1925; 450543/1923;
32812 (1930). П. Зимавов.
T. Э. m. XX: