 > Техника, страница 91 > Цианамид кальция
> Техника, страница 91 > Цианамид кальция
Цианамид кальция
Цианамид кальция, кальций-цианамид, CaCN2 — кальциевая соль цианамида (смотрите) CN · NH2; обладает структурой Ca=N—CEN. Чистый Ц. к. представляет бесцветные кристаллы, уд. в 2,3, возгоняющиеся при 1° 1 090°; он, умеренно растворим в воде (2,5 : 100 при 25°) и нерастворим в е. В вддных растворах Ц. к. быстро гидролизуется, переходя в более растворимую кислую соль состава (CN · NH)2Ca; последняя тоже непрочна и в дальнейшем распадается, образуя мочевину CO(NH2)2, дициандиамид (CN2H2)2 и другие продукты. Аналогичные процессы идут под действием на Ц. к. углекислоты и влаги воздуха: сначала образуется кристаллич. соединение CaCN2 · С02 · 5Н20, затем (через свободный цианамид) продукты гидролиза—мочевина и др., вплоть до угольной кислоты и аммиака. Такая же цепь реакций имеет место при внесении Д. к.^в почву в качестве удобрения. При взаимодействии CaCN2 с сернокислым алюминием, а также при пропускании С02 в раствор (CN · NH)2Ca (на холоду) получается свободный цианамид. Ц. к. устойчив при t° до 1 350°; выше 1 400° наступает диссоциация (CaCN2==Ca-f C + N2), которая при 1 600° делается полной. Технич. Ц. к.—порошок или зерна тем-Hocepojo цвета с содержанием CaCN2 49-i-66%; темный цвет продукта обусловлен присутствием мелко раздробленного графита.
Получение. Чистый CaCN2 м. б. получен по способу Франка—действием паров синильной кислоты на известь при t° 800—850°:
СаО + 2 HCN=CaCNa + СО + Н2 (1)
пли по способу Камеяма—взаимодействием извести с дициандиамидом при 900—1 000°:
2 СаО + (CN2H2)2=2CaCN2 + 2Н20. (2)
Для промышленных целей Ц. к. получают исключительно по способу Франка и Каро— путем азотирования карбида кальция свободным азотом при t° 1 000—1 100°. Реакция
CaC2+N2=CaCN2+C (3)
экзотермична; ее теплойой эффект ~68 000 cal. Производство Ц. к., всегда сочетаемое с производством карбида, включает следующие технологии. операции: 1) размол карбида, 2) получение азота, 3) азотирование карбида, 4) охлаждение Ц. к., 5) дробление, размол и просеи вание Ц. к., 6) газовыделение (часто также обработка маслом или грануляция) и 7) упаковка продукта. Размол карбида производится в закрытых мельницах в атмосфере азота или дымовых газов; в зависимости от состава карбида к нему добавляют обычно нек-рое количество извести; нередко вводят также CaF2 (до 2%), который понижает t° азотирования. Азот получают фракционировкой жидкого воздуха; он должен быть не ниже 99,7%-ной чистоты и совершенно свободен от карбидной пыли.
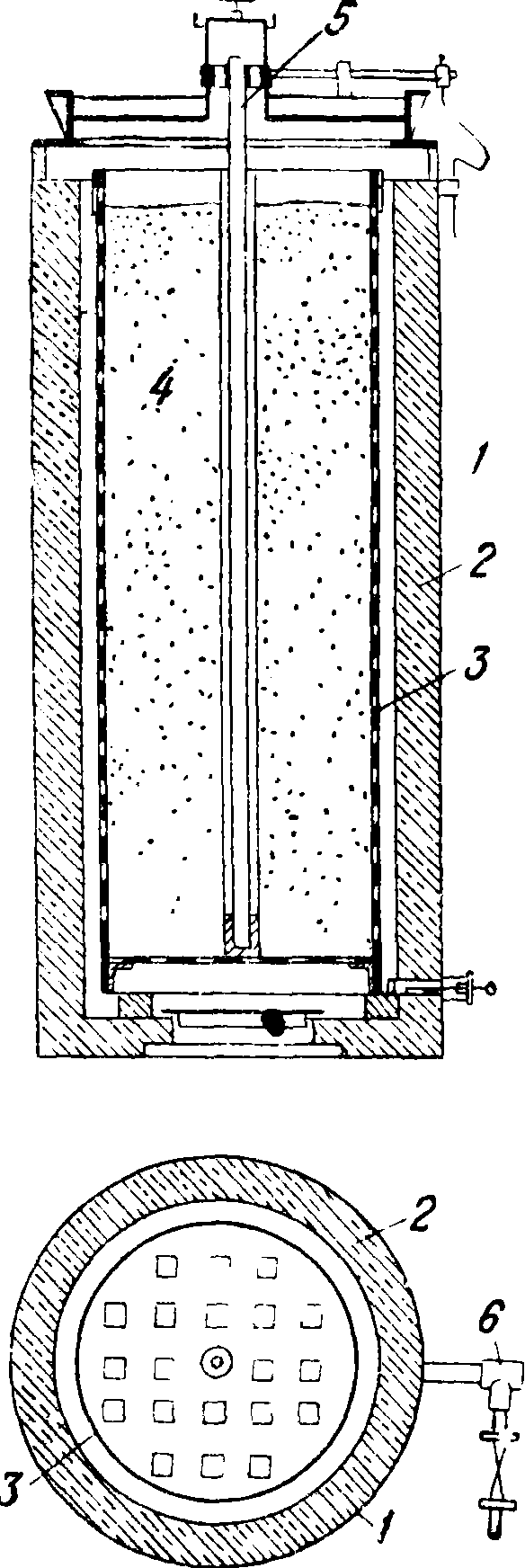
Процесс азотирования в настоящее время ведется почти исключительно в печах Франка-Каро (смотрите фигуру) нериодич. действия, дающих за каждый выпуск 1 -р 5 тонн Ц. к. Печь состоит из железного кожуха 1 с шамотной футеровкой 2; в нее ставится слегка коническая железная корзина 3 с дырчатыми стенками и дном, выложенная бумагой и наполненная карбидной шихтой 4; угольный стержень 5, защищенный бумажной гильзой, является электрическим сопротивлением и служит для предварительного разогревания шихты до начала реакции; азот вводится через трубу 6 в нижнюю часть печи, а избыток его удаляется через отверстие в верхней части. Процесс азотирования длится 24-У 36 ч.; краткое описание его— см. Аммиак. Корзину 3 как наиболее быстро изнашиваемую часть аппаратуры в последнее время часто заменяют простой картонной гильзой такого · же размера. Туннельные печи непрерывного действия, применявшиеся при производстве Ц. к. по методу Польцениуса-Крауса, в настоящее время больше не строятся. Реакция (3) является обратимой при более высоких t°: чем выше t° печи, тем меньше % азота в получаемом продукте. Так, при t° 1 200° устойчив лишь продукт, содержащий не более 21% N, а при t° 1 120°—продукт с 26% N; поэтому при азотировании крайне важно не допускать излишнего перегрева. Готовые блоки Ц. к. извлекают из печей и охлаждают в отдельном помещении на вагонетках; охлажденные блоки разбивают на куски, пропускают через дробилки и затем размалывают в тонкий порошок на шаровых мельницах. Полученный т. о. продукт содержит до 20% свободной СаО и 2—3% непрореагировавшего карбида; при хранении он представляет опасность вследствие образования ацетилена за счет СаС2 и влаги воздуха. Поэтому до выпуска с завода цианамид кальция подвергают операции «газовыделения», обрабатывая его во вращающихся «гидромиксерах» водяной пылью; количество воды дозируется таким образом, чтобы разложить остаточный карбид и погасить всю известь. Чтобы продукт при его употреблении для удобрительных целей не пылил, к нему добавляют обычно ок. 2% минерального масла или каменноугольной смолы; эту операцию можно производить од-( повременно с газовыделением. Иногда вместо ’ отяжеления маслом готовят гранулированный продукт, для ,чего вводят при процессе газовыделения большее количество воды.
Готовый рыночный Ц. к. имеет следующий примерный состав (продукция American Суап-amid Со., 1917 г.): 57% CaCN2, 20% Са(ОН)2, 12% углерода свободного, 3% СаС03, 2% Fe2034-Al203, 2% Si02, 2% связанной Н20, 1% влаги и 1% CaS. Содержание общего азота в продажном Ц. к. колеблется 17-У23%. Расход энергии на 1 тонна Ц. к. (для наиболее крупных установок) равен ~3 000 kWh. Если же учитывать и производство карбида, то для получения 1 килограмм связанного азота в форме CaCN2требуется: 2,8 килограмм кокса, 0,8 килограмм угля (на производство извести для СаС2), ок. 8 килограмм известняка и до 16 kWh энергии. Тара для Ц. к.—двойные мешки (наружный матерчатый, внутренний—из плотной бумаги).
За последнее время разработаны нек-рые новые способы получения Ц. к., представляющие большой технич. интерес. Сюда относится реакция углекислого кальция с аммиаком при t° 600-У8000 (Reitzine):
CaC03 + 4NH3 + C02=2H20+(NH4)2C03 + CaCN2
и в особенности взаимодействие тех же веществ в присутствии окиси углерода (Франк и Гей-ман), идущее по ур-иям:
СаС03=Са0 + С02, со + NH3=HCN+H20, CaO+2HCN=CaCN2 + CO + H?при высокой f и в присутствии CaF2 как катализатора. Получаемый продукт содержит 35% N, то есть представляет почти чистый CaCN2; он подучил название белого Ц. к. Указанные методы уже проверялись в полузаводском масштабе и возможно будут внедрены в промсть.
Заводское производство Ц. к. существует с начала 20 в На 1932 г. имелось по всем странам 38 з-дов с общей производственной мощностью свыше 1 млн. т CaCN2. Нек-рые из этих з-дов законсервированы, остальные работают с неполной нагрузкой. Мировая продукция Ц. к. (в пересчете на чистый азот) равнялась в 1926 году 193 000 т, в 1929 г.— 254 000 т, в 1930 г.—263 ООО т, в 1931 г.—201 000 т, имея тенденцию к дальнейшему снижению. Производственная мощность з-дов Ц. к. на 1931 г. распределялась между главными производящими странами след, образом (в тыс. т азота): Германия—125, США и КанаДа—115, Франция—48, Япония—45, Норвегия—45, Польша—36, Италия—25, Югославия—22.
Применение. Ок. 75% всей продукции Ц. к. используется непосредственно как азотистое удобрение, годное под культуры табака, кукурузы, пшеницы, сахарного тростника, свекловицы, хлопчатника, крестоцветных и бобовых, преимущественно на подзолистых почвах. Другой важной областью применения Ц. к. является переработка его на мочевину (смотрите). Производство аммиака из Ц. к., основанное на реакции
CaCN2+3 Н20=СаС03+ 2NH3 + 23 000 cal
(в автоклавах при t° не ниже 160° и щелочной среде), практиковавшееся в значительных размерах на з-дах 3. Европы и Америки в 1915— 1919 гг., в настоящее BpeMif почти целиком прекращено и не может иметь крупного промышленного значения. Напротив, разрабатываемые сейчас методы получения из Ц. к. цианидов (смотрите Цианистые соединения) имеют все данные к развитью в ближайшем будущем. В небольших размерах Ц. к. перерабатывается на комбинированные удобрения (аммофос, фосфазот), оксалаты, тиомочевину, дициандиамид и гуанидин (используемый в производстве чатых веществ). В США Ц. к. был предложен как средство борьбы с нематодами.
Лит.: Фокин Л., Химия цианамида и его производных, «Труды комиссии по связанному азоту», П., 1920, выл. 4; Андреев И., Исследования в области азотных соединений, там же, П., 1921—1922, вып. 7; Кузнецов Л., Производство карбида и цианамида кальция, М.—Л., 1932; Я н к е Ф., «Химич. промсть и торговля», Берлин, 1923, стр. 20; Цытович Е., «Химич. промсть», Берлин—М., 1926, стр. 51 и 186, Ипатьев В., «ЖХП», 1930, т. 7, стр. 454; Шварц И. и С о л ю с С., «Химстрой», М., 1931, стр. 866; Р а τη е р Е., «Удобрение и урожай», 1929, стр. 73; А х роме и к о А., там же, 1931, стр/728; его же, «ЖХП», 1933, 2у стр. 48; Рабовский Г. иШилова М., там же, 1932, 4У стр. 50 (анализ цианамида кальция); Miinzinger A., Stickstoffkalk, В, 1906; Ргап-k e Е., Cyanamid, Easton, Ра., 1913; Waes er В., Die Luftstickstoff industrie, Lpz., 1922; Vogel J. u. Schulze-Altenburg A., Karbid u. Azetylen als Ausgangsmaterial far Produkte d. chemischen Industrie, Lpz., 1924; Waeser B., Stickstoffindustrie, Dresden—Lpz., 1924; Ernst F., Fixation of Atmospheric Nitrogen, L., 1928 (др. изд. N. Y., 1928); Caro N., Die neueren Grundlagen d. Kalkstickstoffindustrie, В., 1928; Frank Η., M a k k u s W. u. Y a n k e F., Der Kalkstickstoff in Wissenschaft, Technik u. Wirtschaft, Stg., 1931; Ullm. Enz., 2 Aufl., B. 3, p. 1; R e m e 1 6 A. u. Rassow B., «Z. ang. Ch.», 1920, B. 33, p. 139; «MetalIborse», B., 1928, Jg. 18, p. 2637, 1929, Jg. 19, p. 117; Frank H. u. Heimann K., «Z. ang. Ch.», 1931, B. 44, p. 372; Cochet A., ibid., p. 367; Новейшие патенты: Г. Π. 514253, 516445; Ан. Π. 338023, 346463, 364225; Швейц. Π. 142733. В. Янковский.