 > Техника, страница 94 > Электрокапиллярные явления
> Техника, страница 94 > Электрокапиллярные явления
Электрокапиллярные явления
Электрокапиллярные явления, явления, связанные с изменением пограничного натяжения (поверхностного натяжения на границе фаз) между фазами при изменении величины заряда на этой границе. Впервые Э. я. были изучены на системе ртуть—раствор электролита. В теоретич. отношении Э. я. имеют большое значение в связи с вопросом о строении пограничных слоев, о природе эдс на границе металл— раствор и в связи с проблемой нулевого заряда электрода. Практическое значение Э. я. нашли в капиллярном электрометре Липмана-Оствальда. В последнее время делаются попытки применить теорию Э. я. к объяснению ряда технологии, процессов (флотация и др.). Впервые Э. я. были изучены Липманом в конце 19 в Затем Гуи, Нернст и Фрумкин собрали богатый опытный материал и дали теорию этих явлений.
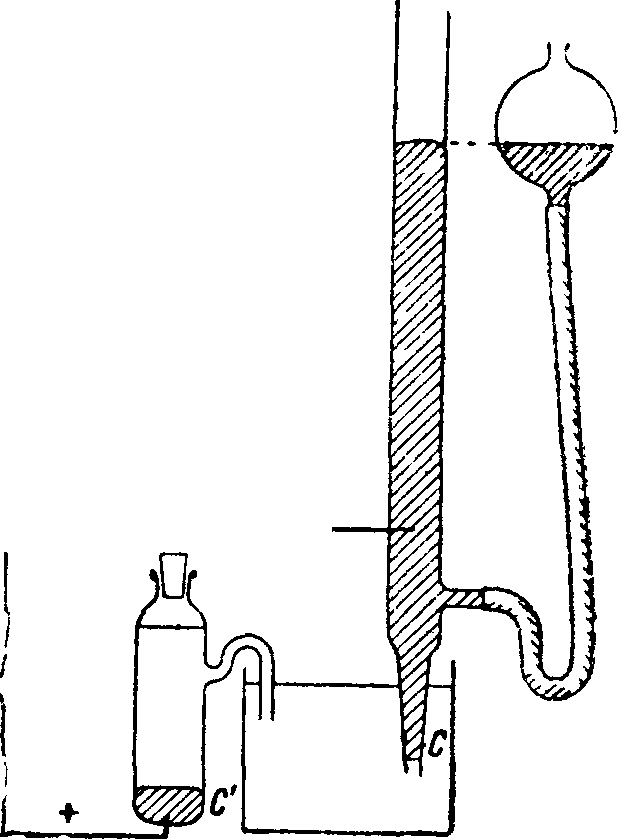
Прибор, в котором проведена большая часть точных электрокапиллярных измерений, называется капиллярным электрометром Гуи.
Принцип его следующий. В растворе, содержащем незначительное количество ионов ртути, находятся 2 ртутных электрода С и С (фигура 1). Поверхность одного из них С Фиг· г большая, другого С—очень маленькая (ртуть в капилляре). Пропусканием слабого тока достигается сильное изменение концентрации ионов ртути в капилляре, то есть сильная концентрационная поляризация малого электрода. Большой электрод практически не поляризуется, т. к. сила тока, приходящаяся на единицу поверхности, здесь примерно в тысячу раз меньше, чем на малом электроде. Зная величину наложенной эдс Е и считая потенциал большого-электрода постоянным, мы получаем относительное значение потенциала капиллярного электрода. Этот электрод устроен так, что одновременно можно определить пограничное натяжение между раствором и ртутью маленького электрода, соответствующее данной поляризации. Опыт показал, что при некотором потенциале пограничное натяжение имеет максимальное значение. При удалении от этого потенциала как в сторону больших, так и в сторону меньших потенциалов натяжение на
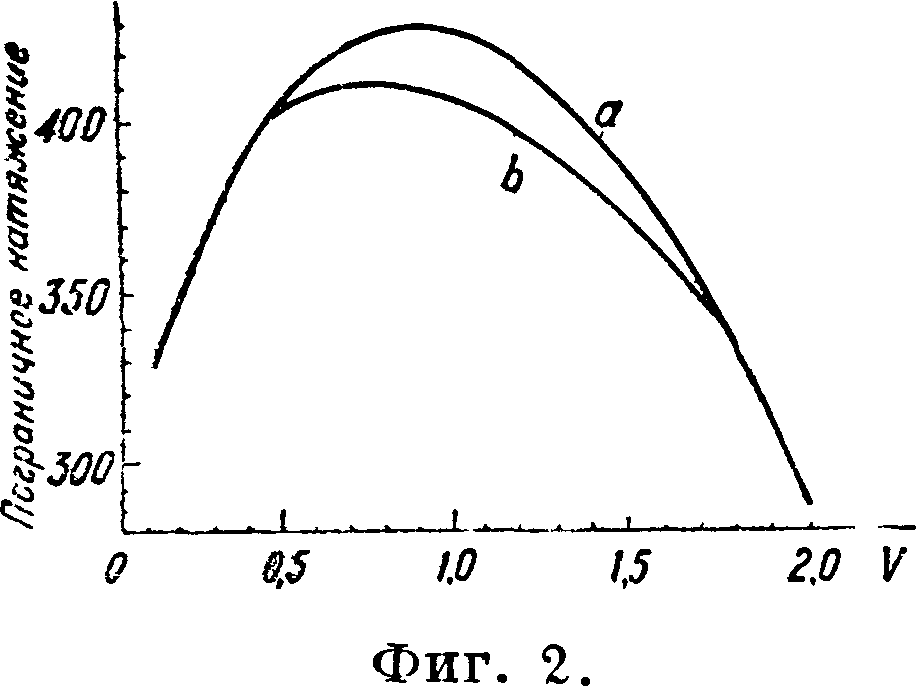
границе металл—раствор понижается. Зависимость пограничного натяжения от скачка потенциала, изображенная графически (так называемая электрокапиллярная кривая), дает более или менее правильную параболу (фигура 2, а).
Если к раствору прибавить какое-нибудь поверхностно-активное (то есть способное адсорбироваться) вещество, то кривая в области максимума теряет свою правильную форму, оказывается сниженной, сам максимум смещается и оказывается уже при ином потенциале (фигура 2. б). Также несколько отличные кривые получаются при переходе от водных растворов к неводным, а также при замене ртути на другие жидкие металлы (галлий), сплавы и амальгамы. Итак оказалось, что все эти кривые имеют вид, б. или м. близкий к параболе с максимумом при разных потенциалах, в зависимости от состава раствора и металлической фазы.
Капельный электрод. В тесной связи с Э. я. стоит другая группа явлений, заключающаяся в изменениях концентрации раствора или возникновении тока при увеличении поверхности металлического электрода. Эти явления наблюдаются при помощи так называемого капельного электрода. Струя ртути вытекает из узкого отверстия и попадает в разбавленный раствор ртутной соли, разбиваясь здесь на мелкие капельки. Концентрация ионов ртути в месте втекания струи ртути в раствор постепенно уменьшается, доходя до определенной величины, после чего она остается постоянной. При этом поверхностное натяжение ртути увеличивается, достигая определенной максимальной величины. Если соединить такой капельный ртутный электрод проволокой с неподвижной ртутью, находящейся на дне сосуда в этом же растворе, то по проволоке пойдет ток, а концентрация ионов изменяться уже не будет. При определенных (очень маленьких) концентрациях ионов ртути нет ни изменения концентрации ни перехода электричества. Эти концентрации точно равны концентрациям, при которых пограничное натяжение ртути, измеренное в электрокапиллярном приборе, имеет максимум.
Теория. Э. я. получили объяснение в связи с теорией Нернста возникновения эдс и теорией адсорбции. По теории Нернста при погружении металла в раствор происходит переход небольшого количества ионов металла в раствор или из раствора в металл. Ионы переходят под действием двух противоположных сил: осмотич. давления ионов металла в растворе и «электролитич. упругости растворения» металла. Перешедшие катионы и оставшиеся в первой фазе анионы (или электроны) притягивают друг друга (останавливая тем дальнейший переход). Таким образом на границе двух фаз получается двойной электрический слой. Граница ведет себя, как конденсатор. Согласно теории Штерна, обкладка этого конденсатора, прилегающая к раствору и образованная притянувшимися из раствора ионами, частично образует плотный слой, находящийся на расстоянии ионного радиуса от металла, отчасти располагается диффузно по больцмановскому закону распределения. При определенной концентрации ионов обе силы (осмотич. давление и упругость растворения) уравновешиваются, и граница металла оказывается незаряженной. Меняя концентрацию ионов в растворе (или концентрационно поляризуя электрод, что то же), можно изменять величину и знак заряда границы металла. Возникновение заряда на границе двух фаз (например металл—раствор) вызывает уменьшение пограничного натяжения. Действительно, пограничное натяжение есть результат притяжения между частицами, находящимися на границе. Если эти частицы электрически заряжены, то между ними происходит электростатич. отталкивание, которое ослабляет их взаимное притяжение, понижая этим поверхностное натяжение. Тому же способствует адсорбция, происходящая на заряженной границе под влиянием электростатических сил. Поверхностное натяжение имеет максимальное значение, когда заряд поверхности (заряд двойного слоя) равен нулю. Аналогичное объяснение получили явления, имеющие место в капельном электроде. Граница между ртутью и раствором непрерывно обновляется за счет отрывания капелек от струи ртути. На новой поверхности происходит образование двойного электрич. слоя с переходом катионов из раствора в металл и притяжением равного количества анионов к поверхности ртути. Т. о. ртутная соль поглощается из раствора и переносится падающими каплями вниз, где опять переходит в раствор, т. к. капли собираются, и общая поверхность уменьшается. Перенос этот будет продолжаться, пока концентрация ионов ртути не уменьшится до величины, при которой осмотическое давление уравновешивает упругость растворения и поверхность ртути перестает заряжаться. Если соединить проволокой капельный электрод с неподвижным, то двойной электрич. слой (его внутренняя обкладка) будет образовываться практически только за счет электричества, притекающего через проволоку. Причина этого явления станет ясна, если мы вспомним, что при увеличении поверхности ртути в капельном электроде в первый же момент происходит поглощение некоторого количества соли ртути из раствора. Образовавшийся концентрационный элемент вызывает протекание тока, уравновешивающего разность концентраций. Измеряя силу этого тока, можно изучить явление количественно. Когда же концентрация ионов таковд, что поверхность ртути не заряжается, увеличение поверхности не вызывает электрич. тока. Это имеет место при том же потенциале ртутного электрода, при котором пограничное натяжение максимально (заряд равен нулю). Таким образом электрокапиллярные явления и явления, происходящие в капельном электроде, основаны на том, что поверхность раздела двух фаз заряжается вследствие адсорбции ионов, причем образуется двойной электрич. слой, влияющий на величину поверхностного натяжения. Количественно связь между поверхностным натяжением и потенциалом двойного слоя выводится из общего условия равновесия на границе фаз, данного Гиббсом. Получается следующая ф-ла:
(и или в интегральном виде:
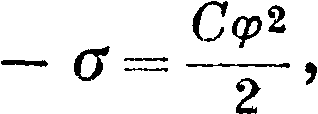
где σ—величина пограничного натяжения при потенциале двойного слоя φ, С—емкость двойного слоя. При интегрировании мы приняли, что С—постоянно. Это правильно в случае крепких растворов чистых электролитов, для которых эта формула хорошо подтверждается опытом. Упомянутое выше снижение поверхностного натяжения в присутствии поверхностноактивных веществ объясняется их адсорбцией на границе металл—раствор. При сильных зарядах поверхности (двойного слоя) адсорбированные молекулы органического вещества вытесняются с поверхности молекулами воды, которые имеют большую диэлектрич. постоянную. Причиной является известное из электростатики втягивание диэлектрика в поле заряженного конденсатора. Следовательно нейтральные молекулы хорошо адсорбируются только при малых зарядах двойного слоя, а смачиваемость металла водой увеличивается при удалении от потенциала, соответствующего нулевому заряду поверхности. Поверхностно-активные ионы (например ион иода) хорошо адсорбируются и при сильных зарядах поверхности в том случае, когда заряды иона и поверхности противоположны.
Строение скачка потенциала. Нулевой заряд двойного слоя наблюдается при весьма различных величинах скачка потенциала металл—раствор. Все это указывает на сложность электрической структуры пограничных слоев, обусловливающей скачок потенциала на границе фаз. Прежние упрощенные представления, принятые в электрохимии со времени классических исследований Нернста и Оствальда, оказались недостаточными. По современным представлениям, развившимся главным образом при изучении Э. я., в образовании того скачка потенциала металл—раствор, к-рый выражается известной ф-лой Нернста, принимают участие: 1) Скачок потенциала внутри метал-лич. фазы около границы (т.н.контактный потенциал). Его образование связано с электронно-ионной структурой металла. 2) Потенциал двойного электрич. слоя на границе фаз, о котором говорилось выше. 3) Скачок потенциала в растворе близ границы. Последний скачок обусловливается наличием на поверхности металла слоя вещества, адсорбированного специфически (то есть не электростатич. силами). Адсорбированные молекулы обычно полярны, то есть с одного конца молекула имеет избыток электричества положительного, с другого—отрицательного, и притом молекулы адсорбируются определенным концом. Поэтому слой адсорбированных молекул и создает свой скачок потенциала. Специфически адсорбироваться могут и молекулы растворителя, например воды. При максимальном поверхностном натяжении (или при отсутствии зарядного тока в капельном электроде) нулю равен только заряд двойного слоя, но никак не весь нерн-стовский скачок потенциала металл—раствор, как это представляли до последнего времени. Следовательно Э. я. не дают способа определения истинной величины скачка потенциала отдельного электрода.
Применение. Э. я. получили практич. применение в капиллярном электрометре Липмана-Оствальда, нашедшем широкое распространение в лабораторной практике. Электрометр служит для обнаружения весьма слабых токов, главным образом при определении эдс методом компенсации, давая возможность найти на шка ле мостика такое положение подвижного контакта, при к-ром через электрометр и измеряемую цепь ток совсем не идет. Т. о. капиллярный электрометр служит т. н. нулевым инструментом. Сосуд электрометра (фигура 3) наполнен ртутью и 10%-ным раствором серной кислоты и запаян. К ртути в двух местах подводятся впаянные в стекло платиновые контакты. Нагибанием сосуда ртуть переливается в другую часть, пока не установится на половине высоты капилляра. При пропускании тока через электрометр вследствие поляризации изменяется поверхностное натяжение ртути в капилляре. В зависимости от направления тока заряд поверхности уменьшается или увеличивается, и поверхностное натяжение увеличивается или уменьшается, и столбик опускается или поднимается. Неподвижность наблюдаемого в микроскоп столбика указывает на отсутствие тока. Через электрометр можно пропускать только очень слабые токи. При сильном токе, если ртуть в капилляре оказывается катодом, на ней может образоваться пузырек водорода, и столбик перестанет Фигура з. двигаться. Еще более портится электрометр при сильном или продолжительном токе в противоположном направлении (когда мениск заряжен положительно). В капилляре при этом может выделиться в крист сернокислая ртуть. Восстановить подвижность ртути в этом случае можно пропусканием слабого тока в обратном направлении (чтобы столбик в микроскопе поднимался). Также помогает переливание ртути из одной части прибора в другую. За исключением момента измерения электрометр должен быть всегда замкнут сам на себя при помощи особого ключа.
Связь Э. я. с некоторыми технич. проблемами начали изучать только недавно (Фрумкин). Влияние заряда на смачивание и адсорбцию надо учитывать при изучении механизма флотации (смотрите). В последнее время в этом направлении ведутся работы с помощью метода краевых углов. Применение теории Э. я. осветило также вопрос о механизме электролитического обезжиривания металлов. Выяснилось также, что прочность прилипания пузырьков газа к электроду при электролизе и величина пузырьков при отрыве их определяются Э. я.
Лит.: Фрумкин А., Элекгрокапиллярные явления и электродные потенциалы, Одесса, 1919; Мюллер Э., Электрохимический практикум, пер. с нем.,4 изд., М.—Л., 1927; Kremann R. и. Μ и 1 1 е г R., Handbuch d. allg^meinen Ohemie, hrsg. v. W. Ostwald, C. Drucker u.
P. Walden, В. 8, T. 1, Lpz., 1930; Freundlich H., Kapillarcbemie, 4 AiifL, В. 1, Lpz., 1930; F г и m k i n A., Die Elektrokapillarknrve, «Ergebnisse d. exakten Natur-wissenschaften», B., 1928, B. 7. Б. Кабанов.